Публикация доступна для обсуждения в рамках функционирования постоянно
действующей интернет-конференции “Бутлеровские чтения”. http:///readings/
УДК 547.541.51:542.938: 542.944: 541.544. Поступила в редакцию 21 сентября 2006 г.
Одноэлектронный перенос в SNS-реакциях ароматических производных серы различной валентности и sp2-атоме углерода
©
Кафедра органической и биологической химии. Ивановский государственный университет.
Ул. Ермака, 39. г. Иваново, 153025. Россия. Тел.: (4932) 37-37-03. E-mail enk2005@rambler.ru
Ключевые слова: сульфонилгалогениды, SNS-реакции, одноэлектронный перенос, квантовохимический расчет,
сродство к электрону.
Аннотация
С позиций теории одноэлектронного переноса проведен анализ реакций нуклеофильного замещения на атоме сульфонильной серы и ее низковалентных аналогах в их ароматических производных в сопоставлении с аналогичными процессами на sp2-атоме углерода. Показана возможность реализации в этих реакциях механизма одноэлектронного переноса (SET). Смещение механизма реакции в сторону механизма SN2, обнаруживаемое корреляциям по Гаммету и диаграмме О'Феррала, увеличивает вероятность реализации SET-механизма. Реакционная способность органических производных S(IV) и S(VI) соответствует концепции Пирсона, при этом локализованные (жесткие) и делокализованные (мягкие) нуклеофилы образуют с этими соединениями отдельные реакционные серии. Соблюдение соотношения активность/селективность для замещения на атоме сульфониль-ной серы и формальное нарушение его для аналогичного процесса на S(VI) объяснено переносом реакционного центра при изменении жесткости нуклеофилов. Реакционная способность соединений S(II) описана на основе теории возмущений.
Введение
Реакции нуклеофильного замещения у сульфонильного атома серы (SNS) (1) в производных аромати-ческих сульфокислот представляют собой частный случай процессов нуклеофильного замещения.
ArSO2X + :Nu - → ArSO2Nu + :X - (1)
Здесь Nu – нуклеофильный реагент (нейтральная молекула, содержащая атом с неподеленной парой электронов, или анион), ArSO2X – субстрат, в котором Ar – ароматический или гетероароматический радикал, X – уходящая группа (галоген, OSO2Ar, SO2Ar, OAr).
SN-реакции на sp3-гибридном атоме углерода исследованы достаточно детально [1] и их закономерности перенесены на аналогичные процессы с участием атомов углерода в состоянии sp2 и некоторых гетероатомов в качестве реакционных центров. В частности, представления о механизмах SN2, SN1 и SAN, диаграмма О'Феррала, правила Торнтона [2] и Харрис-Курц [3] разработаны для реакций галогеналканов и распространены на процессы с участием атомов серы, фосфора и кремния [4].
Считается, например, что SN1-механизм замещения в ArSO2X менее вероятен, чем в производных карбо-новых кислот ArCOX, поскольку катион ArSO2+ менее устойчив, чем ArCO+ [5]. Известно, что механизмы SN2 [5] и SAN [6] для этих соединений кинетически трудно различимы, однако основный и нуклеофильный механизмы катализа сольволиза сульфонилхлоридов (в частности, PhSO2Cl) успешно разделены [7].
Для взаимодействия ядернозамещенных 2-тиофенсульфонилхлоридов (I) с анилином [8] обсуждаются эффекты растворителя в приближении многопараметрической корреляции и предполагается реализация меха-низма SAN. Стадией, определяющей скорость в протонных растворителях, предполагается образование связи S-Nu, а в апротонных – разрыв связи S-X (где X – галоген, уходящая группа). Предполагается [9], что в бинарных растворителях (MeOH-MeCN) эти соединения реагируют с нуклеофилами (AcO-, NO2-, OH-, N3-, и рядом нейтральных – анилин и пиридин) по механизму SN2, варьирующемуся от SN1 до SAN в зависимости от нуклеофила, заместителя и уходящей группы, что обсуждается с привлечением диаграммы О'Феррала, корреляций по Гаммету и соотношения Бренстеда. Механизм присоединения-отщепления предполагается для реакции 3-тиофенсульфонилхлорида с анилином в метаноле, где стадией, определяющей скорость, является нуклеофильная атака анилина [10]. Реакционная способность I в реакции с нуклеофилами в различных средах и изотопные эффекты в D2O обсуждаются на основе анализа по Бренстеду, Ритчи и Эдвардсу [11]. Cульфонильная (A), сульфинильная (B) и сульфониевая (C) уходящих групп располагаются по нуклеофугности в ряд C > B > A [12], соответствующий механизму SN2. Вариант механизма SAN согласуется [13] с величинами σ-констант для атома S в тиофене, полученными из кинетических данных взаимодействия I с анилином в метаноле и сопоставленных с аналогичными величинами для атома кислорода в кольце фурана, полученных по величинам pKa соответствующих карбоновых кислот.
Четвертый механизм – не рассматриваемый в цитированных выше работах – подобен механизму SN2, однако движение :Nu - относительно RSO2X при переносе электронной плотности с ВЗМО(:Nu-) на НСМО (RSO2X) при его реализации отсутствует, поэтому перенос заряда происходит при «замороженной» конфигурации частиц. Этот механизм называется механизмом одноэлектронного переноса (single electron transfer, SET) [14]. Соотношение между SN2 и SET-реакциями является одним из основных современных вопросов физической органической химии [15]. Для SNS-реакций данный вопрос практически не рассматривался [16], а для процессов SEAr в ароматическом ряду (которые можно отнести к нуклеофильному замещению на гетероатомах – например, на атоме азота при нитровании) SET-механизм впервые предложен и развит в работах, цитированных в [17].
Реализацию переходного состояния (transition state, TS) процесса нуклеофильного замещения [18] (2) можно представить как SET-процесс c предельными структурами с переносом спиновой плотности (3), вклю-чающий вертикальный перенос заряда с ВЗМО нуклеофила (Nu) на НСМО электрофила (субстрата RX, S) (по разрыхляющей орбитали связи C-X) с последующим схождением реакционного комплекса по поверхности потенциальной энергии (ППЭ) возбужденного состояния и возвратом на ППЭ основного. Соответствующие диаграммы корреляции состояний приведены в [14, 19-21] и на рис. 1.
R-X + Nu - → [Nu....R....X]- → Nu-R + X - (2)
R-X + :Nu - à [R* - X-…Nu*] à [R* -Nu - + * X] à R-Nu + X - (3)
Ea = Ec - B = f ∙ [IP(Nu) - EA(S)] – B (4)
Активационный барьер (Ea, ΔG≠) в теории SET пропорционален барьеру вертикального одноэлектронного переноса, который равен разнице между вертикальным потенциалом ионизации нуклеофила IP(Nu) и электронным сродством субстрата EA(S) [19]) (4). Здесь B – резонансная энергия стабилизации переходного состояния, представляющего собой гибрид основного и первого возбужденных состояний с различным вкладом каждого, Ec – высота энергетического барьера в точке пересечения диаграмм состояний. Коэффициент f интерпретируется как индекс задержки образования связи C-Nu. Параметр f > 0, поскольку увеличение электронного сродства субстрата облегчает электронный перенос. Вертикальный потенциал ионизации используется вследствие переноса электрона при "замороженной" геометрии частиц в комплексе столкновения [20]. Представления о SET как вероятном процессе в реакциях замещения вообще и нуклеофильного замещения в частности развиты теоретически и проверены экспериментально [19-22].
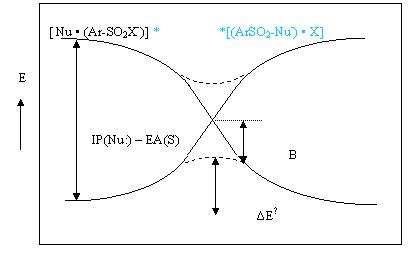 |
Рис. 1. Диаграмма корреляции состояний для механизма одноэлектронного переноса
Результаты и их обсуждение
1. Реакции присоединения по карбонильной группе
На примере нуклеофильных Ad-реакций по группе С=O, где нуклеофильная атака на карбонильный атом углерода является определяющей скорость (5), было показано [22], что корреляции между Ea (ΔG≠) и IP(Nu), близкие к линейным с удовлетворительными коэффициентами корреляции, распадаются на две – для локализо-ванных (ΔG≠лок) и делокализованных (ΔG≠дел) нуклеофилов соответственно. Параметры корреляций (6-8) в табл. 1 для реакций нуклеофилов с 2,4-динитрофенилацетатом [R1 = Me, R2 = 2,4-(NO2)2PhO] определены по данным [22].
+ H+
R1R2С=O + Nu - à R1R2C(Nu)O - à R1R2C(Nu)OH (5)
Табл. 1. Корреляции ΔG≠ и IP(Nu) для реакий нуклеофильного присоединения по карбонильной группе
2,4-(NO2)2PhOCOCH3: Y = a*IP(Nu) + b (ΔG≠ и IP – ккал/моль). Локализованные нуклеофилы:
HOO-, ClO-, MeO-, CF3CH2O-, CN-, HO-, F-. Делокализованные нуклеофилы: PrS-, PhO-, PhS-, ONO-, N3-, AcO-.
N | Y | a±s(a) | B±s(b) | R*) | Sad | N | tкрит | ttэксп |
(6) | ΔG≠лок | 0.16± 0.02 | -13.5 ± 3.0 | 0.97 | 0.88 | 7 | 11.55 | 2.4 |
(7) | ΔG≠дел | 0.39±0.11 | - 45.7 ± 18.8 | 0.87 | 2.01 | 6 | 4.22 | 2.57 |
(8) | lnK1 | 7.58±1.02 | -1.12±0.07 | 0.97 | 0.25 | 4 |
*) Здесь и далее коэффициенты корреляции проходят проверку на статистическую
значимость по критерию Стьюдента (t) при степени риска 5% (tэксп > tкрит) [23]).
В данной реакционной серии соблюдается соотношение реакционная способность/селективность, так как чувствительность реакции к изменению IP(Nu) (dΔG≠/dIP(Nu) для локализованных нуклеофилов ниже (0.16), чем для делокализованных (0.39), а активность их выше (ниже активационный барьер), поскольку карбонильный атом углерода является жестким реакционным центром. Поэтому в реакции с жесткими нуклеофилами электронная поддержка с их стороны имеет меньшее значение, а реакция идет быстрее.
2. Реакции ядернозамещенных тиофенсульфонилхлоридов

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



