Реакция Фоля (на аминокислоты, содержащие слабосвязанную серу).
Принцип метода. Основан на щелочном гидролизе сульфгидрильных групп SH белка с последующим отщеплении серы в виде сульфида свинца (PbS) черно-бурого цвета (см. уравнение).
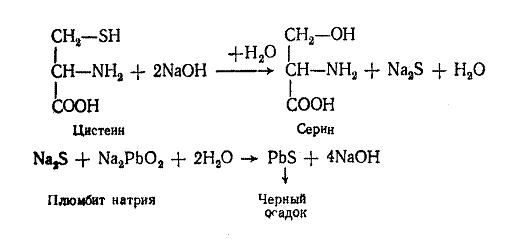
ВНИМАНИЕ! Соблюдать меры безопасности при работе с реактивом Фоля (содержит NaOH и Na2PbO2).
Ход работы. В три пробирки наливают по 5 капель растворов: в 1-ю – яичного белка, во 2-ю – желатина, в 3-ю – миозина. В каждую пробирку добавляют по 5 капель реактива Фоля. Затем интенсивно кипятят и дают постоять 1–2 мин. При этом в 1-й и в 3-й пробирках образуется черный или бурый осадок сульфида свинца. Желатин осадка не образует, т. к. в нем нет серосодержащих аминокислот.
Выводы по результатам работы.
_________________________________________________________________________________________________________________________________________________________________________________________________
Лабораторная работа № 2. Реакции осаждения белков
Осаждение белков при кипячении.
ВНИМАНИЕ! Соблюдать меры безопасности при работе с нагреванием пробирок.
Ход работы. В 5 пробирок наливают по 5 капель раствора белка. Первую пробирку нагреть до кипения. Жидкость мутнеет, т. к. разрушаются водные оболочки вокруг молекулы белка, и происходит укрупнение его частиц. Мицеллы белка несут заряд и удерживаются во взвешенном состоянии.
Во 2-й пробирке нагреть раствор до кипения и добавить 2 капли 1 %-го раствора уксусной кислоты до слабого подкисления. При отстаивании выпадает осадок белка. Частицы белка теряют заряд и приближаются к изоэлектрическому состоянию.
В 3-ю пробирку добавить 5 капель уксусной кислоты для сильнокислой реакции среды. При кипячении жидкости осадка не образуется, поскольку белковые мицеллы перезаряжаются и несут положительный заряд, что повышает их устойчивость.
В 4-ю пробирку налить 5 капель раствора уксусной кислоты, 2 капли насыщенного раствора хлористого натрия и нагреть. Выпадает белый хлопьевидный осадок, т. е. частицы белка теряют заряд.
В 5-ю пробирку добавить 2 капли раствора гидроксида натрия. При кипячении осадок не образуется, т. к. в щелочной среде отрицательный заряд на частицах белка увеличивается.
Выводы по результатам работы.
_________________________________________________________________________________________________________________________________________________________________________________________________
Осаждение белков концентрированными минеральными кислотами.
ВНИМАНИЕ! Соблюдать меры безопасности при работе с концентрированными азотной и серной кислотами.
Ход работы. В 2 пробирки наливают по 10 капель концентрированных кислот: азотной и серной. Наклонив пробирки под углом 45 градусов, осторожно по стенке пробирки приливают равный объем раствора белка так, чтобы обе жидкости не смешивались. На границе двух жидкостей образуется осадок в виде небольшого белого кольца. При добавлении избытка азотной кислоты осадок не исчезает, а при добавлении серной кислоты осадок растворяется.
Выводы по результатам работы.
_________________________________________________________________________________________________________________________________________________________________________________________________
Осаждение белков органическими растворителями.
Ход работы. В 2 пробирки вносят по 5 капель раствора белка и прибавляют по 15–20 капель этилового спирта и ацетона.
Выводы по результатам работы.
_________________________________________________________________________________________________________________________________________________________________________________________________
Осаждение белков органическими кислотами.
ВНИМАНИЕ! Соблюдать меры безопасности при работе с трихлоруксусной кислотой.
Ход работы. В две пробирки наливают по 5 капель раствора белка и добавляют по 2 капли раствора ТХУ (трихлоруксусной кислоты) в одну и 2 капли сульфосалициловой – в другую. Следят за изменением растворов.
Выводы по результатам работы.
________________________________________________________________________________________________________________________________________________________________________________________________
_
_
_
Лабораторная работа № 3. Разделение альбуминов и глобулинов методом высаливания (УИРС)
Принцип метода. Основан на обратимой реакции осаждения белков из растворов с помощью высоких концентраций нейтральных солей (NaCl, NH4Cl, MgSO4 и др.).
Ход работы. К 1 мл неразведенного яичного белка добавляют 1 мл насыщенного раствора сульфата аммония и перемешивают. Получается полунасыщенный раствор сульфата аммония, в котором выпадает осадок яичного глобулина. Через 5 мин осадок отфильтровывают, в фильтрате остается яичный альбумин. Для высаливания альбуминов к фильтрату добавляют порошок сульфата аммония до полного насыщения, т. е. пока новая порция порошка остается нерастворенной. Выпавший осадок альбумина отфильтровывают. С фильтратом проделывают биуретовую реакцию. Отрицательная реакция указывает на отсутствие белка.
Выводы по результатам работы.
_________________________________________________________________________________________________________________________________________________________________________________________________
_
_
Рекомендуемая литература
Основная
1 Кухта, В. К и др. Биологическая химия: учебник / , , ; под ред. . – Минск: Асар, М.: Издательство БИНОМ, 2008. – С. 45-46, 54-60.
2 Биохимия: Учебник для вузов / Под ред. . – 4-е изд., испр. – М.: ГЭОТАР-Медиа, 2006. – С. 9-73, 75-80, 83-92.
3 Филиппович, Ю. Б. Основы биохимии. – 4-е изд. – М.: Агар, 1999. – С. 49-78, 95-105.
4 Николаев, А. Я. Биологическая химия. М.: Медицинское информационное агентство, 2004. – С. 61-63, 68-78.
5 и др. Биохимия человека: в 2-х т.: Пер. с англ., М.: Мир, 2004. – Т.1: С. 47-51, 63-66, 79-81.
Дополнительная
6 Березов, Т. Т. Биологическая химия / , . – М.: Медицина, 1998. – С. 114-143.
7 Ленинджер, А. Л. Основы биохимии. М.: Мир, 1985. Т. 1. С. 226–302.
8 , Биоорганическая химия, М.: Медицина, 1991. С. 313–376.
9 и др. Молекулярная биология клетки. М.: Мир, 1994. Т. 1. С. 113–171.
Занятие 4
Ферменты-2. Механизм действия ферментов
Цель занятия: закрепить знания по структуре ферментов, сформировать представления о механизме действия ферментов. Научиться выполнять качественные реакции на активность некоторых гидролитических ферментов.
Исходный уровень знаний и навыков
Студент должен знать:
1 Теоретические основы химической кинетики.
2 Строение моносахаридов. Качественные реакции на альдегидные и спиртовые группы.
3 Строение полисахаридов. Свойство и качественные реакции.
4 Механизм образования шиффовых оснований.
5 Строение и механизм катализа коферментами NAD+ и NADP+.
Студент должен уметь:
1 Проводить качественные реакции на продукты ферментативного гидролиза.
Структура занятия
1 Теоретическая часть
1.1 Свойства ферментов (термолабильность, специфичность и др.). Механизм действия ферментов. Этапы взаимодействия фермента и субстрата. ишера, Д. Кошланда и современные взгляды.
1.2 Теория промежуточных соединений. Основы термодинамики катализа. Энергия активации. Энергетический барьер.
1.3 Кинетика ферментативных реакций (факторы, влияющие на скорость ферментативных реакций: природа фермента и субстрата, их концентрация, pH, температура, лекарственные препараты и др.). Константа Михаэлиса (Km) – определение, физическое значение.
1.4 Регуляция активности ферментов. Роль гормонов, цАМФ, активаторов, ингибиторов.
1.4.1 Регуляция активности путем химической модификации ферментов (ограниченный протеолиз, фосфорилирование, метилирование и др.).
1.5 Виды ингибирования.
1.6 Аллостерическая регуляция. Свойства аллостерических ферментов.
2 Практическая часть
2.1 Решение задач и проведение контроля конечного уровня знаний.
2.2 Лабораторные работы.
Задачи
1 При увеличении концентрации субстрата скорость ферментативной реакции...
а) сначала возрастает, затем падает;
б) не изменяется;
в) сначала возрастает, затем стабилизируется на постоянном уровне;
г) непрерывно возрастает пропорционально концентрации субстрата;
д) сначала убывает, затем возрастает?
2 Температурный оптимум для большинства ферментов находится в диапазоне:
а) от 36 до 38°C; б) от 40 до 44°C; в) от 30 до 34°C; г) от 0 до 8°C?
3 Энергия активации – это…
а) энергия, необходимая для перевода всех молекул фермента в активированное состояние;
б) энергия, необходимая для перевода всех молекул субстрата в активированное состояние;
в) разница величин энергий субстратов и продуктов реакции;
г) общая энергия системы?
4 Взаимодействие, описываемое выражением «как рука к перчатке»:
а) субстрат + активный центр;
б) ингибитор + активный центр;
в) регулятор + аллостерический центр;
г) якорная площадка + каталитическая площадка?
5 Активность ЛДГ при увеличении температуры с 30 до 40°C:
а) не изменится; б) станет равной нулю; в) уменьшится в 2-4 раза; г) увеличится в 2-4 раза; д) возрастет в 10 раз?
6 Активность АсАТ при постепенном изменении температуры с 30 до 70°C:
а) сначала увеличится, затем резко снизится; б) не изменится; в) увеличится в среднем в 32 раза; г) немедленно упадет до нуля; д) будет постепенно нарастать?
7 Константа Михаэлиса – это…
а) молярный коэффициент экстинкции фермента;

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



