а) 3 АТФ; б) 6 АТФ; в) 9 АТФ; г) 12 АТФ; д) 15 АТФ?
Лабораторные работы
Лаборатоpная работа № 1. Открытие некоторых субстратов ЦТК (лимонной и янтаpной кислот)
Принцип метода. Ди - и трикарбоновые кислоты, карбоксильные группы которых расположены рядом, при взаимодействии с резорцином и концентрированной серной кислотой образуют флюоресцирующие в ультрафиолетовом свете продукты.
ВНИМАНИЕ! Соблюдать меры безопасности при работе с источником ультрафиолетового излучения, концентрированной серной кислотой и нагреванием на спиртовке.
Ход работы. В две пробирки добавляют по 1 капле воды (избыток воды мешает реакции) и растворяют: в 1-й – несколько кристаллов цитрата, а во
2-й – янтарной кислоты. Затем в обе пробирки вносят по 10–12 капель концентрированной серной кислоты и несколько кристаллов резорцина. Содержимое пробирок осторожно нагревают (но НЕ КИПЯТЯТ!) до появления окраски желтого цвета. К охлажденным пробиркам добавляют по 20 капель дистиллированной воды и наблюдают в ультрафиолетовом свете флюоресценцию: голубую – в пробирке с цитратом и зеленую – с сукцинатом.
Выводы по результатам работы.
_________________________________________________________________________________________________________________________________________________________________________________________________
_
_
_
Лаборатоpная работа № 2. Качественное обнаружение цитохромоксидазы.
Принцип метода. Цитохромоксидаза, содержащаяся в скелетной мышце, обесцвечивает 2,6-дихлорфенолиндофенол (2,6-ДХФИФ, краска Тильманса), переводя его в восстановленную форму (см. уравнение):
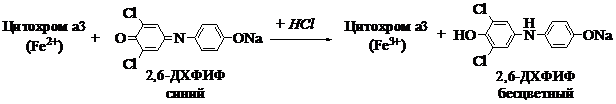
Ход работы. 1 г свежих скелетных мышц, освобожденных от жировой ткани, тщательно растирают в ступке в течение 10 мин. Мышечную кашицу фильтруют через слой марли и многократно промывают твердый осадок дистиллированной водой до обесцвечивания промывных вод.
На мышечную кашицу, отжатую между листами фильтровальной бумаги, капают 2-3 капли раствора 2,6-ДХФИФ и наблюдают его обесцвечивание, связанное с активностью цитохромоксидазы мышечной ткани (восстановление краски Тильманса в лейкоформу).
Выводы по результатам работы.
_________________________________________________________________________________________________________________________________________________________________________________________________
_
_
_
Рекомендуемая литература
Основная
1 Кухта, В. К и др. Биологическая химия: учебник / , , ; под ред. . – Минск: Асар, М.: Издательство БИНОМ, 2008. – С. 96-97, 99-101, 131-139, 178-182.
2 Биохимия: Учебник для вузов / Под ред. . – 4-е изд., испр. – М.: ГЭОТАР-Медиа, 2006. – С. 126-127, 264-274, 281-294.
3 Филиппович, Ю. Б. Основы биохимии. – 4-е изд. – М.: Агар, 1999. – С. 161-164, 355-357, 423, 411-417.
4 Николаев, А. Я. Биологическая химия. М.: Медицинское информационное агентство, 2004. – С. 66-68, 128, 172-177, 235-247.
5 и др. Биохимия человека: в 2-х т.: Пер. с англ., М.: Мир, 2004. – Т.1: С. 111-124, 172-180, 278-280.
6 Березов, Т. Т. Биологическая химия / , . – М.: Медицина, 1998. – С. 345–353.
Дополнительная
7 Основы биохимии. М.: Мир, 1985. Т. 2. С. 477–507.
Занятие 7
Биологическое окисление-2. Тканевое дыхание.
Окислительное фосфорилирование.
Микросомальное и перекисное окисление
Цель занятия: сформулировать современные представления о механизмах получения, депонирования и утилизации энергии в живых организмах, путях потребления кислорода в организме в норме и при патологии.
Исходный уровень знаний и навыков
Студент должен знать:
1 Понятие об электродвижущей силе окислительно-восстановительных реакций.
2 Строение NAD+, NADP+, FAD, FMN, кофермента Q, цитохромов и их роль в окислительно-восстановительных процессах.
3 Строение дыхательной цепи и принципы ее функционирования.
4 Электронное строение атома кислорода и его активных форм.
5 Сущность свободнорадикальных процессов.
Студент должен уметь:
1 Проводить титрационный анализ.
Структура занятия
1 Теоретическая часть
1.1 Окислительное фосфорилирование (ОФ). Пункты фосфорилирования. Коэффициент P/О ‑ показатель степени сопряжения ОФ. Механизмы сопряжения окисления и фосфорилирования. Хемиосмотическая теория сопряжения окислительного фосфорилирования П. Митчелла. Разобщение окисления и фосфорилирования. Разобщители, виды, их механизм действия. Биологическое значение разобщения ОФ.
1.2 Значение тканевого дыхания в биоэнергетике клетки и организма. Энергетический баланс одного оборота ЦТК.
1.3 Микросомальное окисление. Понятие о микросомах. Характеристика ЭПС. Микросомальная ДЦ. Основные переносчики: NAD+, NADP+, FAD и FMN ‑ зависимые дегидрогеназы, цитохромы b5, P450, их функции. Субстраты и косубстраты микросомального окисления (метаболизм ксенобиотиков).
1.4 Сходство и отличие микросомальной и митохондриальной ДЦ. Связь ЦТК, ДЦ митохондрии с микросомальной ДЦ. Биологическое значение и органное распределение микросомального окисления.
1.5 Перекисное окисление. Электронное строение атома кислорода. Механизмы образования активных форм кислорода. Перекисное окисление в норме и при патологии. Субстраты перекисного окисления. Антиоксидантная защита (АОЗ): ферментная (СОД, каталаза, пероксидаза и др.) и неферментная (глутатион, витамины А, С, Е, метаболиты, и др.). Витамины A, C, E их строение и роль в обмене.
1.6 Окислительный стресс как результат нарушения баланса между реакциями перекисного окисления и системой АОЗ.
2 Практическая часть
2.1 Решение задач.
2.2 Лабораторная работа.
2.3 Проведение контроля конечного уровня знаний.
Задачи
1. Фермент, который осуществляет перенос электронов непосредственно на кислород:
а) гексокиназа; б) супероксиддисмутаза; в) пероксидаза; г) цитохромоксидаза?
2. Компонент цепи переноса электронов и протонов, который собирает электроны от разных субстратов окисления:
а) НАДН-дегидрогенеза; б) цитохром c; в) убихинон (КоQ)?
3. Разобщение дыхания и фосфорилирования достигается при:
а) повышении проницаемости внутренней мембраны митохондрий для протонов;
б) снижении активности Н+ зависимой АТФ-азы;
в) ингибировании АДФ-АТФ транслоказы?
4. Атомы и железа, и меди входят в активный центр фермента...
а) цитохрома c; б) цитохромоксидазы; г) НАДН-дегидрогеназы; д) убихинолдегидрогеназы; е) сукцинатдегидрогеназы?
5. Убихинон легко диффундирует в мембране митохондрий, потому что является...
а) небольшой гидрофильной молекулой;
б) небольшой липофильной молекулой;
в) крупной липофильной молекулой;
г) крупной гидрофильной молекулой?
6. Коэффициентом фосфорилирования называется:
а) отношение количества связанной Н3РО4 к количеству поглощенного О2;
б) отношение объемов образующегося СО2 и поглощаемого О2;
в) отношение количества энергии, аккумулированного АТФ, к энергии, высвободившейся при окислении?
7. Разобщитель окислительного фосфорилирования:
а) токоферол; б) динитрофенол; в) цианистый калий; г) амитал?
8. Согласно хемиосмотической теории протоны «возвращаются» из межмембранного пространства в матрикс митохондрий:
а) при помощи ферментов дыхательной цепи;
б) в любом месте мембраны по градиенту концентрации;
в) через протонную АТФ-синтазу?
9. В метаболизме чужеродных соединений участвует фермент:
а) супероксиддисмутаза; б) цитохром b; в) цитохром c1; г) цитохром Р450; д) сукцинатдегидрогеназа?
10. Протонная АТФ-синтаза для образования АТФ использует энергию:
а) трансмембранного протонного градиента;
б) макроэргической связи промежуточного соединения;
в) заключенную в НАДФН?
11. Фермент микросомального окисления цитохром Р450 локализован в…:
а) митохондриях; б) рибосомах; в) лизосомах; г) эндоплазматической сети?
12. Фермент, защищающий клетку от токсического действия кислорода:
а) НАДН-дегидрогеназа; б) моноаминооксидаза; в) цитохромоксидаза; г) супероксиддисмутаза?
13. Ингибитор перекисного окисления липидов (ПОЛ):
а) токоферол; б) цианистый калий; в) тироксин; г) арахидоновая кислота; д) пируват?
14. Угарный газ (СО) нарушает биоэнергетические процессы, потому что блокирует:
а) АТФ-синтазу; б) цитохромоксидазу; в) цитохром b; г) сукцинатдегидрогеназу?
15. Разобщители нарушают синтез АТФ, потому что:
а) блокируют АТФ-синтазу;
б) уменьшают трансмембранный потенциал;
в) ингибируют цитохромоксидазу;
г) разрушают митохондрии?
Лабораторная работа. Количественное определение каталазы по Баху и Зубковой
Принцип метода. Основан на титриметрическом определении количества перекиси водорода, расщепленной ферментом за определенный промежуток времени, по следующему уравнению:
2KMnO4 + 5H2O2 + 3H2SO4 ¾® K2SO4 + 2MnSO4 + 8H2O + 5O2
2KMnO4 + 5H2O2 + 4H2SO4 ¾® 2KHSO4 + 2MnSO4 + 8H2O + 5O2
KMnO4+H2O2+H2SO4 ® O2+MnSO4+K2S +H2O
О количестве расщепленной перекиси водорода судят по разности количества KMnO4, израсходованного на титрование до и после действия каталазы.
Активность каталазы выражают с помощью каталазного числа и показателя каталазы. Каталазным числом называют количество миллиграммов перекиси водорода, которое разлагается в 1 мкл крови.
Ход работы. Разведенную кровь (1 : 1000) взбалтывают и добавляют по 1 мл в две колбы, приливают по 7 мл дистиллированной воды; в опытную пробу добавляют 2 мл 1 % раствора H2O2, а в контрольную – 5 мл 10 % раствора H2SO4. Действие каталазы в кислой среде (в контрольной пробе) прекращается, т. к. оптимум pH = 7,4.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



