Министерство здравоохранения Республики Беларусь
Учреждение образования «Гомельский государственный медицинский университет»
Кафедра биохимии
, В. Т. свергун,
БИОХИМИЯ
практикум
Темы занятий
занятие 1 Вводное занятие. Современные биохимические методы исследования
Занятие 2 Строение и функции белков
занятие 3 Ферменты-1. Строение и функции белков.
Строение, свойства, номенклатура и классификация ферментов.
занятие 4 Ферменты-2. Механизм действия ферментов
занятие 5 Ферменты-3. Медицинская энзимология
ЗАНЯТИЕ 6 Биологическое окисление-1. Цикл Кребса. Пути потребления кислорода в организме.
занятие 7 Биологическое окисление-2. Тканевое дыхание.
Окислительное фосфорилирование. Микросомальное и перекисное окисление.
занятие 8 Контрольное занятие по разделам «Введение в биохимию», «Энзимология и биологическое окисление».
Гомель 2013
Раздел 1 Введение в биохимию
Занятие 1
Вводное занятие. Современные биохимические методы исследования
Цель занятия: знакомство с правилами внутреннего распорядка на кафедре биохимии, с правилами работы в химической лаборатории и правилами техники безопасности. Знакомство основными методами биохимических исследований.
Структура занятия
1 Теоретическая часть
1.1 Ознакомление с правилами внутреннего распорядка на кафедре биохимии и правилами работы в химической лаборатории. Проведение инструктажа по технике безопасности. Знакомство со структурой курса биохимии.
1.2 Биохимия как фундаментальная медико-биологическая наука. Значение биохимии в подготовке врача.
1.3 Характеристика основных биохимических методов, используемых в эксперименте и клинике:
а) на уровне целого организма:
- наблюдение за организмом:
o при удалении органа;
o изменении диеты (голодание или усиленное питание);
o приеме лекарств;
o введении специфических ядов и токсинов;
- наблюдения за человеком и животными со специфическими заболеваниями;
- использование ЯМР-спектроскопии и др.;
б) перфузия изолированного органа;
в) использование тканевых срезов;
г) использование целых клеток;
д) использование гомогенатов;
е) выделение изолированных клеточных органелл;
ж) метод субфракционирования клеточных органелл;
з) выделение метаболитов и ферментов;
и) клонирование генов, кодирующих ферменты и другие белки.
2 Практическая часть
2.1 Применение Международной системы единиц (СИ) в международной лабораторной практике.
2.2 Особенности работы в биохимической лаборатории.
2.3 Инструктаж по технике безопасности.
2.4 Устройства и приборы, применяемые в биохимической лаборатории. Правила работы с ними.
Задачи
1 Согласно термина «биохимия», в живых организмах изучается:
а) переход количества в качество;
б) взаимодействие живых организмов с веществом;
в) превращения вещества и энергии;
г) количественный состав;
д) качественный состав?
(ответ: г, д)
2 Для изучения остаточного азота в плазме крови необходимо избавиться от белков, осаждением их трихлоруксусной кислотой. К какому этапу исследования относится эта процедура?
а) выделение изолированных клеточных органелл;
б) метод субфракционирования клеточных органелл;
в) выделение метаболитов и ферментов;
г) клонирование генов, кодирующих ферменты и другие белки.
(ответ: в)
3 Катаболизм белков сопровождается синтезом в печени мочевины CO(NH2)2. Среднее содержание азота в белке 16%. Какое количество мочевины (моль) может образоваться при катаболизме 175 г белка?
(ответ: 175*0,16/14/2=1 моль)
4 Большинство биохимических показателей концентрации веществ выражается в единицах СИ моль/л. Почему для концентрации белка в сыворотке крови (65-85 г/л) не используются эти единицы?
(ответ: из-за гетерогенности белков сыворотки крови)
Применение Международной системы единиц (СИ) в международной лабораторной практике
Для усвоения данного материала используются учебные пособия и таблицы единиц СИ.
Особенности работы в биохимической лаборатории
Студенты знакомятся с правилами проведения занятий и правилами работы в биохимической лаборатории.
Инструктаж по технике безопасности
Студенты знакомятся с инструкциями по технике безопасности и пожаробезопасности, получают дополнительный инструктаж от преподавателя и расписываются в журнале техники безопасности.
Лабораторные работы
Лаборатоpная работа. Устройства и приборы, применяемые в биохимической лаборатории. Правила работы с ними.
Студенты под руководством преподавателя знакомятся с проведением исследований в биохимической лаборатории, а также с правилами пользования пипетками, центрифугой, термостатом, фотоэлектроколориметром и рефрактометром.
Работа с микропипетками включает ряд навыков и умений: сменять наконечник, правильно использовать 2 упора хода поршня (первый упор – для точного отмеривания заданного количества, второй упор – для внесения образца в пробирку или колбу). Перед внесением пробы убедиться, что в отобранном образце нет пузырьков воздуха. В пипетках с вариабельным объемом требуемый объем устанавливается путем вращения лимба с цифровым индикатором.
Рекомендуемая литература
Основная
1 Биохимия: Учебник для вузов / Под ред. . – 4-е изд., испр. – М.: ГЭОТАР-Медиа, 2006. – С. 69-73.
2 Филиппович, Ю. Б. Основы биохимии. – 4-е изд. – М.: Агар, 1999. – С. 15-22.
3 Марри, Р. и др. Биохимия человека: в 2-х т.: Пер. с англ., М.: Мир, 2004. – Т.1: С. 16-20.
Занятие 2
Строение и функции белков
Цель занятия: Изучить структуру и физико-химические свойства белков. Научиться определять содержание общего белка в плазме крови биуретовым методом.
Исходный уровень знаний и навыков
Студент должен знать:
1 Основные правила техники безопасности при работе в химической лаборатории.
2 Строение и классификацию альфа-аминокислот.
3 Кислотно-основные свойства аминокислот. Реакции на их функциональные группы.
4 Уровни структурной организации белка.
5 Особенности строения пептидной связи.
6 Качественные реакции на белки и пептиды.
7 Комплексные соединения (комплекс меди в биуретовой реакции).
Студент должен уметь:
1 Проводить качественные реакции на белки и пептиды.
Структура занятия
1 Теоретическая часть
1.1 Введение в биохимию. Краткая история биохимии. История отечественной биохимии. Общая характеристика обмена веществ. Понятие об анаболизме, катаболизме и метаболизме.
1.2 Белки – важнейшие компоненты организма. Функции белков, строение, классификация и свойства аминокислот. Обзор уровней структурной организации белковой молекулы. Молекулярная масса белков. Форма и размеры белковой молекулы.
1.3 Принципы определения структуры белка:
1.3.1 Кислотный гидролиз белка;
1.3.1.1 Разделение аминокислот с помощью ионообменной хроматографии;
1.3.1.2 Количественный анализ полученных фракций;
1.3.2 Определение аминокислотной последовательности в белках и олигопептидах;
1.3.2.1 Ферментативное расщепление пептидов (пепсином, трипсином, химотрипсином, папаином);
1.3.2.2 Химическое расщепление пептидов (бромцианом);
1.3.2.3 Определение С-концевых аминокислот (карбоксипептидазами);
1.3.2.4 Определение N-концевых аминокислот (дансил-хлоридом, динитрофторбензолом, фенилизотиоцианатом);
1.3.2.5 определение первичной структуры белка (аминокислотной последовательности);
1.3.2.6 методы пептидных карт («метод отпечатков пальцев»).
1.3.3 Изучение пространственной структуры белковой молекулы (вторичная, третичная, четвертичная структуры):
1.3.3.1 Рентгеноструктурный анализ.
1.3.3.2 Изучение трехмерных моделей белка (Protein Data Bank).
1.3.4 Представление о нативно-развернутых белках – функционально-активной форме белков в клетке.
2 Практическая часть
2.1 Решение задач.
2.2 Лабораторные работы.
2.3 Проведение контроля конечного уровня знаний.
Задачи
1 Рассмотрите указанные группы аминокислот и отметьте, какие из них являются гидрофобными:
а) тир, асп, глу; б) ала, лиз, сер; в) иле, лей, лиз; г) вал, лей, ала; д) арг, гли, цис?
2 Многие белки, содержащие 2 и более доменов, обнаруживают гомологию аминокислот. Эти белки образуются путем:
а) посттрансляционной модификации (процессинга); б) генетических изменений; в) дупликации генов и их слияния; г) аллостерической кооперации; д) транспептидных образований.
3 Остатки каких аминокислот в белках-гликопротеидах ковалентно связывают углеводы? Напишите пентапептид с этими аминокислотами (-ала-X-трп-Y-гли), где X и Y – названные аминокислоты.
4 Остатки каких аминокислот в белках-гистонах обладают положительным зарядом? Напишите пентапептид с этими аминокислотами (-ала-X-мет-Y-гли), где X и Y ‑ названные аминокислоты.
5 К фибриллярным белкам относятся:
а) альбумины; б) гистоны; в) коллагены; г) глобулины.
Лабораторные работы
Лабораторная работа. Количественное определение общего белка в сыворотке крови биуретовым методом (УИРС)
ВНИМАНИЕ! Соблюдать меры безопасности при работе с раствором гидроксида натрия.
Принцип метода. В щелочной среде пептидные связи белка образуют с ионами двухвалентной меди комплекс фиолетового цвета (см. уравнение). Интенсивность окраски раствора прямо пропорциональна концентрации белка, определяемой фотометрически.
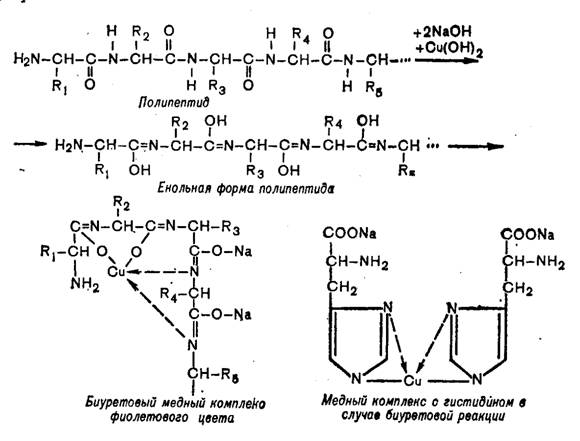
Ход работы. В пробирку наливают 0,05 мл сыворотки крови, затем добавляют 2,5 мл биуретового реактива. Содержимое пробирки осторожно перемешивают, избегая пенообразования, и через 30 мин фотометрируют в кюветах 5 мм при 540 нм (зеленый светофильтр) против контрольного раствора (дистиллированная вода). Измерив экстинкцию исследуемого раствора, по калибровочной кривой определяют концентрацию белка.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



