Полноту прохождения реакций взаимодействия алкалоидов с AgNO3 контролировали методами рентгенофазового анализа (образование кристаллических AgCl и AgBr ) и ИК-, ПМР-спектроскопии (образование новых соединений – нитратов анабазина и лаппаконитина).
Термохимическое определение энтальпии растворения полученного нитрата анабазина в воде проводили при разбавлениях 1:6000; 1:9000; 1:18000. Экстраполированная зависимость ΔHmраств.~f![]() описывается соотношением (кДж/моль):
описывается соотношением (кДж/моль):
ΔHm раст (C10H14N2НNO3) = 20,37 + 390,74 ![]() . (7)
. (7)
Из выражения (7) определена энтальпия растворения С10Н14N2HNO3 в бесконечно разбавленном (стандартном) водном растворе, равная 20,37±0,07 кДж/моль.
3.4-3.8 Термохимия растворения цитизина и его производных, морфолинодитиокарбамата калия, сальсолинодитиокарбамата сальсолина, гидрохлорида N-оксида и комплекса гармина с хлорангидридом п-толуолсульфокислоты, комплекса стахидрина с хлорангидридом п-толуолсульфокислоты в воде и 96 %-ном этаноле
Методом изотермической калориметрии исследованы энтальпии растворения в воде и 96 %-ном этаноле алкалоида цитизина С11Н14N2О (I), выделенного в лаборатории химии фенольных и стероидных соединений АО «НПЦ «Фитохимия» на уровне квалификации «ч. д.а.» и его производных, синтезированных на уровне марки «х. ч.» в Институте органического синтеза и углехимии (г. Караганда). Этими производными являются О, О-диметил-N-цитизинилфосфат C13H19N2O4P (II), цитизиновинилоксиэтиламинотиомочевины C16H21N3O2S (III), цитизинодитио-карбамат триэтиламмония С18Н29N3ОS2 (IV), цитизинодитиокарбамат натрия С12Н13N2ОS2Na (V) и цитизинодитиокарбамат калия С12Н13N2ОS2K (VI).
В таблице 3 приведены результаты экстраполяции термохимических исследований.
Таблица 3 – Коэффициенты уравнения ΔНmраст.=a+b![]() и ΔH0раств., кДж/моль
и ΔH0раств., кДж/моль
Соединение | a | b | ΔH0раств., кДж/моль |
I | 96 %-ный этанол | ||
36,13 | -311,83 | 36,13±0,47 | |
II | -8,58 | 377,89 | -8,58±0,14 |
III | 11,51 | 461,88 | 11,51±0,18 |
I | вода | ||
-6,65 | -99,48 | -0,65±0,01 | |
IV | 23,90 | -198,22 | 23,90±0,27 |
V | 24,76 | -116,26 | 24,76±0,41 |
VI | 22,87 | -129,30 | 22,87±0,30 |
Аналогично вышеуказанным соединениям, на калориметре ДАК-I-IA при 25 єС исследованы энтальпии растворения в воде и в 96 %-ном этаноле при различных разбавлениях: БАС-морфолинодитиокарбамата калия С5Н8NOS2К (I), сальсолинодитиокарбамата сальсолина С23Н30N2O4S2 (II), которые получены на уровне квалификации «х. ч.» в ИОСУ (г. Караганда), производные гармина: гидрохлорид N-оксида С13Н13N2O2Cl (III) и комплекс гармина с хлорангидридом п-толуолсульфокислоты С20Н19N2O3SCl (IV), комплекс стахидрина с хлорангидридом п-толуолсульфокислоты С14Н20O4NSCl (V), выделенные и синтезированные в АО «НПЦ «Фитохимия» на уровне хроматографической чистоты. В таблице 4 приведены результаты экстраполяции калориметрических исследований.
Таблица 4 – Коэффициенты уравнения ΔНmраст.=a+b![]() и ΔH0раств., кДж/моль
и ΔH0раств., кДж/моль
Соединение | a | b | ΔH0раств., кДж/моль |
I | вода | ||
54,18 | 295,17 | 54,2±0,4 | |
II | 98,58 | 2918,5 | 98,6±1,5 |
III | 96 %-ный этанол | ||
30,67 | -325,31 | 30,67±0,53 | |
IV | 4,23 | 191,43 | 4,23±0,06 |
V | 5,65 | 226,3 | 5,65±0,09 |
4 Калориметрия растворения некоторых флавоноидов и их производных в 96 %-ном этаноле, диоксане и диметилформамиде
4.1-4.3 Энтальпия и термохимия растворения пиностробина, оксима пиностробина, тектохризина, артемизетина, кверцетина, рутина, эупатилина и его производного 7-метилового эфира эупатилина в диоксане, 96 %-ном этаноле и диметилформамиде
Подвергаемые к калориметрическому исследованию кристаллы пиностробина С16Н14О4 (I), оксима пиностробина С16Н15NО4 (II), тектохризина С16Н12О4 (III), артемизетина С20Н20О8 (IV), кверцетина C15H10O7 (V), эупатилина С18Н16О7 (VI) и его производного 7-метиловый эфир эупатилина С19Н18О7 (VII) получены на уровне квалификации «ч. д.а.» и хроматографической чистоты в лабораториях химии терпеноидов и химии фенольных и стероидных соединений АО «НПЦ «Фитохимия», а кристаллический рутин С27Н30О16 (VIII) зарубежной фирмы «Socieqade anonima» (Бразилия), имеет «фармакопейную чистоту». Ниже в таблице 5 представлены результаты калориметрических исследований, экстраполированные в область бесконечного разбавления.
Таблица 5 –Уравнения зависимости ΔНmраст.=a+b![]() и ΔН0раст. флавоноидов
и ΔН0раст. флавоноидов
Соединение | a | b | ΔH0раств., кДж/моль |
I | диоксан | ||
74,0 | -11606 | 74,0±0,8 | |
II | 90,6 | -20299 | 90,6±1,5 |
III | 120,6 | -30380 | 120,6±1,1 |
IV | 37,9 | 2482 | 37,9±0,3 |
V | 59,6 | -1500,5 | 59,6±0,9 |
VI | 66,0 | -1077 | 66,0±0,8 |
VII | 72,4 | -1120 | 72,4±0,7 |
VIII | 262,8 | -3608,2 | 262,8±1,5 |
V | 96 %-ный этанол | ||
56,0 | -917,2 | 56,0±0,9 | |
VI | диметилформамид | ||
88,0 | -1032,0 | 88,0±0,7 | |
VII | 111,8 | -575,2 | 111,8±0,6 |
5 Калориметрическое исследование температурной зависимости теплоемкости ряда терпеноидов
5.1 Методика исследований
Исследование изобарной теплоемкости терпеноидов осуществляли на калориметре ИТ-С-400. Прибор позволяет измерять замер температуры от -100 до 400 єС. Предельная погрешность измерения по паспортным данным составляет ±10,0 %. Градуировка прибора проводилась по стандартному медному образцу. При каждой температуре через 25 єС проводились по пять параллельных опытов, результаты которых усреднялись. Хладагентом служил жидкий азот. Погрешность удельных теплоемкостей определялась среднеквадратичным отклонением (![]() ), а мольная теплоемкость – случайной составляющей погрешности (
), а мольная теплоемкость – случайной составляющей погрешности (![]() ). Работа калориметра проверялась определением C0p(298,15) α-Al2O3, опытное значение которого совпадало с его справочным значением с точностью 3,8 %. Верхний предел измерения температуры составляло Тпл–100, чтобы избежать эффект предплавления.
). Работа калориметра проверялась определением C0p(298,15) α-Al2O3, опытное значение которого совпадало с его справочным значением с точностью 3,8 %. Верхний предел измерения температуры составляло Тпл–100, чтобы избежать эффект предплавления.
5.2 Калориметрическое исследование теплоемкостей сесквитерпеновых лактонов с общей формулой С15Н18О3
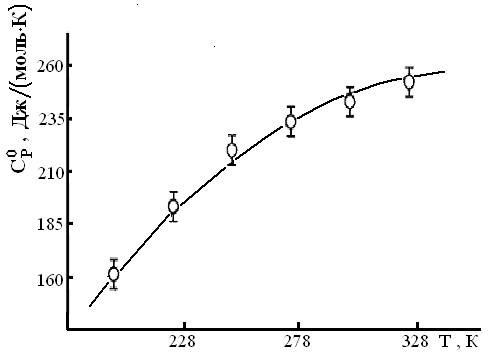
Теплоемкость сесквитерпеновых лактонов С15Н18О3 измеряли на калориметре ИТ-С-400. Графики зависимости Ср0~f(Т) лактонов представлены на рисунке 1. Уравнения указанной зависимости приведены в таблице 6.
|
|
|
|
| Рисунок 1–Температурная зависимость теплоемкости арглабина (а), ахиллина (б), эстафиатина (в), леукомизина (г), б-сантонина (д) |
Таблица 6 – Уравнения зависимости Ср0~f(Т) арглабина, ахиллина, эстафиатина, леукомизина и α-сантонина
Соединение | Сp° = а +в⋅Т + с⋅Т-2, Дж/(моль К) | ∆Т, К | ||
а | b⋅10-3 | -c⋅105 | ||
Арглабин | 276±20 | 120±9 | 54,4±4,0 | 198-223 |
Эстафиатин | 87,5±7,0 | 374±30 | 2,60±0,21 | 198-323 |
α-Сантонин | 123±8 | 556±35 | 19,4±1,3 | 198-398 |
Ахиллин | 1625±91 | -(3394±190) | 307±17 | 198-248 |
884±49 | -(2415±135) | - | 248-273 | |
302±17 | 1272±71 | 317±18 | 273-373 | |
Леукомизин | -(35,7±2,6) | 948±70 | - | 198-223 |
233±17 | -(706±52) | -(50,0±3,7) | 223-273 | |
40,4±3,0 | 737±54 | -(100±7) | 273-373 |
Из данных таблицы 6 и рисунка 1 видно, что ахиллин при 248 К, а леукомизин при 223 К имеет аномальный пик на кривой Ср0~f(Т), что указывает на наличие фазового перехода II-рода, вероятно, связанные со структурными перестройками. С учетом Тпр для ахиллина и леукомизина выведены по 3 уравнения зависимости Ср0~f(Т). Построен мнемонический квадрат по значениям Ср0(298,15) лактонов с общей формулой С15Н18О3 (рисунок 2).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



 а
а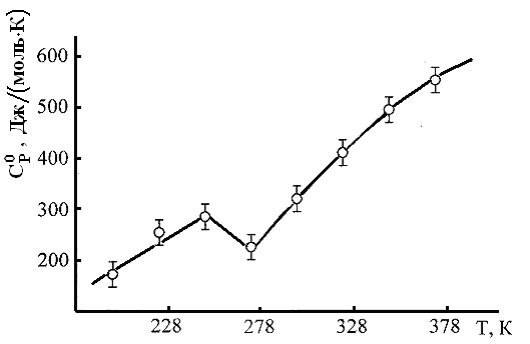 б
б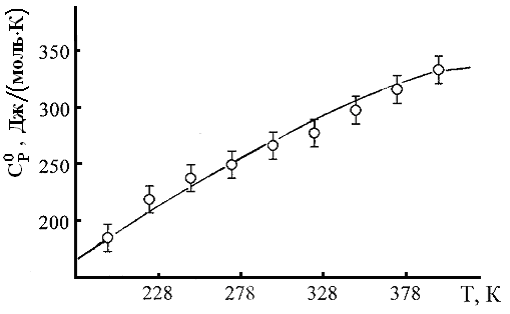 д
д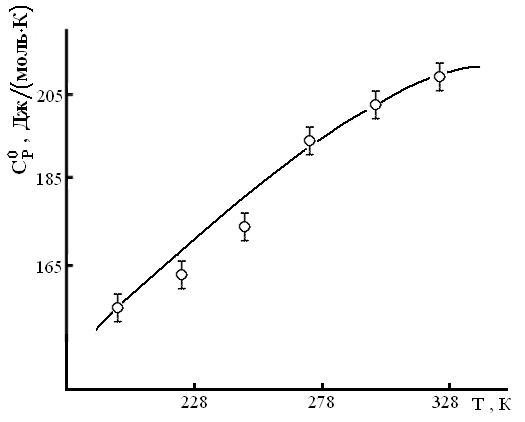 в
в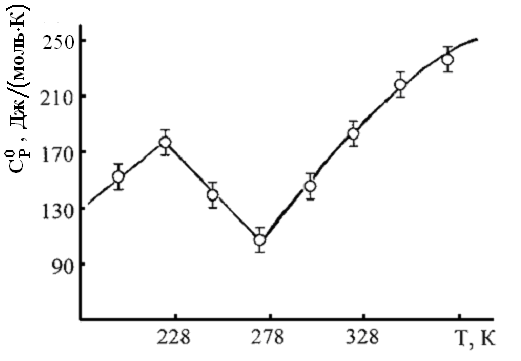 г
г