Если потенциал металла в исследуемом электролите отрицательнее потенциала водородного электрода ( область Ш ), то возможна коррозия как с поглощением кислорода, так и с выделением водорода ( активные металлы). Из рис. 2 следует, что коррозия магния и алюминия возможна при любых рН коррозионной среды как с поглощением кислорода, так и с выделением водорода.
Большинство металлов корродирует с поглощением кислорода на катодных участках, определяющим часто скорость коррозии в слабокислых, нейтральных и щелочных средах. Катодное выделение водорода в сильнокислых средах может лимитировать скорость коррозии активных металлов при водородной деполяризации.
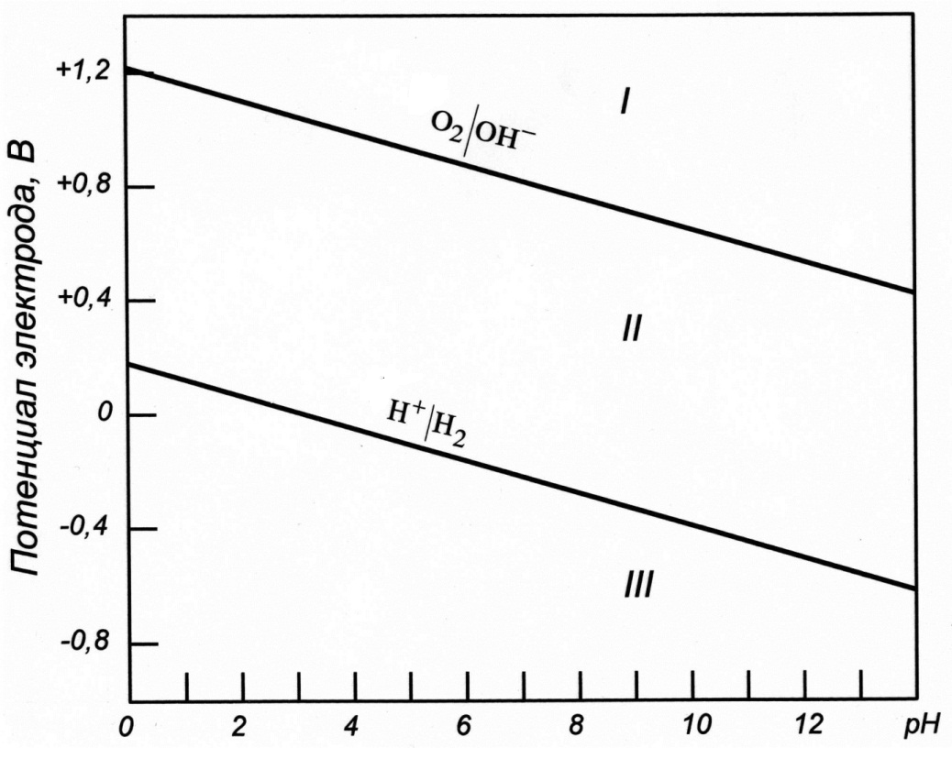
Рис.2. Равновесные потенциалы кислородного и водородного элек-тродов при различных значениях рН электролита и давлениях газов, соответствующих их содержанию в воздухе ( РО2 = 21,3кПа, Р![]()
![]() = 0,05 Па, Т = 297 К).
= 0,05 Па, Т = 297 К).
Расчет по уравнениям:
Е![]()
![]() /ОН– = 1,217 – 0,059рН;
/ОН– = 1,217 – 0,059рН;
ЕН+/Н2 = 0,186 –0,059 рН.
3.2.Диаграммы состояния системы металл – вода(диаграммы Пурбе)
По термодинамическим данным можно построить диаграммы состояния
металл – вода, которые называются диаграммами Пурбе. Эти диаграммы позволяют оценить возможности протекания процесса коррозии металлов. Диаграммы учитывают три типа равновесия в системе металл – вода:
− Равновесия, связанные с обменом электрическими зарядами
Ме = Ме n+ + ne.
Эти равновесия определяются только величиной потенциала и не зависят от рН. Линии, характеризующие эти равновесия, параллельны оси рН.
− Равновесия, не связанные с обменом электрическими зарядами
Ме(ОН)n = Ме n+ + n ОН−..
Эти равновесия определяются только величиной рН и не зависят от потенциала. Линии, характеризующие эти равновесия, параллельны оси потенциалов.
− Равновесия, зависящие как от потенциала, так и от рН, например на
металл-оксидных электродах
Ме + nОН− = Ме(ОН)n + nе.
Потенциал такого электрода определяется уравнением
ЕОН−/Ме = Е 0ОН−/Ме − 0,059 рН.
Из уравнения видно, что линия равновесия имеет наклон, аналогичный
наклону, характеризующему изменение потенциала водородного электрода. Наклон линии равновесия от величины рН в других случаях определяется, исходя из уравнения конкретной электродной реакции.
а б
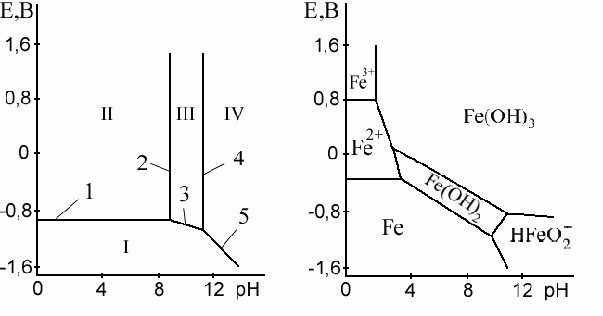
Рис. 3. Диаграммы Пурбе для: а - цинка; б – железа[3].
На рис. 3 приведены диаграммы Пурбе для цинка и железа. Диаграмма для цинка имеет четыре области: I – область термодинамической устойчивости; II, IV – области коррозии и III – область пассивности.
Линии диаграммы отвечают следующим равновесиям:
1 – Zn = Zn2+ + 2e;
2 – Zn2+ + 2OH− = Zn(OH)2;
3 – Zn + 2OH− = Zn(OH)2 + 2e;
4 – Zn(OH)2 + 2OH− = ZnO22− + 2H2O;
5 – Zn + 2H2O = ZnO22− + 4H+ + 2e.
Таким образом, в области II устойчив ион цинка, в области IV–ион цинката. Пассивность цинка в области III обусловлена образованием пленки нерастворимого гидроксида Zn(OH)2.На рис.3 , б приведена диаграмма Пурбе для железа, на которой также обозначены области его термодинамической устойчивости и различные продукты окисления.
3.3.Поляризация электродов коррозионного элемента
Стандартные равновесные электродные потенциалы определяют термодинамическую возможность протекания того или иного коррозионного процесса. В момент замыкания цепи обратимого коррозионного гальванического элемента начальное значение коррозионного тока определяется по закону Ома. Однако в процессе работы гальванического элемента начальное значение тока быстро падает, затем устанавливается какое-то постоянное значение, намного меньше начального. Так как омическое сопротивление во времени существенно не меняется, то снижение коррозионного тока связано с уменьшением начальной разности потенциалов катода и анода
I = ( Eк − Ea) / R
где Ек и Еа – установившиеся потенциалы катода и анода при данном значении тока.
Изменение значений (cдвиг) потенциалов электродов при прохождении тока называется электродной поляризацией.
Сущность явления поляризации сводится к тому, что переход электронов с анода на катод происходит быстрее, чем электродные реакции. В анодном процессе скорость перехода ионов Me n+ в раствор меньше скорости перетекания электронов. Вследствие этого у поверхности электрода скапливается избыток катионов Men+ , и потенциал анода смещается в положительную сторону. В катодном процессе на катоде накапливается избыток электронов, так как молекулы или ионы деполяризаторов не успевают соединяться с электронами, и потенциал катода сдвигается в отрицательную сторону. Явление поляризации в процессах электрохимической коррозии является положительным, так как сильно уменьшает скорость коррозии.
Сдвиг потенциала анода в положительную сторону называют поляризацией анода ДЕа.
Ea = E0 + ДEa (8)
Сдвиг потенциала анода в положительную сторону может быть вызван
несколькими причинами:
1) замедленностью анодного процесса коррозии металла, скорость которого определяется значением энергии активации. Это приводит к возникновению электрохимической поляризации, или перенапряжению ионизации металла ДЕа(эх);
2) замедленностью диффузии ионов металла из двойного слоя в объем электролита, что приводит к возникновению концентрационной поляризации анода ДЕа(конц);
3) замедленностью анодного процесса ионизации металла при возникновении его анодной пассивности. Это сопровождается резким торможением скорости анодного процесса при самопроизвольном падении плотности тока и значительным смещением потенциала анода в положительную сторону ДЕа(пасс).
Сдвиг потенциала катода в отрицательную сторону называют поляризацией катода ДЕк
Eк = Eк0 – ДEк. , (9)
которая может быть обусловлен следующими причинами:
1) замедленностью катодного процесса связывания электронов, поступающих с анода. Это приводит к возникновению перенапряжения катодной деполяризации ДЕк(эх);
2) замедленностью диффузии деполяризатора из объема электролита к катоду или продуктов катодного процесса в обратном направлении. Это приводит к возникновению концентрационной поляризации катода ДЕк(конц).
По степени смещения потенциала электрода при прохождении через него коррозионного тока можно судить о поляризуемости электрода. Если при наложении тока наблюдается незначительное смещение потенциала от его начального значения, то данный электродный процесс протекает практически без торможения. Если же электрод сильно поляризуется (большой наклон поляризационной кривой), это свидетельствует о значительном торможении электродного процесса.
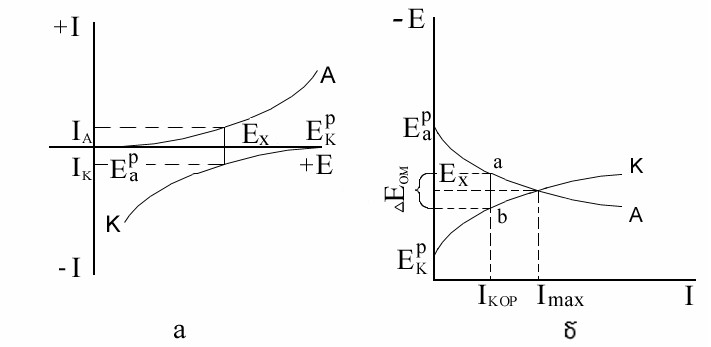
Рис. 4. Два вида поляризационных диаграмм коррозии.
Поляризационные кривые могут быть построены в различных коорди-
натах[3]. . На рис. 4,а представлена наиболее строгая система координат, где более положительные значения потенциала и тока отложены соответственно вправо и вверх, а более отрицательные значения – соответственно влево и вниз. Кривая А отражает кинетику ионизации металла (анодная кривая), кривая К – кинетику восстановления деполяризатора (катодная кривая). Ток коррозии Iкор отвечает потенциалу Ех (потенциал коррозии), когда соблюдается равенство анодного и катодного токов Iк = Iа = Iкор.
Диаграмма (рис.4,б), предложенная Эвансом, является наиболее удобной. На этой диаграмме более отрицательное значение равновесного потенциала откладывается выше, а по оси абсцисс откладывают величины анодного и катодного токов, вне зависимости от того, что они имеют противоположное направление. На диаграмме начальная разность потенциалов Eнач. = Ек – Еа представляет собой разность между начальными (равновесными) потенциалами анодного и катодного процессов. При протекании через коррозионную систему тока наблюдаются анодная ДЕа и катодная ДЕк поляризации. При этом устанавливается общее значение потенциала Ех. Точка пересечения анодной А и катодной К кривых отмечает на оси абсцисс величину максимального тока коррозии Imax. Это максимальное значение тока реализуется лишь в случае, когда омическое сопротивление системы равно нулю или ничтожно мало. Если же R ≠ 0,скорость коррозии будет равна не Imax, а некоторой меньшей величине Iкор.. В этих условиях омическое падение напряжения ДЕом численно равно длине отрезка ab (рис.3,б). Потенциал анода в процессе коррозии будет отрицательнее на величину ДЕом потенциала катода. Таким образом, скорость коррозии зависит от разности обратимых потенциалов анодного и катодного процессов, поляризуемости электродов и омического сопротивления коррозионной среды.
Учет кинетических закономерности катодного и анодного процессов можно осуществить, если ввести понятие анодной Pа и катодной Pк поляризуемости
Pа = ДEа / I, Pк = ДEк / I. (10)
Эти величины иначе называют поляризационными сопротивлениями, так как они отражают сопротивление, оказываемое протеканию анодного Ra и катодного Rк процессов. Поэтому уравнение для расчета скорости коррозии можно записать следующим образом:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |



