6. Методы защиты металлов от коррозии
Возможные методы противокоррозионной защиты разделяются на три группы: 1) изменение свойств коррозионной среды; 2) изменение свойств корродирующего металла или сплава; 3) отделение металла от коррозионной среды ( защитные покрытия). Для первой группы методов характерно стремление уменьшить концентрацию деполяризаторов в среде ( О2, Н+, SO3, NO2 и др. окислителей ), удалить из нее стимуляторы ( активаторы) коррозии (F−, CI–, Br–,HS−, S2−, SO32– и др. ) или ввести в среду добавки ( до 1% ) веществ, замедляющих коррозию ( ингибиторов). Применение ингибиторов– эффективный, универсальный и экономически целесообразный способ противокоррозионной защиты металлов в различных агрессивных средах. Эффективность защитного действия ингибиторов оценивают ингибиторным эффектом ( г ) или степенью защиты (Z ). Ингибиторный эффект показывает, во сколько раз ингибитор уменьшает скорость коррозии и вычисляется по формуле
![]()
![]() =
= ![]()
![]() (13)
(13)
где K, Kо – скорость коррозии соответственно в присутствии ингибитора и без него.
Степень защиты, или защитное действие вычисляется по формуле
Z = ![]()
![]() · 100%. (14 )
· 100%. (14 )
Механизм действия ингибиторов заключается в физической или химической адсорбции их на поверхности металла и последующем торможении катодных и анодных процессов. Характер адсорбции ингибиторов определяется природой активных функциональных групп ингибитора и зарядом поверхности металла. Анодные ингибиторы тормозят растворение металла путем образования на анодных участках защитных пленок( фосфаты, силикаты) или путем перевода металла в пассивное состояние ( хроматы, молибдаты, нитраты, нитриты).Анодные ингибиторы являются «опасными», так как при недостаточной концентрации могут вызвать питтинговую коррозию. Катодные ингибиторы понижают скорость коррозии за счет повышения перенапряжения катодного процесса ( выделения водорода, поглощения кислорода) или образования адсорбционных и фазовых пленок.
В зависимости от условий эксплуатации ингибиторы делятся на следующие группы: 1) ингибиторы атмосферной коррозии( карбонат аммония, смесь уротропина с нитритом натрия, бензоат натрия и др.); 2) ингибиторы для нейтральных и водно - солевых систем ( хроматы натрия или калия, нитрат, силикат или молибдат натрия и др.); 3) ингибиторы кислотной коррозии ( на основе органических веществ); 4) масло - растворимые ингибиторы( ароматические амины, фенолы и др.), вводимые в масла и смазки.
Значительное повышение коррозионной стойкости достигается при легировании металла или сплава специальными добавками, вызывающими торможение катодного или анодного процессов. В качестве катодных легирующих добавок ( до 1% ) используются медь, никель, вольфрам, палладий, платина и др. Торможение анодных процессов связано с уменьшением площади анодных участков или с пассивированием сплава ( при легировании сталей хромом, титаном, молибденом или кремнием).
Защитные покрытия разделяются по ГОСТ 9.301−86 на металлические и неметаллические ( краски, лаки, эмали, смазки и др.). По способу нанесения различают гальванические (электролитическим осаждением цинка, кадмия, никеля, хрома, олова и др.), диффузионные ( насыщением поверхностного слоя металла алюминием, хромом, титаном, кремнием и др.), металлизационные ( распылением жидких металлов), химические (путем химической или электрохимической обработки – оксидирование, фосфатирование, анодирование ) и механотермические покрытия.
Металлические защитные покрытия могут быть анодные и катодные(рис.8). Анодные покрытия имеют электродный потенциал более отрицательный, чем потенциал защищаемого металла (например, цинковое покрытие на железе ![]()
![]() 0 Zn2+/Zn = – 0,76 B, Еo
0 Zn2+/Zn = – 0,76 B, Еo![]()
![]() = = – 0,44 B). При нарушении анодного покрытия разрушение основного металла не происходит, так как пеоследний является катодом коррозионного элемента. Схема работы коррозионного элемента в этом случае может быть представлена в виде
= = – 0,44 B). При нарушении анодного покрытия разрушение основного металла не происходит, так как пеоследний является катодом коррозионного элемента. Схема работы коррозионного элемента в этом случае может быть представлена в виде
|ЇЇЇЇЇЇЇЇ↓ |ЇЇЇ![]()
![]()
( – ) A Zn / Zn2+ Fe O2/ OH– K (+). ( 15 )
|→ Н+/Н2
![]()
![]() An−
An−
Катодными называют покрытия, электродный потенциал которых в данной среде имеет более положительное значение, чем потенциал основного металла, например никель (олово, медь) на стали (железе). При нарушении катодного покрытия основной металл будет анодом и начнет корродировать, а металл покрытия – катодом. Схема работы микрогальванических элементов в этом случае следующая:
|ЇЇЇЇЇЇЇ↓|ЇЇЇ![]()
![]()
( – ) A Fe / Fe2+ Ni O2/ OH– K (+). (16 )
(Sn, Cu) Н+/Н2
|______![]()
![]()
![]()
![]() An−
An−
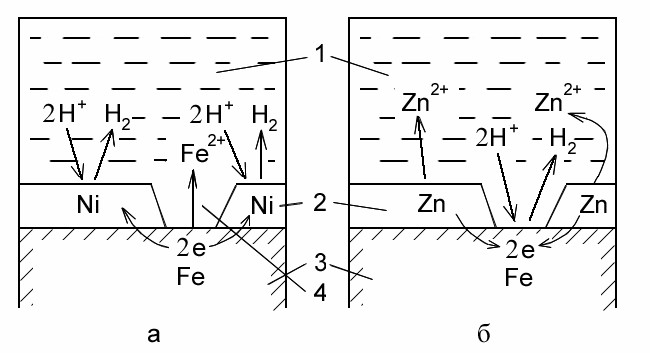
Рис. 8 . Схема коррозии металла в кислом растворе при нарушении металлических покрытий:
а - катодного, б - анодного; 1– раствор, 2 – покрытие, 3 –основной металл,
4 –дефект в покрытии.
В местах обнажения основного металла коррозия усиливается. Следовательно, необходимо, чтобы в катодных покрытиях было минимальное количество пор..
В коррозионных средах с хорошей электропроводностью применяют электрохимическую защиту (протекторную, катодную и анодную защиту, электродренаж). Протекторная защита состоит в создании макрогальванического элемента, в котором защищаемый металл является катодом, а анодом (протектором) служит более активный металл или сплав (алюминий, цинк, их сплавы). Эффективность протекторной защиты зависит от электропроводности среды, разности потенциалов между протектором и защищаемой конструкцией, от площади контакта и способа размещения протектора.
При катодной защите конструкцию искусственно делают катодом путем присоединения к отрицательному полюсу внешнего источника тока, к положительному полюсу присоединяют чугунный или стальной лом, графит. Катодная защита успешно применяются для защиты морских сооружений (шлюзов, эстакад), трубопроводов, судов, изделий из стали, меди и алюминия.
Сущность анодной защиты состоит в создании на поверхности защищаемой конструкции пассивирующей пленки путем анодной поляризации от внешнего источника постоянного тока. Присутствие галогенидных ионов в коррозионной среде делает невозможным применение анодной защиты сплавов на основе железа из-за опасности развития питтинговой коррозии. До уровня промышленного применения доведена анодная защита стальных емкостей для хранения и перевозки кислот и щелочей, а также защита автоклавов из углеродистой стали при щелочной варке целлюлозы.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |



