Iкор =( Ек − Еа ) / (Ra + Rк +Rом ) ( 11 )
Максимальный ток коррозии соответствует полному отсутствию омического сопротивления
Imax =( Ек − Еа ) / (Ra + Rк ) ( 12 )
Виды контроля электрохимической коррозии металлов:
— Анодный контроль. Процесс протекает при значительной анодной поляризации и малой величине катодной поляризации, т. е. ДЕа >>ДЕк.
— Катодный контроль. Процесс протекает при значительной катодной поляризации и малой анодной поляризации, т. е. ДЕк >>ДЕа.
— Омический контроль. Величина коррозионного тока определяется омическим сопротивлением цепи.
— Смешанный анодно-катодный контроль. Процесс протекает при значительной катодной и анодной поляризациях, т. е. ДЕк ≈ ДЕа.
3.4. Анодный процесс коррозии и пассивность металла
В ряде случаев при анодной поляризации происходит резкое снижение скорости растворения металла. Скорость коррозии многих металлов резко уменьшается при введении в состав раствора сильных окислителей. Металл переходит в пассивное состояние. Пассивность металла – это состояние относительно высокой коррозионной стойкости, вызванное торможением анодного процесса электрохимической коррозии.
Для ряда металлов при анодной поляризации становится возможным не
растворение металла в виде катионов, а образование на поверхности защитных оксидных пленок с пассивацией металла. При возникновении пассивного состояния анодный процесс растворения металла тормозится образовавшейся оксидной пленкой. При этом потенциал анода смещается в положительную сторону и уменьшается коррозионный ток. Явлениями пассивности объясняется малая скорость коррозии нержавеющих сталей, алюминия, титана и других металлов и сплавов в определенных условиях.

Рис. 5. Анодная поляризационная кривая c пассивацией.
На анодной поляризационной кривой (рис.5), соответствующей переходу металла в пассивное состояние, можно выделить ряд характерных точек и участков: ЕaР – начальный потенциал анода, Еок – потенциал образования оксида металла, Еп – потенциал начала пассивации, Епп – потенциал полной пассивации. На участке 1—2 происходит только электрохимическое растворение металла с образованием гидратированных ионов. При смещении потенциала в положительную сторону относительно равновесного потенциала Еок (участок 2—3) одновременно с растворением металла идет процесс образования оксида, однако скорость растворения металла превышает скорость образования оксида. В точке 3, соответствующей потенциалу начала пассивации Еп, скорости растворения металла и образования пассивной оксидной пленки становятся равными, а соответствующая этому значению потенциала плотность тока imax(предельный ток пассивации) характеризует максимальную скорость растворения металла. Последующее смещение потенциала в положительную область (участок 3—4) обусловлено преимущественным протеканием реакции образования пассивной пленки. Омическое сопротивление на границе металл –раствор возрастает, а ток поляризации, вследствие этого уменьшается. Точка 4 соответствует завершению пассивации металла. Потенциал, соответствующий данному состоянию, называется потенциалом полной пассивации Епп. На участке 4—5 металл находится в пассивном состоянии. Этот участок независимости тока от потенциала практически наблюдается до тех пор, пока не будет достигнут потенциал какого-нибудь нового анодного процесса окисления с образованием анионов или с выделением кислорода. Новому анодному процессу соответствует частичное или полное растворение пассивной пленки (участок 5—6).
Существуют две основные теоретические концепции, объясняющие
пассивность металла, – пленочная и адсорбционная. Согласно пленочной
теории (, , Эванс), пассивность наступает в
результате образования на поверхности металла фазовой пленки толщиной 10−100 нанометров. Такая пленка оксида или гидроксида увеличивается по толщине с ростом потенциала во всей области пассивности. Пленочная теория, основанная на том, что кислород химически связан с поверхностью металла, не может объяснить все известные факты в области пассивности. Во многих случаях на поверхности металла отсутствует фазовая пленка.
Согласно адсорбционной теории (, ,
) пассивность наступает в результате адсорбции кислорода на
поверхности металла. При этом установлено, что пассивность может наступить даже тогда, когда поверхность металла не полностью_покрыта слоем в одну молекулу [3,4].
4.Поведение железа и его сплавов в агрессивных средах
Потенциал железа при активной коррозии близок к потенциалу процесса Fe→ Fe2++2e, т. е. Е0=–0,44В. В окислительных условиях железо имеет более положительный электрохимический потенциал в связи с его пассивацией. Однако по своей склонности к пассивации железо находится примерно в середине ряда пассивности
Cu< Pb<Sn<Cd< Zn< Mn < Fe <Co <Ni < Mg<Mo<Cr<Al <Ta<Zr <Ti.
Ряд возрастания степени пассивности не будет соответствовать ряду повышения коррозионной стойкости металлов, так как коррозионная стойкость зависит не только от пассивности, т. е. анодного торможения, но и от катодного торможения, термодинамической устойчивости металла в данных условиях.
Повышение доступа окислителей к поверхности железа ведет к облегчению пассивации и повышению коррозионной стойкости. При повышении концентрации кислорода в воде до 16 см3/л коррозия железа резко возрастает, а затем, проходя через максимум в атмосфере кислорода, снижается до малых значений. Увеличение скорости коррозии объясняется действием кислорода как катодного деполяризатора, а снижение – наступающей пассивацией железа. Однако повышение температуры или присутствие в растворе F−, Cl-, Br- активирует железо в окислительных средах.
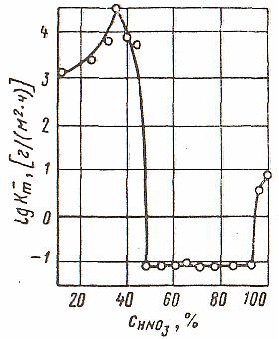
Рис. 6 . Зависимость логарифма скорости коррозии железа
от концентрации HNO3 при 20 °С[2].
Как видно из рис. 6, максимальная скорость коррозии наблюдается в 35%-ной HNO3. В области концентраций 50-90 масс.% железо практически устойчиво. На нем устанавливается потенциал, близкий к потенциалу платинового электрода. Повышение скорости растворения железа с увеличением концентрации HNO3 свыше 90% объясняется возможностью образования более растворимых оксидов железа(V1), т. е. процессом его перепассивации. Максимальная скорость коррозии железа наблюдается в 50%-ной H2SO4. В более концентрированных растворах 70-100% идет снижение скорости коррозии, что объясняется окислительным пасссивирующим действием H2SO4 (конц). Это позволяет применять железные емкости для хранения и транспортировки концентрированной H2SO4 и олеума.
Скорость коррозии железа и низкоуглеродистых сталей в соляной кислоте возрастает в экспоненциальной зависимости от концентрации HCl. Во фтороводородной кислоте железо быстро разрушается при кон-центрации кислоты <50 масс.%, но в более концентрированных растворах (60-95%) при обычной температуре достаточно устойчиво. В органических кислотах (уксусной, лимонной, щавелевой, муравьиной) железо корродирует, но со значительно меньшей скоростью, чем в сильных минеральных кислотах.
5.Влияние кислотности среды на коррозию
Влияние концентрации ионов водорода в коррозионной среде на скорость коррозии металлов определяется их непосредственным участием в электродном процессе или их способностью влиять на растворимость продуктов коррозии, или возможностью образовывать защитные оксидные
пленки при изменении рН раствора. Увеличение концентрации ионов водорода влияет на скорость коррозии особенно сильно в том случае, когда процесс коррозии контролируется не диффузией, а процессом разряда ионов водорода.
Скорость коррозии железа (рис. 7, кривая 1) в области значений рН от 4 до 10 не зависит от концентрации водородных ионов. В этом интервале рН скорость коррозии железа в неперемешиваемых электролитах определяется скоростью диффузии кислорода к поверхности металла. В указанной области поверхность железа находится в контакте с раствором, насыщенным гидратированным гидроксидом железа (II), рН которого составляет 9,5. При рН<4 пленка гидроксида железа(11) растворяется; катодным процессом является восстановление ионов водорода, вследствие чего происходит ускоренное растворение железа. При рН >10 скорость коррозии снижается в результате пассивации железа в щелочных растворах, а затем при рН>13 наступает некоторое увеличение скорости коррозии из-за растворения пассивной оксидной пленки на железе в концентрированной щелочи. Каждый металл характеризуется определённой зависимостью скорости коррозии от рН раствора (рис. 7).

Рис. 7. Влияние рН раствора на характер зависимости скорости коррозии для различных металлов: 1 – железа; 2 – благородных; 3 – цинка и алюминия; 4 – никеля и кадмия [3].
Независимость скорости коррозии благородных металлов (платина, золото, серебро), устойчивых в кислых и в щелочных средах, от рН выражается прямой 2, параллельной оси абсцисс. Цинк и алюминий неустойчивы в кислотах и в щелочах. В сильно кислых средах образуются аквакатионы Zn2+ и А13+, а в щелочах – гидроксокомплексы и анионы ZnO22− и AlO2−-, поэтому на кривой 3 наблюдаются подъемы в кислой и щелочной областях. Никель и кадмий устойчивы в нейтральном и щелочном растворах и корродируют в кислом растворе (кривая 4). Подобные зависимости скорости коррозии имеют место при отсутствии окислителей и других ионов, образующих защитные слои на металлах.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |



