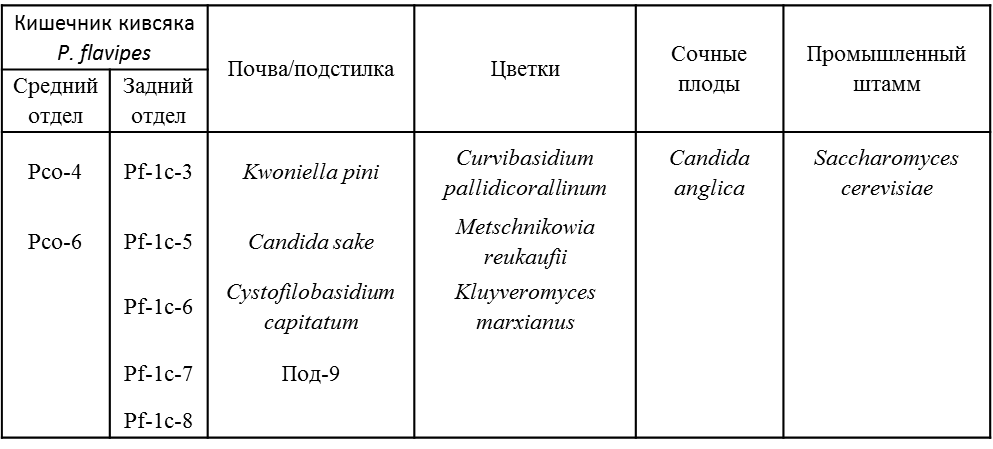
Таблица 1. Используемые штаммы дрожжей и места их выделения
2. Методы исследования
1. Метод выращивания культур в жидкой среде.
Культуры для экспериментов выращивались в течении 2-3 суток в жидкой среде ГПД (глюкозо-пептонно дрожжевая) (г/л): D-глюкоза – 20; пептон – 10; дрожжевой экстракт – 5, хлорамфеникол – 0,5.
В коническую колбу вносили 25 мл жидкой среды, затем вносили культуру дрожжей, закрывали пробкой и ставили на качалку Orbital Shaker PSU-10 в режиме 120 об/мин.
2. Измерение оптической плотности суспензии дрожжей (Денситометрический метод)
Учет роста численности клеток производился по изменению оптической плотности исследуемой смеси суспензии дрожжей и кишечной жидкости в среде.
Этот метод основан на законе Бугера— Бэра (Орлов, 1963), устанавливающего зависимость между ослаблением света растворами и концентрацией поглощающего свет компонента. Компонентом, поглощающим свет, в нашем случае выступают непосредственно клетки. Чем больше оптическая плотность, тем хуже исследуемый раствор пропускает пучок света и тем больше количество клеток.
Пропускание света (Т) в общей формуле можно представить так:
Т=I/I0 (1)
где I0-интенсивность пучка света до взаимодействия с веществом, а I-после взаимодействия.
Оптическая плотность же выражается так:
D= - lg(I/I0) = - lgT (2)
Оптическая плотность, как это следует из закона Бугера—Бэра, прямо пропорциональна концентрации вещества, и поэтому ею удобно пользоваться при количественных определениях. Связь между концентрацией и оптической плотностью вытекает из следующих рассуждений. Если монохроматический световой поток интенсивностью I0 падает на поглощающий слой, то выходящий пучок I оказывается ослабленным. Изменение интенсивности пучка dI в результате взаимодействия с одним из тонких слоёв dl, на которые можно разделить всю толщину слоя суспензии l, пропорционально толщине слоя и интенсивности светового пучка
dl= - kI0dl (3)
где k — коэффициент пропорциональности, минус указывает на уменьшение энергии в результате поглощения.
Если бы световой пучок, падающий на каждый из слоев dl, был одинаков, то формула была бы справедлива для любой толщины. Однако интенсивность света, проходящего через слои dl, последовательно уменьшается. Поэтому общее решение находится путем интегрирования дифференциального соотношения
dI/I0= - kdl = II0∫dI/I0 = - l0∫kdl (4)
откуда
ln(I/I0)=-kl, или I=I0e-kl (5)
Это соотношение выведено Бугером. Поскольку поглощение света определяется количеством частиц вещества, расположенных на пути светового пучка, то увеличение концентрации вызывает такое же изменение интенсивности света, как и изменение толщины поглощающего слоя (закон Бэра).
Тогда
I=I0e-klC (6)
где С-концентрация.
Выведенное положение строго справедливо для монохроматического излучения. Вводя обозначение Ɛл=2,303k (излучательная способность на данной длине волны) и переходя к десятичным логарифмам, получим
lg(I/I0)=- ƐлlC (7)
Используя уравнение (2) получим
D= ƐлlC (8)
Используя этот метод можно вести довольно точный учет роста численности клеток, что требует скрупулезных подсчетов в некотором объёме суспензии, затем перерасчёта на весь объём изучаемой суспензии и затем возможно соотнести единицу оптической плотности и численности клеток, но в данной работе мы принимаем, что рост оптической плотности прямо пропорционален росту количества клеток, и используем снимаемые показания непосредственно для характеристики роста популяций дрожжей.
3. Спектроскопия ЯМР.
Согласно толковому англо-русскому словарю по нанотехнологии (Арсланов, 2009): «Ядерно-магнитный резонанс (ЯМР) – явление резонансного поглощения радиочастотной электромагнитной энергии веществом с ненулевыми магнитными моментами ядер, находящимся во внешнем постоянном магнитном поле. Ненулевым ядерным магнитным моментом обладают ядра 1Н, 2Н, 13С, 14N, 15N, 19F, 29Si, 31P и др. ЯМР обычно наблюдается в однородном постоянном магнитном поле В0, на которое накладывается слабое радиочастотное поле В1 перпендикулярное полю В0.»
Сигнал в спектре ЯМР характеризуется рядом параметров.
Химический сдвиг
В постоянном магнитном поле происходит расщепление энергетических уровней, соответствующих различным ориентациям магнитного момента (спина) ядра в магнитном поле. Но в реальной молекуле на атом также действует локальное магнитное поле, создаваемое совокупной электронной плотностью соседних ядер. В итоге суммарный вектор магнитного поля, действующего на данное ядро, определяется как внешним магнитным полем, так и химическим окружением ядра. Поскольку величина расщепления энергетических уровней пропорциональна намагниченности в данной точке молекулы, то резонансная частота поглощения будет индивидуальной для каждого типа атомов. Разница частот поглощения изолированного атома и химически связанного называется химическим сдвигом, поскольку именно она определяется локальным магнитным полем. Это абсолютный химический сдвиг, но его использование крайне затруднительно в силу сложности экспериментального измерения и значительной удаленности сигнала изолированного атома от областей поглощения химически связанных атомов. Поскольку зависимость резонансной частоты поглощения линейна в широких диапазонах значений, то в качестве стандарта обычно используют произвольно выбранное вещество, резонансный сигнал которого находится рядом, но не пересекается с областями поглощения атомов большинства химических соединений. Это относительный химический сдвиг. Для спектроскопии ЯМР на ядрах 1Н и 13С в качестве условного нуля выступает тетраметилсилан (CH3)4Si. На практике отсчет ведется не от нулевого сигнала стандарта, а от сигналов остаточных протонов дейтерированного растворителя, для которых заведомо известны химические сдвиги в данной шкале отсчета. Из-за того, что частотный сдвиг слишком мал по отношению к основной ЯМР чистоте, химический сдвиг выражается в частях на миллион (ppm).
Интенсивность сигнала
Уникальной особенностью спектроскопии ЯМР является то, что интегральная интенсивность сигнала зависит только от числа соответствующих атомов в образце, поэтому сравнивая площади пиков (интегральную интенсивность), мы можем достаточно точно оценить соотношения типов атомов в молекуле.
Форма сигнала
В подавляющем большинстве случаев сигнал атома в спектре 1Н ЯМР состоит из нескольких линий различной интенсивности. Количество и соотношение интенсивностей линий определяется спиновой конфигурацией соседних атомов с ненулевым спином и позволяет судить о связности атомов в молекуле, что дает информацию о структуре. К тому же форма сигнала достаточно индивидуальна и позволяет различать сигналы с близкими химическими сдвигами, но несколько различающимся структурным окружением.
Как уже было сказано выше, положение сигнала в спектре определяется только его химическим окружением и для различных функциональных групп существуют характеристические области химических сдвигов. Это свойство спектроскопии позволяет проводить групповой анализ смесей. Поскольку наши кишечные жидкости представляют собой сложную смесь различных соединений – белковой природы, полисахаридов и так далее, то мы использовали спектроскопию 1Н ЯМР для проведения группового анализа фракций и оценки состава. Это позволит сравнить состав кишечных жидкостей, дать качественную оценку различий в их составе и связать с их активностью.
Спектры ПМР регистрировали на спектрометре Bruker Avance-600 с рабочей частотой по 1H 600,22 МГц для растворов в D2O. Химические сдвиги (δ, м. д.) измеряли относительно остаточного сигнала растворим. д.).
Анализ проводился Александром Сергеевичем Сигеевым.
3. Методика исследования
1. Отобранные животные помещались в контейнеры с подстилкой из их местообитания и в течении двух недель вскрывались для получения кишечной жидкости. Раздельно собиралась кишечная жидкость среднего и заднего отдела. Отобранная КЖ помещалась в пробирки типа Эппендорф, проходила первичную стерилизацию при помощи центрифугирования в течении 10 минут при 12000 оборотах в минуту и надосадочная жидкость замораживалась при -18оС в морозильнике.
2. Дрожжи для экспериментов выращивались в жидкой ГПД среде с добавлением хлорамфеникола концентрации 500 мг/л в течении 2-3 суток.
3. Непосредственно перед экспериментом кишечная жидкость размораживалась и проходила ещё несколько циклов по 15 минут центрифугирования до того момента, когда осадка не образуется.
4. В дальнейшем, КЖ проходила фильтрацию через бактериальные фильтры с диаметром пор 0,22 мкм.
5. Суспензия дрожжей отмывалась от среды и продуктов метаболизма также центрифугированием: после осаждении дрожжей вся надосадочная жидкость извлекалась, в пробирку помещался тот же объем стерильной воды, что был и у надосадочной жидкости, содержимое пробирки встряхивалось до образования однородной суспензии. Этот цикл проводился три раза.
Далее существуют некоторые отличия в методиках экспериментов.
6. В опытах с взаимодействием кишечных жидкостей двух отделов как московской Cylindroiulus caeruleocinctus, так и крымской Pachyiulus flavipes на штаммы не идентифицированные, но выделенные из кивсяков, измерения поводились на длине волны 405 нм. В ячейке планшеты смешивались кишечная жидкость и суспензия дрожжей в соотношении 1:1 (по 10 мкл в случае КЖ московской многоножки, и по 5 в случае с московской многоножкой). Смесь выдерживалась до 60 минут, а затем добавлялась питательная среда (ГПД с хлорамфениколом 500 мг на 1 л) до суммарного объема 200 мкл.
7. Планшет помещали в микропланшетный фотометр (microplate absorbance reader) Sunrise фирмы «Tecan». Эксперимент проходил при температуре +25єС. Измерения проводились каждые 6 часов в случае с крымским кивсяком и каждые 30 минут в случае с московским. Оптимальное время между измерениями - 30 минут.
8. В последующих экспериментах уже для измерений использовали другую длину волны 620 нм. Это может предотвратить погрешность измерений из-за потемнения самой кишечной жидкости.
9. Дальнейший эксперимент был направлен на изучение влияния разбавления суспензии дрожжей. Выращивалась двухсуточная суспензия идентифицированных дрожжей (Candida sake, Kluyveromyces marxianus), затем отмывалась от среды и разбавлялась в 10 и 100 раз. Затем в ячейки помещалась суспензия и КЖ среднего и заднего отделов московского и крымского кивсяков в соотношении 1:1 (по 5 мкл); через 40 минут в них добавлялось 190 мкл среды. Оптическая плотность снималась каждые 30 минут при длине волны 620 нм и температуре +25єС с помощью микропланшетного фотометра.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



