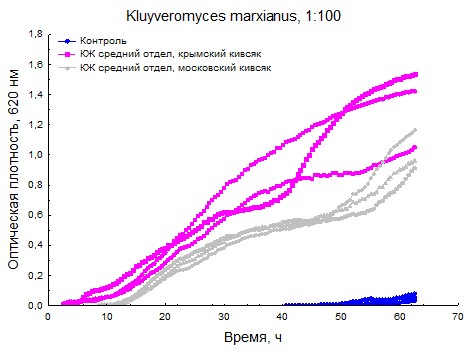
Рисунок 9. Кривые роста Kluyveromyces marxianus при разбавлении суспензии дрожжей.

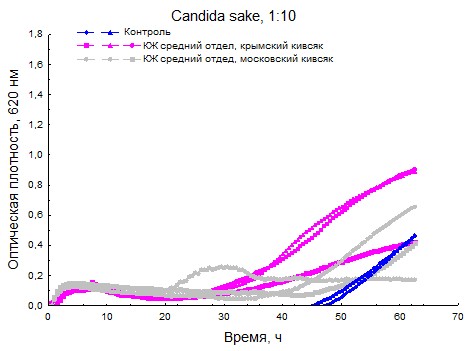
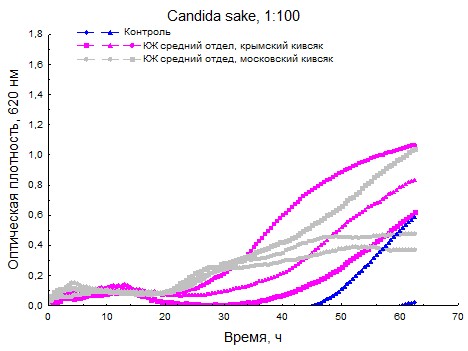
Рисунок 11. Кривые роста Candida sake при предварительном разбавлении суспензии дрожжей.
Данные максимальной удельной скорости роста (см. приложение 5) говорят нам о том, что почвенный Candida sake подавляется КЖ среднего отдела как московской, так и крымской многоножки, а вот выделенный с цветков Kluyveromyces marxianus имеет максимальную удельную скорость роста при воздействии КЖ среднего отдела московского кивсяка даже выше, чем в контроле.
Эксперименты с различными концентрациями суспензий дрожжей и соотношением объема кишечной жидкости кивсяка московского к общему объему смеси отличаются от предыдущих экспериментов тем, что финальное разбавление кишечной жидкости суспензией дрожжей и средой составило 1:1. Суспензия дрожжей была разбавлена в 1000 раз. Таким образом, концентрация действующего вещества была гораздо выше, чем в предыдущих случаях.
В ходе экспериментов для штамма Curvibasidium pallidicorallinum были получены следующие кривые роста (см. рисунок 12).
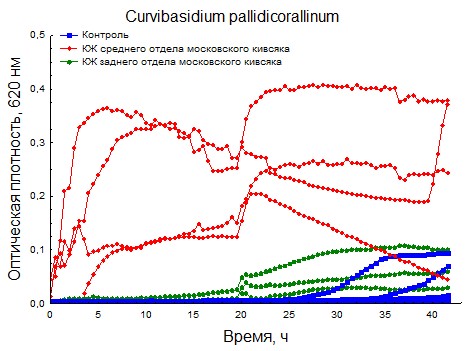
Рисунок 12. Кривые роста штамма C. pallidicorallinum после воздействия кишечной жидкости кивсяка С. сaeruleocinctus
При микроскопировании ячеек с кишечной жидкостью из среднего отдела мы наблюдали отсутствие живых дрожжевых клеток. Морфологически дрожжи после КЖ заднего отдела и контроли ничем не отличаются.
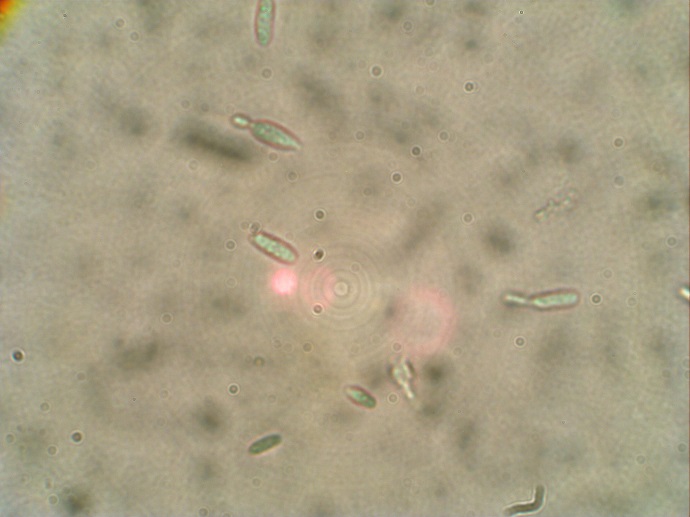
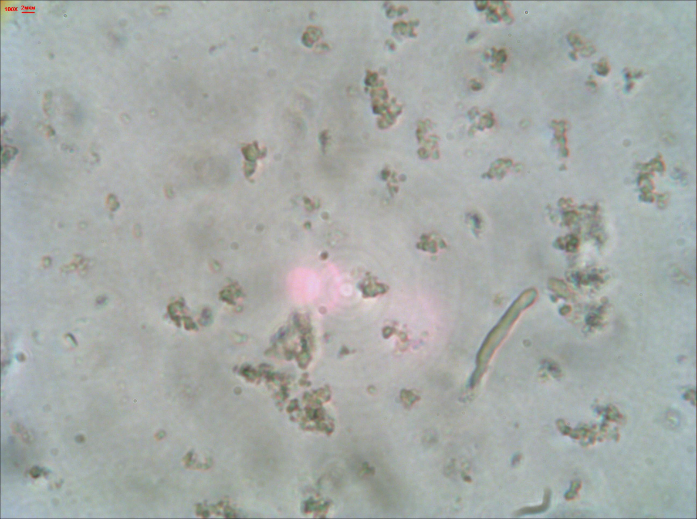
Рисунок 13. Клетки C. pallidicorallinum: контроль (слева) и после воздействия КЖ среднего отдела (справа)
Другие штаммы в ячейках с кишечной жидкостью среднего отдела имеют схожиее кривые роста. Так как эти показания обусловлены не увеличением численности дрожжевых клеток, а агрегированием мертвых или изменённых клеток, решено было не заниматься расчетами кинетических параметров.
Для установления жизнеспособности клеток в ячейках с кишечной жидкостью был произведен посев содержания соответствующих ячеек на агаризованной ГПД среде с добавлением хлорамфеникола (500 мг/л) (см. приложение 6). По результатам посева становится ясно, что в ячейках с любым штаммом и кишечной жидкостью среднего отдела кивсяка C. caureleocinctus нет ни одной КОЕ (Колониеобразующие единицы) на 10 мкл.
Отметим, что КЖ среднего отдела московского кивсяка убивает штаммы цветочные C. pallidicorallinum, Metschnikowia reukaufii и подстилочный Kwoniella pini (см. приложение 7).
4.2 Анализ спектров ЯМР кишечных жидкостей кивсяков
Общий вид спектров представлен в приложении 8.
1. Область 6.5-8.5. (см. приложение 9) Эта область отвечает в первую очередь за ароматические структуры. По спектрам можно сказать следующее: А) У образцов 1 и 2 (средний и задний отделы кивсяка крымского) аминокислотный состав (для аминокислот с ароматическими фрагментами) качественно схож. Количественно заметны различия – в образце №2 (задний отдел) существенно больше интенсивность пиков в районе 8.5 ppm. Если предполагать, что в этой области имеются только сигналы от ароматических протонов – то это бензольное кольцо с 1-2 COOH группами или аналогичными, либо полиазотный гетероцикл.
Б) Образец №3 (КЖ среднего отдела московского кивсяка) качественно отличается – в нем есть пики при 6.75 и 7.05 ppm, которые в остальных образцах присутствуют в следовых количествах. По сдвигам эти сигналы могут относиться к триптофану.
В) Образец №4 в целом похож на №3 (соответственно задний и средний отдел кишечника московского кивсяка), но соотношения сигналов меняются – более интенсивными становятся те, что относятся к области слабого поля – в районе 8.5 ppm, а те, что в более сильном поле – 6.75 – 7.3 – теряют интенсивность.
Г) В образцах № 1 и № 3 (относятся к средним отделам) также присутствует дублет при 7.75 ppm, который отсутствует в образцах №2 и №4 (относятся к задним отделам). Таким образом можно предположить, что состав белковых фракций данных образцов различен, причем в образцах №1 и№3 и в образцах №2 и №4 преобладают разные фракции.
2. Сигнал в районе 3.0 ppm – наблюдается только в образцах №2-4 (КЖ задних отделов), в образце №1 его интенсивность мала. Причем если в образцах №1-2 (КЖ крымского кивсяка) это синглетный сингал, то в №3-4 (КЖ московского кивсяка) он имеет форму триплета, что говорит о том, что они относятся к разным соединениям. Также следует обратить внимание на область в районе 2.35 ppm – в случае образцов №1,3 (КЖ СО)– здесь сигнал отсутствует, а в образцах №2,4 (КЖ ЗО) наличествуют сигналы, причем разные для каждого образца.
Наиболее существенные отличия наблюдаются в области алифатических сигналов (см. приложение12) Так в районе 1.83 ppm в случае образцов №2,4 наблюдается интенсивный пик, в случае образцов №1,3 его интенсивность весьма мала. В то же время в районе 0.7 ppm ситуация ровно обратная – в образцах №1,3 в этой области имеется интенсивный сигнал алифатических протонов, тогда как в образцах №2,4 сигнала в этой области нет.
Таким образом, на основании этих данных можно сделать следующий вывод – образцы кишечной жидкости делятся на две группы по сходству – образцы №1 и №3 (КЖ средних отделов) и образцы №2 и №4 (КЖ задних отделов). Эти группы имеют заметные сходства по типу и виду сигналов, но, несмотря на это внутри групп тоже наблюдаются различия, хотя и существенно меньшие и в большей степени количественные, чем между группами. В силу очень сложного состава кишечных жидкостей более детальный анализ не представляется возможным.
Заключение
Реакция штаммов на воздействие кишечной жидкости разных отделов различна: от подавления роста культур до нейтральной реакции и даже стимуляции роста. Четкой корреляции со средой обитания, откуда были выделены эти дрожжи, нет. Кишечная жидкость проявляет киллерные свойства в разных концентрациях, даже при разбавлении в 40 раз. При определенном значении концентрации кишечной жидкости среднего отдела Cylindroiulus caeruleocinctus (2 объёма КЖ к 1 объёму разбавленной суспензии дрожжей) в клетках дрожжей происходит необратимые изменения и потеря жизнеспособности. Разбавление суспензии дрожжей перед взаимодействием с кишечной жидкостью приводит к увеличению длительности лаг-фазы роста популяции. ЯМР анализ показал, что наиболее схожи между собой кишечные жидкости средних отделов и задних отделов C. сaeruleocinctus и P. flavipes. Различия внутри этих групп тоже есть, но существенно меньшие и в большей степени количественные.Список литературы
Арсланов англо-русский словарь по нанотехнологии. - М. ИФХЭ РАН, 2009. -261 c. Бызов взаимодейсвия в почве. М.: Изд-во ГЕОС, 2005. -212с. , Стриганова почвенных беспозвоночных в разложении растительных остатков и круговороте веществ // Зоология беспозвоночных. Почвенная зоология. М., 1978, Т. 5. - С. 8 - 69. , Орлов -химические методы исследования почв. М.: Изд-во Моск. ун-та, 1964. -348с. Козловская почвенных беспозвоночных в трансформации органического вещества болотных почв. –Л.: Наука -1976- 212с. Курчева почвенных животных в разложении и гумификации растительных остатков. - М.: Наука, 1971, -154 с. Марфенина дождевых червей на микроскопические грибы как деструкторы органических веществ в почве. // Деструкция органических веществ в почве. Вильнюс - 1989 - С. 104-108. , , Бызов дрожжевых грибов и коллембол в почве // Микробиология. — 2006. — Т. 75, № 6. — С. 1–9. , , Звягинцев оценка влияния мезофауны на скорость разложения растительного опада. // Вестн. Моск. Ун-та. – Сер. Почвоведение. – 1985- №3-С. 37-45 Покаржевский модель миграции веществ в сообществах почвенных животных. // Почвенная фауна Северной Европы. –М.: Наука, 1987- С. 34-37 Стебаев комплексы в биогеоценозах. // Почвенные организмы как компоненты биогеоценоза, М.: Наука,-1984 - с. 3-1 Cтриганова характеристика деятельности разных групп почвенных беспозвоночных в процессах разложения лесной подстилки. // Экология. -1971 - №4- С.36-43 , , и др. Реакция микроорганизмов на воздействие пищеварительной жидкости дождевых червей // Микробиология. — 2007. — Т. 76, № 1. — С. 45–54. Ву Нгуен Тхань. Судьба дрожжей в ассоциациях с почвенными беспозвоночными. Автореф. дисс. … канд. биол. наук. М.: Изд-во МГУ, 1993, 24 с. Уголёв адекватного питания и трофология. - Л.: Наука, 1991. 272 с. Bignell D. E. Relative assimilation of C-labelled microbial tissue and C-plant fibers ingested with leaf litter by the millipede Glomeris marginata under experimental conditions. //Soil Biology and Biochemistry,-1989, V. 21,-pp. 819-827. Cooke A. The effects of fungi on food selection by Lumbricus terrestris L. //Earthworm Ecology, J. E. Satchell, (Ed.), Chapman and Hall,-1983,-pp. 365-373. Dash M. C., Mishra P. C., Behera N. Fungal feeding by a tropical earthworm. //Tropical Ecology,-1979, V. 20,-pp. 9-12. Dash N. K., Behera N., Dash M. C. Gut load, transit time, gut microflora and turnover of soil, plant and fungal material by some tropical earthworms. // Pedobiologia,-1986, V. 29-pp. 13-20. Domshe K. H., Banse M. Mykologische Untersuchungen Am Regenwurm Exkrementen. // Soil Biology and Biochemistry,-1972, V. 4,-pp. 31-38 Gunnarson T., Selective feeding on a maple leaf by Oniscuss asellus (Isopoda). //Pedobiolodia. -1987 v. 30, N 3- P. 161-165. Hanlon R. G.D., Some factors influencing microbial growth on soil animal faeces. // Pedobiologia-1981. V. 21, N 3/4.-P. 257-263. Lee, K. E. & Wood, T. G. Termites and soils. - London. Academic Press,-1971. 252p. Paul F. Hendrix, Earthworm Ecology and Biogeography in North America –London, Lewis Publishers - 1995 -245pp Piearce T. G. Gut contents of some Lumbricid earthworms // Pedobiologia. -1978. V. 18.-P. 153-157. Sharpley, A. N.; Syers, J. K. and Springel, J. A. Effect of sutface-casting earthworms on the transport of phosphorus and nitrogen in surface runoff from pasture. // Soil biology and biochemistry. 1979 - №11 - 459-462 рр. Syers, J. K.; Sharpley, A. N.; Keeney, D. R. Cycling of nitriogen by surface-casting earthworms in a pasture ecosystem. // Soil biology and biochemistry. 1979-№11- 181-185 pp.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



