Задача 28. Рассчитать э. д.с. гальванической цепи, состоящей из нормального водородного электрода и водородного электрода, опущенного в чистую воду. Составить гальваническую цепь и записать реакцию протекающую на электродах.
Таблица 8.1
Стандартные электродные потенциалы в водных растворах при 25 °.
№ | Электрод | е, В. |
1 | Н+/Н2 | 0,00 |
2 | Zn2+/Zn | -0,763 |
3 | Cu2+/Cu | +0,337 |
4 | Хингидронный | +0,704 |
5 | Mn 3+/ Mno4- | 1,206 |
6 | Mn2+/MnO2 | +1,23 |
7 | MnO4 -/MnCl2 | +1,51 |
8 | NO3 -/NO | +0,96 |
9 | S2O8 2-/ 2SO42- | +2,010 |
10 | Fe3+/ Fe2+ | +0,771 |
11 | O2/ H 2O2 | +0,682 |
12 | NO 3-/ NO 2- | +0,940 |
13 | Потенциал насыщенного каломельного электрода | +0,2503 |
14 | Потенциал 1,0н каломельного электрода | +0,2810 |
15 | Потенциал 0,1н каломельного электрода | +0,3335 |
16 | Ag/Ag+ | +0,799 |
17 | Mn2+/MnO-4 | -1,52 |
18 | Потенциал 1,0н хлорсеребряного электрода | +0,2381 |
19 | Потенциал 0,1н хлорсеребряного электрода | +0,2900 |
Таблица 8.2
Коэффициенты активности ионов в зависимости от заряда
и концентрации при 25 0 С
С г-моль /дм3 | однозарядный | двухзарядный |
0,001 | 0,965 | 0,903 |
0,01 | 0,900 | 0,744 |
0,1 | 0,780 | 0,465 |
Тема 9. Поверхностные явления. Адсорбция.
Адсорбция это процесс изменения концентрации на границе раздела 2х фаз, одна из которых обычно пребывает в жидком или твердом состоянии и называется адсорбентом. Другая фаза пребывает в состоянии газа или жидкости и называется адсорбтивом.
В простейшем случае процессы адсорбции классифицируются по агрегатному состоянию адсорбента или адсорбтива.
Для всех жидких адсорбентов мерой адсорбции служит поверхностное натяжение (![]() ) или поверхностная активность (
) или поверхностная активность (![]() ). Величину адсорбции (
). Величину адсорбции (![]() ) рассчитывают по уравнению Гиббса:
) рассчитывают по уравнению Гиббса:
![]() ,
,
где ![]() - равновесная концентрация адсорбтива, кмоль/м3;
- равновесная концентрация адсорбтива, кмоль/м3;
![]() - универсальная газовая постоянная (см. Приложение табл. );
- универсальная газовая постоянная (см. Приложение табл. );
![]() - температура, К.
- температура, К.
Если ![]() < 0, или
< 0, или ![]() то вещество накапливается в поверхностном слое и называется поверхностно-активным веществом (ПАВ).
то вещество накапливается в поверхностном слое и называется поверхностно-активным веществом (ПАВ).
Если ![]() >0, или
>0, или ![]() > 0, то концентрация в поверхностном слое будет меньше, чем в объеме, а величина адсорбции – отрицательна.
> 0, то концентрация в поверхностном слое будет меньше, чем в объеме, а величина адсорбции – отрицательна.
Известно, что с удлинением углеводородной цепи органических соединений их растворимость в воде уменьшается. Эту зависимость можно охарактеризовать правилом Траубе – Дюкло :
с увеличением длины углеводородной цепи органических соединений одного гомологического ряда на группу –СН2 адсорбционная активность возрастает в 3,2 раза.
На твердых поверхностях (адсорбентах) характеристики процесса зависят также и от агрегатного состояния адсорбтива.
Мерой адсорбции из растворов служит изменение концентрации (![]() ), величину адсорбции рассчитывают по уравнению Ловица:
), величину адсорбции рассчитывают по уравнению Ловица:
![]() ,
,
где ![]() - разность концентрации до и после адсорбции, кмоль/м3;
- разность концентрации до и после адсорбции, кмоль/м3;
![]() - объем адсорбтива, м3;
- объем адсорбтива, м3;
![]() - масса адсорбента, кг.
- масса адсорбента, кг.
Гмах и константы (![]() и
и ![]() ), характеризующие процесс адсорбции находятся с помощью построения изотерм по Ленгмюру и Фрейндлиху.
), характеризующие процесс адсорбции находятся с помощью построения изотерм по Ленгмюру и Фрейндлиху.
Уравнения и изотермы адсорбции
![]() ( Ленгмюра)
( Ленгмюра)
![]() или
или ![]() (Фрейндлиха)
(Фрейндлиха)
Ленгмюра Фрейндлиха
Г lg Г
Гmax
б tg б =1/n
с lg K lg Сp
где Г – величина адсорбции, кмоль/кг,
Г – предельное количество адсорбированного вещества или максимальная адсорбция, кмоль/кг,
Х/т –величина адсорбции на единицу массы адсорбента, кмоль/кг.
На поверхности твердого адсорбента может происходить из растворов электролитов – ионная и полярная адсорбция. При этом на поверхности адсорбента образуется двойной электрический слой. Адсорбционная активность ионов зависит от их концентрации и от природы (степени окисления и гидратации). Ряды ионов, составленные в порядке уменьшения их адсорбционной активности называются лиотропными, например, для одновалентных катионов лиотропный ряд выглядит так:
![]()
Катионы различной валентности, их можно расположить в следующий ряд: ![]()
Если на поверхности уже адсорбирован электролит, то при появлении в адсорбтиве (растворе) других ионов почти всегда в той или иной степени наблюдается обменная адсорбция. При этом адсорбент, поглощая определенное количество каких-либо ионов, одновременно выделяет в раствор эквивалентное количество других ионов того же знака.
количественно описал процесс ионного обмена на твердой поверхности
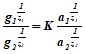 ,
,
где ![]() - количество обменивающихся ионов в адсорбтиве, г-экв/г;
- количество обменивающихся ионов в адсорбтиве, г-экв/г;
![]() - активности обменивающихся ионов.
- активности обменивающихся ионов.
При небольших концентрациях (природные растворы) вместо активности можно пользоваться значением концентрации.
Обменная адсорбция имеет большое значение в земледелии, биологии и технике. Почва (хороший природный адсорбент) способна поглощать и удерживать определенные ионы, например К+ и NH4+, необходимые для питания растений. Взамен этих катионов почва выделяет эквивалентное количество других катионов: H+, Ca2+, Mg2+ и др От природы поглощенных ионов в значительной мере зависят физические и агротехнические свойства почвы.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 |




