Запах воды обусловлен наличием в ней пахнущих веществ, которые попадают в неё естественным путем и со сточными водами. Определение запаха основано на органическом исследовании характера и интенсивности запаха воды при 20о С.
Для определения запаха воды студенты наливают ее в колбу на 2/3 объема с притертой пробкой и сильно встряхивают в закрытом состоянии. Открывают быстро колбу и сразу отмечают интенсивность запаха, используя таблицу:
Балл | Интенсивность запаха | Качественная характеристика |
0 | – | Отсутствие ощутимого запаха |
1 | Очень слабое | Запах, неподдающийся обнаружению потребителем, но обнаруживаемый в лаборатории опытным исследованием |
2 | Слабое | Запах, не привлекающий внимания потребителя, но обнаруживаемый, если на него обратить внимание |
3 | Заметное | Запах, легко обнаруживаемый и дающий повод относиться к воде с неодобрением |
4 | Отчетливое | Запах, обращающий на себя внимание и делающий воду не пригодной для питья |
5 | Очень сильное | Запах настолько сильный, что делает воду непригодной к употреблению |
Определение вкуса
Вкус воды студенты определяют при уверенности, что она безопасна. Кипятят воду в колбе, затем охлаждают ее до комнатной температуры. Небольшой глоток исследуемой воды набирают в рот и держат несколько минут не глотая. Отмечают вкус и наличие привкуса.
Интенсивность вкуса и привкуса выражают в баллах, по пятибалльной системе:
1 балл - очень слабый
2 балла - слабый
3 балла - заметный
4 балла - отчетливый
5 баллов - очень сильный
В норме вкус и привкус воды не должен превышать 2 балла
II. Определение качества воды методами химического анализа
1. Водородный показатель (pH)
Питьевая вода должна иметь нейтральную реакцию (pH – около 7). Значение pH воды водоемов хозяйственного, культурно-бытового назначения регламентируется в пределах 6,5-8,5.
pH в исследуемой воде студенты оценивают с помощью универсальной индикаторной бумаги, сравнивая её окраску со шкалой.
Питьевая вода должна иметь нейтральную реакцию (pH около 7).
В пробирку студенты наливают 5 мл исследуемой воды, 0,1 мл фенолфталеина, перемешивали и по окраске раствора оценивают величину pH:
Розово-оранжевая – pH около 5,
Светло-желтая – 6,
Светло-зеленая – 7,
Зеленовато-голубая – 8.
рН можно определить с помощью индикаторной бумаги, сравнивая её окраску со шкалой.
2. Определение карбонатной жесткости воды
1. Сущность метода
Временная или карбонатная жёсткость воды обусловлена присутствием растворимых солей гидрокарбонатов кальция и магния.
Карбонатная жёсткость воды устраняется кипячением.
Ca(HCO3)2 → CaCO3 + CO2 +H2O
Жёсткость воды определяют, чтобы выяснить ее пригодность для растениеводства, животноводства, для питания, для технических целей (охлаждение двигателей машин).
Карбонатная жёсткость определяют методом нейтрализации. Рабочим раствором является HCI.
Ca(HCO3)2 + 2HCI → CaCI2 + 2CO2 + 2H2O
Mg(HCO3)2 + 2HCI → MgCI2 + 2CO2 + 2H2O
2. Выполнение измерений
В колбу для титрования студенты вносят 100 мл пробы, приливают 3 капли метилоранжа, оттитровывают раствором HCl до розовой окраски.
3. Обработка результатов.
Расчет карбонатной жесткости.
Х=V*1000*N,
Vпр
где V - объем HCl 0,1моль/дм3, израсходованный на титрование, см3
N - нормальность рабочего раствора г-экв./ дм3;
Vпр.- объемы пробы, взятой на анализ, см3;
4. Сходимость результатов.
За результат определения принимают среднее арифметическое двух параллельных определений, расхождение между которыми не превышает 0,01 г-экв./ дм3
2.1 Определение общей жёсткости воды
1. Сущность метода
Комплексонометрический метод определения жёсткости воды основан на способности ионов кальция магния образовывать прочные внутрикомплексные соединения с динатриевой солью этилендиаминтетрауксусной кислоты (Трилон Б).
2. Выполнения измерения.
В колбу для титрования студенты вносят 50 мл пробы. Прибавляют градуированной пипеткой 2,5 мл аммиачно-буферный раствора. Прибавляют 4 капли индикатора хром темно-синий, энергично взбалтывают. Оттитровают 0,01 н раствором Трилона Б по каплям, хорошо перемешивая до перехода сиреневого цвета в синевато – сиреневый. Снимают показания объёма по бюретке и проверяют правильность точки эквивалентности, добавив в колбу для титрования контрольную каплю сли раствор окрасится в синий цвет, то титрование заканчивают.
3. Обработка результатов.
Расчет общей жесткости воды проводится по формуле:
Xж=V*K*N*1000,
Vпр
где V - объем Трилона Б, пошедший на титрование без контрольной капли, мл;
Vпр - объем пробы, взятой на анализ (50 мл);
К - поправка к концентрации Трилона Б 0,01 моль/см3;
N - концентрация Трилона Б 0,01моль/ см3;
1000 - пересчет см3 в.
4. Сходимость результатов.
За результат измерения принимают среднее арифметическое двух параллельных определений, расхождение между которыми не превышает 2% относительных.
Более простой способ для определения карбонатной жесткости:
- студенты наливают в склянку 10 мм анализируемой воды и добавим 5-6 капель фенолфталеина. Возникновение розовой окраски говорит о наличии карбонат-ионов. Если окраска не появляется, то карбонат-ионы в пробе отсутствуют.
3. Обнаружение общего железа
1 метод
Предельно допустимая концентрация (ПДК) общего железа в воде водоемов и питьевой воде составляет 0,3 мг/л, лимитирующий показатель вредности.
Студенты помещают в пробирку 10 мл исследуемой воды, прибавляют одну каплю концентрированной азотной кислоты, несколько капель раствора перекиси водорода и примерно 0,5 мл раствора роданида калия. При содержании железа 0,1мг/л появляется розовое окрашивание, а при более высоком – красное.
2 метод
Приближенное определение ионов Fe+3
Окрашивание, видимое при рассмотрение пробирки сверху вниз на белом фоне | Примерное содержание ионов железа Fe+3 |
Отсутствие Едва заметное желтовато-розовое Слабое желтовато-розовое Желтовато-розовое Желтовато-красное Ярко-красное | менее 0, 05 от 0, 05до 0, 1 от 0, 1 до 0, 5 от 0, 5 до 1, 0 от 1, 0 до 2, 5 более 2, 5 |
Определение
Студенты к 10 мл исследуемой воды прибавляют 1-2 капли HCl и 0,2 мл (4 капли) 50 % раствора KNCS. Перемешивают и наблюдают за развитием окраски.
Fe3+ + 3NCS - = Fe(NCS)3
Определение окисляемости воды
1. Сущность метода
Окисляемость воды вычисляют по количеству кислорода, расходуемого на окисление органических и легкоокисляющихся продуктах (сульфитов, нитритов, железа (II)) пробы в определенных условиях.
Метод основан на окислительно - восстановительной реакции между перманганатом калия (сильным окислителем) и органическими веществами. Рабочим раствором служит перманганат калия KMnO4 0,01 н.
1 этап - получение кислорода на окисления органики и окисления её:
2KMnO4 + 3H2SO4 = K2SO4 + 2MnSO4 + H2O + 5О
2 этап - определение количества перманганата калия, израсходованного на окисление:
2MnO4 + 5H2C2O4 + 3H2SO4 = 2MnSO4 + 10CO2 + K2SO4 +8H2O
Окисляемость воды выражают числом миллиграммов кислорода, израсходованного на окисление 1 дм3 воды.
Вода считается пригодной для хозяйственно - питьевых нужд, если её окисляемость не превышает 3 мг О2/дм3.
2. Подготовка для выполнения измерения.
Предварительная обработка колб для титрования: налить в колбу до половины объема концентрированного KMnO4 + 1 см3 H2SO4 (1:3), закрыть воронкой, прокипятить 3-5 минут, смесь вылить, осадок на стенках колбы растворить в 5 см3 концентрированной соляной кислоты. Колбу ополоснуть дистиллированной водой.
3. Выполнения измерения.
В подготовленную по п. 3 колбу для титрования вносят 2,5 см3 H2SO4 (1:3), точно 10 см3 перманганата калия 0,01 моль/дм3 из заранее подготовленной бюретки и 50 см3 пробы воды (мерной колбой). Колбу зарыть воронкой и смесь прокипятить в течении 10 минут (с момента закипания). Колбу снимают с электроплитки и сразу вносят в неё 10 см3 0,1 н щавелевой кислоты, перемешивают до обесцвечивания. Горячий обесцвеченный раствор титруют раствором KMnO4 0,01 моль/дм3 до появления слабо розовой окраски, неисчезающей 2-3 минуты.
4. Обработка результатов
Окисляемость воды в мг/дм3 рассчитывают по формуле:
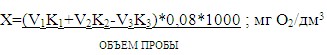
V1- объем KMnO4 введенный в пробу, см3;
V2- объем KMnO4 пошедший на титрование, см3;
V3 - объем раствора щавелевой кислоты, см3;
К1 и К2 - коэффициент поправки и концентрации перманганата калия и щавелевой кислоты соответственно;
0,08 - количество грамм кислорода, соответствующее 1 см3 KMnO4 0,01 моль/дм3 ;
1000 - перевод граммов в миллиграммы.
5. Сходимость результатов.
За результат определения принимают среднее арифметическое двух параллельных определений, расхождение между которыми не превышает 0,30 мг О2/дм3
Определение остаточного хлора в воде
1. Сущность метода.
Обеззараживания воды для хозяйственно - питьевых нужд проводят методом хлорирования. Часть хлора расходуется, а другая часть остается в воде.
Для определения содержания остаточного хлора применяется йодометрический метод анализа.
Рабочим раствором служит тиосульфат натрия вспомогательным раствором - калий йодистый, индикатор - крахмал.
Хлор является сильным окислителем и может вступить в реакцию с тиосульфатом натрия, но мы не можем определить точку эквивалентности в результате отсутствия изменения цвета. В нашем случае применяется заместительное титрование - в пробу вводится вспомогательный раствор калий йод.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |




