Коллигативные свойства разбавленных растворов неэлектролитов. Явление осмоса, роль осмоса в биологических системах, закон Вант-Гоффа для осмоса. Повышение температуры кипения и понижение температуры замерзания растворов, давление пара над раствором (закон Рауля).
Растворы электролитов. Отклонение от законов Вант-Гоффа и Рауля. Теория электролитической диссоциации. Сильные и слабые электролиты. Закон разбавления Оствальда.
Активность, коэффициент активности. Современное представление о кислотах, основаниях, амфотерных электролитах. Кислоты Бренстеда, Льюиса.
Произведение растворимости. Условия образования и растворения осадков.
Ионное произведение воды, водородный показатель рН и его методы определения. Роль рН. Буферные растворы, механизм буферного действия.
9 Гидролиз солей
Факторы, влияющие на гидролиз. Константа и степени гидролиза солей. Полный гидролиз. Расчет рН в растворах солей.
10 Окислительно-восстановительные реакции
Окислительно-восстановительные свойства веществ: окислители, восстановители. Электродные потенциалы металлов. Стандартный потенциал. Понятие о гальваническом элементе. Водородный электрод. Пользование таблицей электродных потенциалов.
Окислительно-восстановительные потенциалы (редокс-потенциалы). Зависимость потенциала от активностей потенциалопределяющих веществ. Уравнение Нернста. Определение направления протекания окислительно-восстановительных реакций с помощью окислительно-восстановительных потенциалов. Окислительно-восстановительные реакции, протекающие в различных средах. Типы окислительно-восстановительных реакций. Метод электронного баланса и электронно-ионный метод составления уравнений окислительно-восстановительных реакций. Роль окислительно-восстановительных реакций в природе.
11 Электрохимические системы
Химическая и электрохимическая коррозия. Методы защиты от коррозии. Электролиз растворов и расплавов солей.
12 Комплексные соединения
Основные положения координационной теории: центральный ион-комплексообразователь, лиганды, координационное число. Геометрия координационной сферы, внешнесферные ионы. Природа хим. связи в комплексах (по методу ВС). Номенклатура комплексных соединений. Диссоциация и устойчивость комплексных соединений в растворах. Константа нестойкости.
Типы комплексных соединений. Роль комплексных соединений, гемоглобин и хлорофилл.
13 Химическая идентификация веществ
Вещество и его чистота. Качественный и количественный анализ. Аналитический сигнал и его виды. Химический, физический и физико-химический анализ. Теоретические основы видов анализа: титриметрический, гравиметрический, потенциометрический, рефрактометрический анализ.
14 Теоретические основы мембранных технологий
Теоретические основы мембранных технологий, современные мембранные материалы. Перспективы развития мембранных технологий.
15 Основные понятия органической химии
Радикалы, гомологические ряды, функциональные группы. Классификация и номенклатура органических веществ. Реакции полимеризации и поликонденсации как основа синтеза полимеров. Современные полимерные материалы. Полимеры и олигомеры. Пластмассы. Применение полимерных материалов в народном хозяйстве. Основные биохимические процессы, их применение в технологии различных отраслей промышленности.
Список рекомендуемой литературы
Основная:
1 Суворов химия : учеб. для вузов / , . - 5-е изд., испр. - СПб. : Химиздат, 2007. – 622с
2 Глинка химия. М.: Интеграл-Пресс, 2007. 727 с.
3 Глинка и упражнения по общей химии. М.: Интеграл-Пресс,2002, 2006. 240 с.
Дополнительная:
1.Суворов и задачи по общей химии: Учеб. пособие для вузов.-СПб.:Химиздат, 2002.-304с.
2. Задачи и упражнения по общей химии:Учеб. пособие для вузов/ , , и др.; Под ред. . ─ 3-е изд.,испр. ─ М.:Высшая школа,2006. ─ 253,[3]с.:ил. ─ Библиогр.:с.255. ─
3. Сергеев : Учеб. пособие для вузов / . 2-е изд. М.: Книжный дом "Университет", 2007. 333 с.
4 Коровин химия. М.: Высшая школа, 2007. 556 с.
Список методических рекомендаций и методических указаний
1 , Пчёлина классы неорганических соединений. - НовГУ, Новгород, 2007. - 26 с.
2 Кузьмичева посуда. – НовГУ, Новгород, 2007. – 6 с.
3 , Летенкова солей. – НовГУ, Новгород, 2007. – 14 с.
4 , Ульянова растворов. Приготовление растворов заданной концентрации. – Новгород, НовГУ, 2007. – 14 с.
5 , , Летенкова диссоциация. – НовГУ, Новгород, 2007. – 6 с.
6 , , Ульянова показатель. – НовГУ, Новгород, 2007. – 6 с.
7 , Летенкова солей. – НовГУ, Новгород, 2007.
– 12 с.
8 , , Ульянова -восстановительные реакции. - НовГУ, Новгород, 2007.- 38 с.
9 , , Петухова элемент. Электрохимическая коррозия металлов. – НовГУ, Новгород, 2007. – 9 с.
10 , , Петухова водных растворов электролитов.– НовГУ, Новгород, 2007. – 9 с.
ТЕСТОВЫЕ ЗАДАНИЯ
Экзамен по химии проводится в письменной форме с использованием экзаменационных тестов. Примеры тестовых заданий приведены на следующих страницах.
ОБРАЗЕЦ
1. Сколько протонов и нейтронов содержит ядро атома 88 Sr?
1.38; 50. 2. 50; 38. 3. 50; 50. 4. 88; 88. 5. 38; 38.
2.Атомы каких элементов имеют в основном состоянии на внешнем энергетическом уровне электронную конфигурацию ns1?
l. V,Nb, Ta. 2. Li, Na, K. 3. Al, Ga, In. 4. Cl, Br, I. 5. Mn, Tc, Re.
3. Какова электронная формула атома палладия?
1. [Kr]4d8s2. 2. [Kr]4d9 s1. 3. [Kr]4d10 5s°. 4. [Kr]4d105s2 5p6.
4. С точки зрения принадлежности к электронным семействам металлы бывают:
1.только s-элементами ; 2. s - и p - элементами ; 3.только d - элементами ; 4.только f - элементами ; 5.представителями всех четырех электронных семейств.5. У какого из элементов наиболее сильно выражены неметаллические свойства?
1.А1. 2. Si. 3.S. 4.С1. 5.Mg.
6. Высшая и низшая степени окисления углерода равны, соответственно:
1.+3;-5. 2.+4;-4. 3.+5;-3. 4.+4; 0. 5. 0;-4.
7. Какое из веществ имеет молекулярную структуру?
1.Т аО2. 2. РbО2. З. ВаО2. 4. СО2. 5. SiO2.
8. Какой тип химической связи имеет место в молекуле SiH4?
1.Ионная. 2.Ковалентная полярная.3.Ковалентная неполярная.4.Водородная.5.Металлическая.
9. Атомная кристаллическая решетка может быть охарактеризована следующим образом:
В узлах - атомы, связи - ковалентные. В узлах - ионы, связи - ионные. В узлах - катионы, связь - металлическая. В узлах - молекулы, связи - водородные или ван-дер-ваальсовы.10. На основании приведенных термодинамических данных ( ∆Gо образования соединений) сделайте вывод, какой неметалл проявляет наибольшую окислительную активность при взаимодействии с магнием:
Мg3N2 MgF2 MgCl2 MgO
∆ Gо298, кДж/моль а)-400 б)-1091 в)-594 г)-567
11. Какой отрезок на диаграмме показывает значение теплового эффекта реакции?
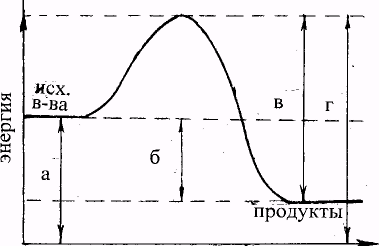
ход реакции
1.а. 2.б. З. в. 4. г.
13. Как можно сместить равновесие вправо в системе
2Р(Т) + ЗН2 (Г) ↔2РН3 (г); ДН > 0 ? (Р - давление, Т - температура.)
1.уменьшить концентрацию Н2; 2.уменьшить Т ; 3.уменьшить Р ; 4.увеличить Р ; 6.увеличить концентрацию РН3.
14. Решить задачу
Определите процентную концентрацию 0,9Н раствора фосфата натрия. Плотность раствора 1,06 г/мл.
15. Расположите вещества в порядке убывания силы электролитов:
а) Н2SeO3 Kд = 3,5 ∙ 10∙-3 б) Н2 S2 O3 Kд = 2,2 ∙ 10-1
в) Н2 С O3 Kд = 4,5 ∙ 10-7 г) Н2 Те O4 Kд= 2,3 ∙ 10-8

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



