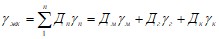 ,
,
где Дм, Дг, Дк – соответственно доля магнетита, гематита и кварца в железистом кварците;
гм, гг, гк – соответственно плотность магнетита, гематита и кварца;
гм = 5,2∙103кг/м3, гг = 5,25∙103кг/м3, гк = 2,64∙103 кг/м3.
гжк=0,35∙5,2∙103 +0,2∙5,25∙103 +0,45∙2,64∙103=4,08∙103кг/м3.
Изменение удельной энтальпии железистого кварцита при нагреве от Т=298 К до Т=400 К равно
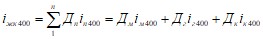
где iм400, iг400, iк400 - соответственно изменение удельной энтальпии магнетита, гематита и кварца, Дж/кг.
Стандартная удельная энтальпия железистого кварцита равна
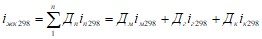 ,
,
где iм298, iг298, iк298 - соответственно стандартная удельная энтальпия магнетита, гематита и кварца (это изменение удельной энтальпии при нагревании тела от Т=0К и доТ=298 К, Дж/кг.
Величина i298 для многих минералов приведена в приложении 1 [ Термодинамика: Учебник. – Москва: МГГУ, 2002. – 441 с.].
Изменение удельной энтальпии происходит по закону
di=Cp(T)dT
Интегрируя последнее выражение, получим применительно к нашему примеру
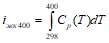 ,
,
где Ср(Т) – изобарная удельная теплоемкость, Дж/(кгК).
Величина Ср(Т) является функцией температуры, для многих минералов ее вид установлен и имеет вид (см. приложение 1) [ Термодинамика: Учебник. – Москва: МГГУ, 2002. – 441 с.]:
![]() , (Дж/кгК),
, (Дж/кгК),
где х, у, z – постоянные;
µ – молекулярная масса минерала, кг/моль.
Для магнетита
х = 39,22; у = 18,86; z = -10,01; µм = 231,55∙10-3 кг/моль,
Для гематита
х = 23,49; у = 18,6; z = -3,55; µг = 159,7∙10-3 кг/моль,
Для кварца
Х = 11,22; у = 8,2; z =-2,7; µк = 60,09∙10-3 кг/моль.
Изменение удельной энтальпии минералов при - нагреве от стандартной температуры Т = 298 К до Т = 400 К будет равно
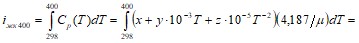
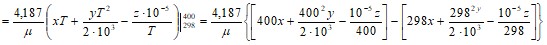 Дж/кг
Дж/кг
Подставляя в последнее выражение значения х, у, z, соответственно для магнетита, гематита и кварца, получим
iм400 = 9,7∙104 Дж/кг; iг400 = 7,7∙104 Дж/кг; iк400 = 105 Дж/кг.
Стандартная удельная энтальпия магнетита, гематита и кварца согласно приложению 1 [ Термодинамика: Учебник. – Москва: МГГУ, 2002. – 441 с.] равна
iм298 = 10,6∙104 Дж/кг; iг298 = 9,75∙104Дж/кг; iк298 = 11,5∙104 Дж/кг.
В итоге получим
![]()
![]() Дж/кг
Дж/кг
![]()
![]() Дж/кг
Дж/кг
Iжк = Iжк298 + Iжк400 = (iжк298 + iжк400)Vгжк =
= (10,83∙104 + 9,44∙104) ∙ 1∙ 4,08∙103 = 8,25∙108 Дж
Задача 5. Определить изменение энтропии 10 кг серы при нагревании ее от температуры T1 = 293 K (20 °C) до T2 = 333 K (60 °C). Средняя удельная теплоемкость серы в данном диапазоне температур равна с = 0,54∙103 Дж/(кгК)/
Решение: согласно уравнению изменения энтропии
![]() Дж/К
Дж/К
Задача 6. Определить энтропию куска железистого кварцита объемом V=1 м3 при температуре Т=498 К (225 ˚С). Минеральный состав железистого кварцита следующий: магнетит Fe3O4 – 35 %, гематит Fe2O3 – 20 %, кварц SiO2 – 45 %.
Решение: Энтропия Sжк куска железистого кварцита объемом 1 м при температуре Т = 498 К равна
Sжк = Sжк298 + Sжк498 = (![]() жк298 +
жк298 + ![]() жк498)Vгжк,
жк498)Vгжк,
где Sжк298 – изменение энтропии железистого кварцита от Т = 0 К до стандартной температуры T = 298 К (стандартная энтропия), Дж/К;
Sжк498 – изменение энтропии железистого кварцита при его нагреве от стандартной температуры Т = 298 К доТ = 498 К, Дж/К;
![]() жк298 – стандартная удельная энтропия железистого кварцита – это изменение удельной энтропии железистого кварцита при нагреве от Т = 0 К до стандартной температуры Т = 298 К, Дж/(кгК);
жк298 – стандартная удельная энтропия железистого кварцита – это изменение удельной энтропии железистого кварцита при нагреве от Т = 0 К до стандартной температуры Т = 298 К, Дж/(кгК);
![]() жк498 – изменение удельной энтропии железистого кварцита при нагревании его от Т = 298 К до Т= 498 К, Дж/(кгК);
жк498 – изменение удельной энтропии железистого кварцита при нагревании его от Т = 298 К до Т= 498 К, Дж/(кгК);
гжк – плотность железистого кварцита, кг/м3.
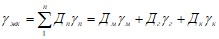 ,
,
где Дм, Дг, Дк – соответственно доля магнетита, гематита и кварца в железистом кварците;
гм, гг, гк – соответственно плотность магнетита, гематита и кварца;
гм = 5,2∙103кг/м3, гг = 5,25∙103кг/м3, гк = 2,64∙103 кг/м3.
гжк=0,35∙5,2∙103 +0,2∙5,25∙103 +0,45∙2,64∙103=4,08∙103кг/м3.
Изменение удельной энтропии железистого кварцита при нагреве его от Т= 298 К до Т = 498 К равно
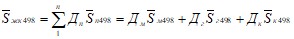
где ![]() м498,
м498, ![]() г498,
г498, ![]() к498 – соответственно изменение удельной энтропии магнетита, гематита и кварца при нагреве от Т = 298 К до Т = 498 К, Дж/(кгК).
к498 – соответственно изменение удельной энтропии магнетита, гематита и кварца при нагреве от Т = 298 К до Т = 498 К, Дж/(кгК).
Стандартная удельная энтропия железистого кварцита равна
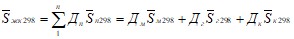
где ![]() м298,
м298, ![]() г298,
г298, ![]() к298 – соответственно стандартная удельная энтропия магнетита, гематита и кварца, Дж/(кгК).
к298 – соответственно стандартная удельная энтропия магнетита, гематита и кварца, Дж/(кгК).
Величина ![]() 298 для многих минералов приведена в приложении 1 [ Термодинамика: Учебник. – Москва: МГГУ, 2002. – 441 с.].
298 для многих минералов приведена в приложении 1 [ Термодинамика: Учебник. – Москва: МГГУ, 2002. – 441 с.].
Изменение удельной энтропии происходит по закону
d![]() = Cp(T)dT/T
= Cp(T)dT/T
или применительно к данному примеру
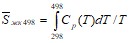 ,
,
где Ср(Т) – изобарная удельная теплоемкость, Дж/(кгК).
Величина Ср(Т) является функцией температуры, для многих минералов ее вид установлен и имеет вид (см. приложение 1) [ Термодинамика: Учебник. – Москва: МГГУ, 2002. – 441 с.]:
![]() , (Дж/кгК),
, (Дж/кгК),
где х, у, z – постоянные;
µ – молекулярная масса минерала, кг/моль.
Для магнетита
х = 39,22; у = 18,86; z = -10,01; µм = 231,55∙10-3 кг/моль,
Для гематита
х = 23,49; у = 18,6; z = -3,55; µг = 159,7∙10-3 кг/моль,
Для кварца
Х = 11,22; у = 8,2; z =-2,7; µк = 60,09∙10-3 кг/моль.
Изменение удельной энтропии минералов при нагреве их от Т = 298 К до Т = 498 К будет равно
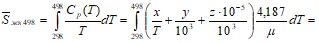
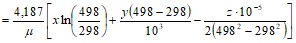 .
.
Подставляя в последнее выражение значения х, у, z и µ соответственно для магнетита, гематита и кварца, получим ![]() м498 = 428 Дж/(кгК);
м498 = 428 Дж/(кгК); ![]() г498 = 415 Дж/(кгК);
г498 = 415 Дж/(кгК); ![]() к498 = 115 Дж/(кгК).
к498 = 115 Дж/(кгК).
Пользуясь приложением 1 [ Термодинамика: Учебник. – Москва: МГГУ, 2002. – 441 с.], определим стандартную удельную энтропию магнетита, гематита и кварца
![]() м298 = 650 Дж/(кгК);
м298 = 650 Дж/(кгК); ![]() г298 = 850 Дж/(кгК);
г298 = 850 Дж/(кгК); ![]() к298 = 687 Дж/(кгК).
к298 = 687 Дж/(кгК).
Окончательно получим
![]()
= 0,35∙650+0,2∙850+0,45∙687=708 Дж/(кгК)
![]()
= 0,35∙428+0,2∙415+0,45∙515=464 Дж/(кгК)
Sжк = (![]() жк298 +
жк298 + ![]() жк498)Vгжк = (708+464)∙1∙4,08∙103=4,4∙106 Дж/К.
жк498)Vгжк = (708+464)∙1∙4,08∙103=4,4∙106 Дж/К.
Задача 7. При нормальном давлении Р=105 Па температура кипения железа равна Т=3023 К (2750˚С). Удельная теплота испарения железа при этом равна r=61,2∙105 Дж/кг. Определить температуру кипения железа, если давление повыситься до 2∙105 Па.
Решение: Универсальная газовая постоянная, отнесенная к одному молю железа, равна R=8,314/µж=8,314/(55,85∙10-3) Дж/(кг∙К), (µж – масса одного моля железа, µж=55,85∙10-3 кг/моль). Согласно фазовым переходам «жидкость пар»

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




