World J Gastroenterol 2005;11(47):7450-7456
World Journal of Gastroenterology ISSN 1007-9327
Влияние Эупатилина (DA-9601) на восстановление слизистой оболочки желудка при повреждении вызванном алкоголем и напроксеном.
TaeYoung Oh, Gook JunAhn, SeulMinChoi, Byoung Ok Ahn, WonBaeKim
Effect of Eupatilin (DA-9601) on the restoration of the gastric mucosa in damage caused by alcohol and naproxen.
Общие характеристики
Цель: изучить эффективность эупатилина, как нового гастропротекторного средства, в лечении повреждений желудка крысы, вызванных этанолом и напроксеном.
МЕТОДЫ: Лабораторным крысам мужского пола предварительно вводили 1 мл 50% этанола два раза в день в течение 5 дней и затем вводили напроксен (50 мг/кг). Эупатилин был введен за 1 ч до напроксена. Через 4 часа после введения напроксена, крысы были умерщвлены. Далее изучалась площадь поражения слизистой оболочки желудка (мм2), гистологические изменения слизистой оболочки и определялся уровень Малонового диальдегида (МДА), Простагландина E2 (PGE2), Глутатиона и Миелопероксидазы (МПО).
РЕЗУЛЬТАТЫ: Предварительное введение этанола и напроксена вызывает желудочные поражения, а также увеличение уровней MДА и MПO. Также введение этанола приводит к уменьшению содержания простагландина E2 и глутатиона в слизистой оболочке желудка. Введение напроксена усугубляет тяжесть поражения.
Эупатилин значительно уменьшил вызванные напроксеном и этанолом повреждения желудка. Эупатилин увеличил содержание в слизистых крыс простагландина E2 и глутатиона и уменьшил уровень MДА и MПO.
ЗАКЛЮЧЕНИЕ: Эти результаты свидетельствуют о том, что потребление алкоголя делает слизистую оболочку желудка более восприимчивой к действию НПВС, отличается снижением эндогенных цитопротекторов, включая простагландин E2 и глутатион, увеличением активации MПO и МДА. Эупатилин, новый гастропротектор, уменьшает уровень повреждения желудка, вызванного применением НПВС и этанола, через многокомпонентный механизм, в котором принимают участие простагландин E2 и глутатион.
ВВЕДЕНИЕ
Последние годы отмечается рост распространенности заболеваний желудочно-кишечного тракта (ЖКТ), как у людей в возрасте 65 лет и старше, так и в молодом возрасте. Наиболее важными и распространенными расстройствами ЖКТ являются гастроэзофагеальная рефлюксная болезнь (ГЭРБ) и пептическая язва желудка. Уровень распространенности язвенной болезни достигает 4-5%.
В начале ХХ века считалось, что пища или стресс являются основными причинными факторами. В последнее время доказана роль генетических и экологических факторов, таким образом, сложная корреляция этих факторов играет большую роль в возникновении повреждений слизистой желудка в настоящее время. Увеличивается число пациентов с повреждением слизистой оболочки желудка в результате повышенной социальной и цивилизационной активности. Основными этиологическими факторами повреждения слизистой оболочки являются Helicobacter pylori (H. pylori), чрезмерное употребление таких лекарств, как нестероидные противовоспалительные препараты (НПВС) и антиагреганты, неправильное питание, пищевые продукты, содержащие ненасыщенные жирные кислоты, например, такие как линолевая кислота, потребление алкоголя, психологический и физиологический стресс. Регулярное лечение с использованием НПВС часто приводит к возникновению диспепсии, язвы, кровотечению и перфорации верхних отделов желудочно-кишечного тракта. Применение НПВС приводит к ингибированию выработки простагландинов (PGE2), увеличению провоспалительных медиаторов, таких как фактор некроза опухоли альфа (ФНО - б) и лейкотриены (LT).
Факторами риска, обусловливающими обострение хронического гастрита на фоне приема НПВС, считаются: возраст, пол, диспепсия, гастроэзофагеальный рефлюкс, а также длительное употребление алкоголя, курение и инфекция H. pylori. Значительно увеличивает риск возникновения кровотечения в верхнем отделе ЖКТ совместное применение НПВС и употребление алкоголя. Алкогольный гастрит впоследствии приводит к нарушению целостности барьера слизистой оболочки желудка.
Поражения желудка, вызванные алкоголем, аналогичны поражениям, вызванным приемом различных НПВС и проявляются – отеком, гиперемией, геморрагиями, эрозиями и кровоизлияниями слизистой оболочки.
Настоящее исследование было проведено с целью изучения влияния НПВС на состояние слизистой оболочки желудка, сенсибилизированной предварительным введением алкоголя, и гастропротективной эффективности эупатилина (Стилен®) при развитии данного поражения, а также с целью выявить основные механизмы действия эупатилина.
Стилен® представляет собой густой экстракт из листьев азиатской полыни (Artemisia asiatica / Artemisia Argyi) и является природным цитопротектором. Лечебные эффекты Стилена® обеспечивает компонент азиатской полыни Эупатилин, который ингибирует образования активных форм кислорода и высвобождение медиаторов воспаления в слизистой оболочке желудка, а также активирует продукцию простагландинов и слизи.
Основные эффекты Стилена® были открыты в начале 90-х годов прошлого века, после чего были проведены доклинические и клинические исследования (28 исследований различного уровня), подтвердившие его клиническую эффективность в отношении эрозивно-язвенных поражений ЖКТ и безопасность приема для человека. В 2002 г. препарат был выпущен на рынок Южной Кореи и сразу получил признание на азиатском рынке, где используется для лечения и профилактики не только НПВС-гастропатии, но и острых и хронических гастритов, в том числе Н. рylori-ассоциированных.
МАТЕРИАЛЫ И МЕТОДЫ
Испытательные материалы и экспериментальные животные.
Методом спиртовой экстракции из полыни Artemisia asiatica / Artemisia Argyi был получен флавоноид эупатилин, который был исследован в ходе анализа методом ВЭЖХ (высокоэффективной жидкостной хроматогрофии) в фармацевтическом институте Dong-A, Корея.
(S)-6-метокса-б-этил-в-нафталинуксусную кислоту (Напроксен), 10% нейтральный формалин, одноосновный фосфат натрия, двухосновный фосфат натрия, хлорид железа (FeCl3), тиобарбитуровая кислота (TBA), трихлоруксусная кислота (ТCА), малондиальдегид (MDA), сульфосалициловая кислота, реактив Эллмана (DTNB), в-никотинамид-аденин-динуклеотид-фосфат восстановленный (в-NADF), глутатионредуктаза, гексадецилтриметиламмония бромид (HTАB), O-дианисидина дигидрохлорид, бычий сывороточный альбумин (BS3) были полученны от Sigma (США).
Для определения уровня PGE2, глутатиона, MПO и МДА использовался набор для радио иммуного анализа (NEN), полученный от Du Pont (США), и p-нитротиофенол, полученный из ТCI (Япония).
Абсолютный этанол, эфир и соляная кислота были приобретены у Дуксана (Корея).
В исследовании использовались 7-недельные здоровые самцы лабораторных крыс, от Чарльз Ривер (Канагава, Япония) прошедшие акклиматизацию в течение 1 недели в стандартных лабораторных условиях [температура: 23 + -2 ℃, влажность: 40-70%, вентиляция: 15-20 / ч, сила света: 150-300 люкс, 12-часовой цикл свет / темнота (освещение: с 7:00 до 19:00)]. Крысам давали стерилизованную УФ-потоком водопроводную воду вволю (вволю) и регулярно наблюдали.
Изучение эффективности эупатилина при остром экспериментальном поражении желудка, вызванном этанолом.
Крысам, голодавшим в течение 24 ч, давали 50% медицинский этанол перорально два раза в день (8: 00 часов и 16: 00 часов) в течение 5 дней. Эупатилин и напроксен (NAP) вводили животным перорально после последнего введения этанол. Крыс разделили на шесть экспериментальных групп:
Группа I: контрольная группа,
Группа II: введение алкоголя,
Группа III: NAP 50 мг / кг без введения алкоголя,
Группа Ⅳ: алкоголь + NAP,
Группа V: эупатилин 60 мг/кг + NAP без введения алкоголя,
Группа Ⅵ: Введение алкоголя + эупатилин 60 мг/кг + NAP.
Через четыре часа после введения NAP, крыс анестезировали эфиром и выполнили полную экстирпацию желудка.
Тринадцать миллилитров физиологического раствора вводили в просвет изолированного желудка и выдерживали в течение 30 мин. Площадь поверхности (мм2) желудочного поражения измеряли с помощью оптического микроскопа (Olympus Ч 10) после гастротомии. Небольшую часть ткани фиксировали в 10% - ном растворе формалина. Слизистую жидкость, собрали на слизистой поверхности желудка и хранили в холодильнике при -74 ℃.
Гомогенизация слизистой желудка.
Замороженную жидкость слизистой оттаивали при комнатной температуре и разбавляли раствором, содержащим 1 мкл буфера Tris-HCl (рН 7,4) на 100 mg и гомогенизируют при 3000 об/мин в течение 10 мин. Супернатант (надосадочная жидкость) хранилась при -20 ° C.
Измерение уровня малонового диальдегида в жидкости слизистой оболочки желудка.
Метод TBA был применен для выполнения измерение MDA. К раствору два миллимоля FeCl3 на литр воды было добавлено 100 мл супернатанта, тщательно перемешали и инкубировали в водяной бане при 37 ° С в течение 30 мин. Затем добавили растворы 30% TCA, 0,75% TBA и 5 моль/л HCl и кипятили для реакции на водяной бане в течение 15 мин. Реакционную смесь охлаждали до комнатной температуры и центрифугировали при 3 000 об/мин в течение 10 мин. Далее была измерена оптическая плотность супернатанта при 550 нм и определено количество MDA (нмоль /л/мг белка).
Измерение простагландина (PG) E2 в жидкости слизистой оболочки желудка.
Количество PGE2 измеряли с помощью набора RIA. После того как проба и индикатор были добавлены в буфер для анализа, их смешали с антисывороткой и инкубировали при t 2-8 ° С в течение 24 ч. Осаждающий реагент добавили к смеси, хорошо встряхнули и затем инкубировали в течение 30 мин при t 2 -8 ° С. Количество PGE2 (pg/mg белка) измеряли при помощи гамма-счетчик с использованием осадка, полученного при центрифугировании при 3 000 об / мин в течение 30 мин.
Измерение количества глутатиона в жидкости слизистой желудка.
Образец, добавленный к 4% раствору сульфосалициловой кислоты, центрифугировали при 3 000 об / мин для устранения белка и при комнатной температуре провели реакцию с 0,1 моль / л буферного раствора фосфата натрия (рН 7,5), содержащего 6 ммоль /л реактива Эллмана, 0,3 ммоль /л никотинамидадениндинуклеотидфосфат ( НАДФ), 50 ед. глутатионредуктазы. Kоличество глутатиона (nmol/мg белка) было рассчитано по поглощению p-нитрофенола, измеренного при 412 нм используя супернатант от центрифугирования при 3000 об / мин в течение 10 мин.
Измерение количества миелопероксидазы в жидкости слизистой оболочки желудка.
Количество миелопероксидазы (МЕ/мг белка) измеряли на слизистой оболочке желудка, повторяя методы предыдущих отчетов. После гомогенизации слизистой оболочки желудка в 0,5% растворе HTAB, содержащем 50 ммоль / л калия фосфат (рН 6,5), гомогенизированные образцы замораживали и размораживали трижды. Супернатант был добавлен в реакционный буфер, содержащий O-дианисидина дигидрохлорид и перекись водорода, и количество миелопероксидазы рассчитывали по поглощению при 460 нм за 1 мин.
Статистический анализ
Данные были выражены как среднее (± стандартное отклонение) и все статистические анализы проводились с использованием SigmaStat ® от Windows 2.0, программного обеспечения (Jandel Corporation, USA). Статистическую значимость оценивали односторонним анализом дисперсии, за которым следовал тест Бонферрони или тест Даннетта на множественное сравнение. Р <0,05 считались значимыми
РЕЗУЛЬТАТЫ
Изучение эффективности эупатилина при остром экспериментальном поражении желудка, вызванном этанолом.
Группа II (алкоголь) - площадь грубого поражения составила (мм2) 16,0 ± 1,8 (табл. 1, рис. 1). Группа III (НПВС) область грубого поражения оставила 30,0 ± 6,0 мм2, так же имелись петехиальное поражение слизистой оболочки желудка.
Группа IV (алкоголь + НПВС) общая площадь поражения составила 65,3 ± 6,7 мм2, что было значительно больше чем в группаах II и III. Слизистая оболочка желудка была со значительным геморрагическим повреждением и кровотечением.
Группа V (эупатилин + НПВС) общая площадь поражения составила 5,0 ± 1,2мм2. Эупатилин значительно ингибирует серьезное желудочное поражение по сравнению с группой III (Р <0,05).
Группа VI (алкоголь) площадь повреждения слизистой оболочки желудка составила 20,0 ± 2,1, что значительно меньше чем в группе IV.
Таблица 1. Динамика показателей МДА, МПО, простагландина Е2 и глутатиона в модели экспериментального поражения слизистой оболочки желудка крыс, вызванного воздействием напроксена, алкоголя и эупатилина.
Группа I Контрольная группа | Группа II Алкоголь | Группа III NAP | Группа Ⅳ алкоголь + NAP | Группа V эупатилин + NAP | Группа Ⅵ Эупатилин+алкоголь + NAP | |
Площадь поражения – мм2 | 0 | 16,0+1,8 | 30,0+6,0 | 65,3+6,7 | 5,0+1,2 | 20,0+2,1 |
МДА – нмоль/л/мг | 3,43+0,44 | 3,66+0,58 | 4,61+0,83 | 5,30+0,89 | 3,16+0,18 | 3,92+0,84 |
PG E2 – пг/мг | 194,5+21,5 | 159,5+30,2 | 62,0+13,8 | 47,1+11,9 | 307,2+27,3 | 180,3+18,3 |
Глутатион – нмоль/мг | 2,01+0,14 | 1,18+0,17 | 1,01+0,21 | 0,55+0,1 | 2,68+0,22 | 2,16+0,28 |
МПО – МЕ/мг | 0,78+0,11 | 1,19+0,27 | 0,92+0,27 | 0,92+0,27 | 0,58+0,04 | 1,08+0,10 |
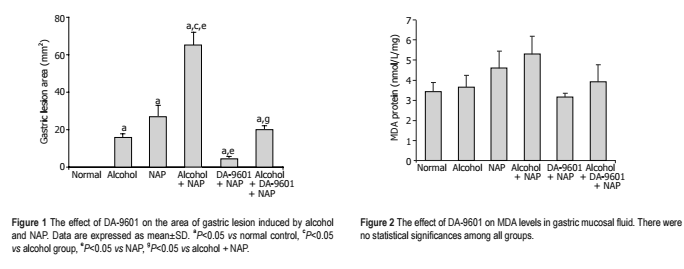
Рисунок 1 Влияние эупатилини на площадь желудочного поражения, вызванного алкоголем и Напроксеном (NAP). Данные выражены как среднее ± SD. а - P <0,05 по сравнению с нормальным контролем, c - Р <0,05 против алкогольной группы, e-P <0,05 по сравнению с NAP, g-P <0,05 по отношению к алкоголю + NAP.
Рисунок 2 Влияние эупатилина на уровень малондеальдегида (MDA) в жидкости слизистой оболочки желудка. Статистических значений среди всех групп нет.
Уровень малонового диальдегида (MДA) в жидкости слизистой оболочки желудка
Уровень MДA (табл. 1, рис. 2) в группе контроля I и II (алкоголь), указывающий на перекисное окисление липидов, составлял 3,43 ± 0,44 (нмоль / л /мг белка) и 3,66 ± 0,58 без значительных отличий между ними. Было обнаружено, что группа III (NAP) и IV (алкоголь + NAP) имели 4,61 ± 0,83 и 5,30 ± 0,89 соответственно. Заметна тенденция к увеличению уровня MDA групп III и IV без статистических различий. В группа V (эупатилин+NAP) определен уровень MDA 3,16 ± 0,18, что на 31,5% ниже по сравнению с группой III (NAP), но это не существенное различие между ними. В случае группы VI (Алкоголь + эупатилин + NAP), уровень MDA был 3,92 ± 0,84 (нмоль / л /мг белка), это меньше на 15,0%, но сопоставимо с Группой IV, статистически значимих различий нет.
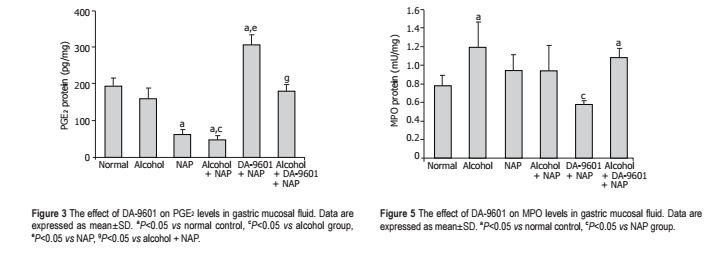
Рисунок 3 Влияние эупатилина на уровни PGE2 в жидкости слизистой желудка. Данные выражены как среднее ± SD. а - P <0,05 по сравнению с нормальным контролем, c - P <0,05 по отношению к группе алкоголя, e - P <0,05 по сравнению с NAP, g - P <0,05 по отношению к алкоголю + NAP.
Рисунок 5 Влияние эупатилина на уровни МПО в жидкости слизистой желудка. Данные выражены как среднее ± SD. а - P <0,05 по сравнению с нормальным контролем, c - Р <0,05 по сравнению с группой NAP.
Уровень простагландина (PG) E2 в жидкости слизистой желудка.
Уровень PGE2 в контрольной группе I составил 194,5 ± 21,5 (мкг / мг белка) (табл.1, рис.3). Уровень простагландина оценивался как маркер цитопротекции. Группа II (алкоголь) уровень PGE2 составил 159,5 ± 30,2, что ниже на 18,0% по сравнению с группой I (группа контроля), но это отклонение не существенно. Группа III (NAP) уровень PGE2 составил 62,0 ± 13,8, что свидетельствует о значительном снижении – на 68,1% (P <0,05). Уровень PGE2 в группа IV (алкоголь + NAP) составил - 47,1 ± 11,9, что ниже на 70,5% по сравнению с группой II (алкоголь) и на 24,0% оказалось ниже по сравнению с группой III (NAP). Уровень PGE2 группы V (эупатилин + NAP) 307,2 ± 27,3, и он был на 57,9% выше, чем нормальный в группе 1 (Р <0,05), и на 395,5% выше, чем у группы III (NAP) (P <0,05). Группа VI (алкоголь + эупатилин + NAP) показала уровень PGE2 180,3 ± 18,3, что аналогично с группой контроля I, но выше на 282,8% (P <0,05) по сравнению с группой IV (алкоголь + НПВС).
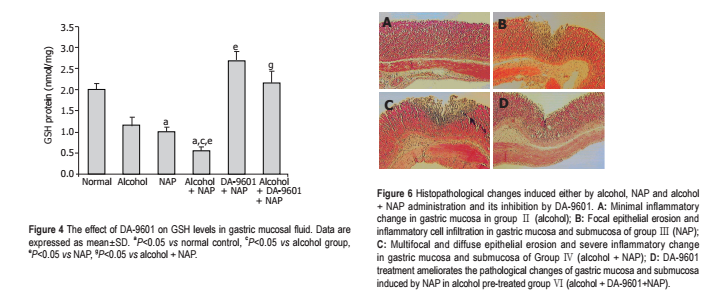
Рисунок 4 Влияние эупатилина на уровнь глутатиона в жидкости слизистой оболочки желудка. Данные выражены как среднее ± SD. а - P <0,05 по сравнению с нормальным контролем, c - P <0,05 по отношению к группе алкоголя, e - P <0,05 по сравнению с NAP, g - P <0,05 по отношению к алкоголю + NAP.
Рисунок 6 Гистопатологические изменения, вызванные алкоголем, NAP и алкоголем+ NAP и их ингибирование эупатилином.
A: Минимальное воспалительное изменение слизистой оболочки желудка в группе II (алкоголь);
Б: Очаговая эпителиальная эрозия и инфильтрация воспалительных клеток в слизистый и подслизистые слои оболочку желудка в III группе (NAP);
C: мультифокальная и диффузная эпителиальная эрозия, тяжелые воспалительные изменения в слизистом и подслизистом слое желудка в IV группе (алкоголь + НПВС);
D: Эупатилин уменьшает патологические изменения в слизистом и подслизистом слое оболочки желудка, индуцированные NAP и алкоголем в группе VI (алкоголь + эупатилин + NAP).
Уровень глутатиона.
Уровни глутатиона в слизистой оболочке желудка (табл.1, рис. 4) были следующими:
в группе I (группа контроля) - 2,01 ± 0,14 (нмоль/мг). В группе II (алкоголь) - 1,18 ± 0,17, что на 41% ниже. В группе III (NAP) - 1,01 ± 0,21, что - на 49,8% ниже. Разница между ними значительная (P <0,05). Уровень глутатиона в IV группе (Алкоголь + NAP) составил 0,55 ± 0,10, что составило разницу в 53,4% и 45,5% из группы II (алкоголь) и группы III (NAP) соответственно. Группа V (эупатилин + NAP) показала 2,68 ± 0,22, это на 165% выше по сравнению с группой III, и это было даже выше, чем у группы I (группа контроля). Уровень глутатиона в группе VI составил 2,16 ± 0,28, что в 4 раза выше, чем в группе IV (P <0,05).
Уровень миелопероксидазы (МПО).
Уровень МПО в группе I (группа контроля) был 0,78 ± 0,11 (табл.1, рис. 5). В то время как группа II (алкоголь) демонстрирует значительное увеличение МПО - 1,19 ± 0,27 по сравнению с контрольной (Р <0,05). Увеличение МПО в группе III (НПВС) - 0,92 ± 0,27 и в группе IV - 0,92 ± 0,27 (алкоголь + NAP), что на 20% ниже по сравнению с контрольной группой Группа V (эупатилин + NAP) показала 0,58 ± 0,04, что ниже на 25,6% по сравнению с группой I (группа контроля) и был значительно меньше по сравнению с группой II (алкоголь) и группе III (NAP) (Р <0,05). Уровень МПО в группе VI (алкоголь + эупатилин + NAP) составил 1,08 ± 0,10, что фактически аналогично группе II (алкоголь) и группе III (NAP).
Гистопатологические исследования
Гистологические изменения изображены на рис. 6
В группе II (алкоголь) наблюдались минимальные воспалительные изменения слизистой оболочки желудка. Группа III (NAP) имела очаговую эпителиальную эрозию и клеточную инфильтрацию в слизистый и подслизистый слои желудка. В группе IV (алкоголь + NAP) желудочное поражение усугублено - мультифокальная и диффузная эпителиальная эрозия, тяжелые воспалительные изменения в слизистом и подслизистом слое желудка. Применение эупатилина уменьшает патологические изменения в слизистом и подслизистом слое оболочек желудка, индуцированные NAP и алкоголем (группа VI).
ОБСУЖДЕНИЕ
В данном исследовании было продемонстрировано, что введение алкоголя или напроксена вызывает поражение слизистой желудка, а совместное их применение значительно увеличивает поражение слизистой желудка. Лечение эупатилином активирует факторы защиты слизистой оболочки желудка, увеличивает регенерацию эпителиального слоя и эффективно уменьшает площадь поражения, вызванного алкоголем и напроксеном.
Этиологическими факторами, которые вызывают повреждение слизистой оболочки желудка являются – стресс, злоупотребление алкоголем, курение, медикаментозные воздействия, переедание, негативные факторы окружающей среды. Вероятность возникновения пептической язвы вследствие комбинации этих причинных факторов резко возрастает. Из медикаментозных препаратов наибольшее этиологическое значение имеют - чрезмерное использование НПВС, пероральных антикоагулянтов (варфарин, аценокумарол, анизиндион, фениндион, дифенадион и т. д.) и кортикостероидных гормонов (триамцинолон, дексаметазон, кортизон, гидрокортизон, преднизолон, преднизон). Прием алкоголя приводит к нарушениям микроциркуляции в слизистой оболочке желудка, вызывает кровоизлияния в слизистой оболочке желудка и отек в подслизистом мышечном слое. Также оказывает прямое раздражающее действие на слизистую оболочку желудка, что приводит к развитию острого гастрита, связанного с микроциркулярным застоем. При повреждении слизистой оболочки желудка возникает ишемия и снижается уровень АТФ в слизистой оболочке желудка, происходит нарушение микроциркуляции. Повреждение желудочно-кишечного тракта вследствие хронического употребления низкой концентрации алкоголя, как правило, не выявляется при грубом исследовании. Однако, если слизистая оболочка желудка подвергается внешнему воздействию дополнительного раздражителя, то поражение желудка становится более серьезным и обширным.
Было продемонстрировано, что эупатилин в дозе 60 мг / кг оказывал выраженное профилактическое и лечебное воздействие на пораженную слизистую оболочку желудка. Также было документально подтверждено, что эти эффекты соответствовали увеличению синтеза простагландина на фоне эупатилина.
Аспирин впервые был синтезирован в 1899 году. В настоящее время в медицинской практике используется множество НПВС. Размер рынка НПВС больше, чем 60 млрд. в год. С каждым годом рынок НПВС увеличивается. Однако прием НПВС вызывает поражение слизистой оболочки желудка. Механизм его развития связан с тем, что НПВС ингибируют циклооксигеназу (ЦОГ), блокируя тем самым синтез простагландина Е2. НПВС вызывают поражение желудочно-кишечного тракта не только за счет снижения уровня простагландина, но также путем прямого индуцирования нейтрофильной инфильтрации в желудочных капиллярах, развитию оксидантного стресса и образования активных радикалов.
Существует несколько методов уменьшения неблагоприятных эффектов НПВС. Прежде всего, аспирин вводится в форме таблетки с кишечнорастворимой оболочкой и прямое раздражение слизистой оболочки желудка предотвращается. Наконец, разработаны НПВС с высокой селективностью к ЦОГ II. Несмотря на эти усилия, 62,2% пациентов, что принимают НПВС на долгосрочной основе, жалуются на клинические осложнения в верхнем отделе желудочно-кишечного тракта, из которых гастрит (38,5%), язва желудка (15,5%), язва двенадцатиперстной кишки (1,9%) были наиболее распространенными. Высокий уровень развития осложнений на фоне приема НПВС имеет мультиэтиологическую природу – прием лекарственных препаратов на фоне нарушения питания (алкоголь, переедание) и стресс.
Было обнаружено, эупатилин повышает уровень выработки простагландина E2 и глутатиона, как в нормальном состоянии, а также при желудочном поражении, вызванном алкоголем или аммиаком. Более того, эупатилин повышал уровень глутатионовой защиты слизистой оболочки желудка, не влияя на эффективность НПВС, когда эупатилин вводили совместно с НПВС у крыс, пораженных артритом. Перекисное окисление кислорода и перекисное окисление липидов рассматриваются как важнейшие этиологические факторы, приводящие к поражению слизистой желудка в результате окислительного стресса. Свободные радикалы кислорода запускают и поддерживают ишемическое состояние в слизистой оболочке желудка, а гидроксильный радикал и супероксид-анион приводят к поражению желудка в силу уменьшения скорости кровотока.
В настоящем исследовании был измерен уровень МДА и MПO которые способствуют поражению слизистой желудка и уровень простагландина E2 и глутатиона, которые являются факторами защиты. Уровень МДА и МПО в группе приема эупатилина уменьшились до уровня контрольной группы, тогда как уровни простагландина E2 и глутатиона были увеличены в группе, получившей эупатилин. Это доказывает эффективность применение эупатилина в лечении и профилактике НПВС индуцированных поражений слизистой оболочки желудка, которая более восприимчива к НПВС на фоне введение алкоголя крысам.
Таким образом гастропротективный эффект Эупатилина осуществляется путем нормализации продукции простагландинов, дополнительного улучшения функции слизистой желудка за счет повышения содержания глутатиона, уменьшения воспаления за счет снижения уровня МДА и MПO. Учитывая все это, следует сделать вывод, что лечение Эупатилином оказывает защитное действие на слизистую оболочку желудка у пациентов, которые регулярно употребляют алкоголь и/или НПВС.



