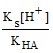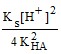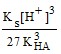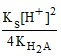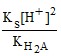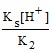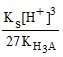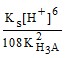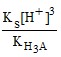so = ![]() = 5,0 ⋅ 10–3 М.
= 5,0 ⋅ 10–3 М.
Расчет ионной силы раствора по формуле I = (0,005 ⋅ 22 + 0,005 ⋅ 22) / 2 = = 0,02 М позволяет затем найти величину коэффициента активности двухзарядного иона из справочных таблиц или вычислить по уравнению Дебая-Хюккеля
lg fi = –0,51 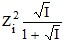 при I ≤ 0,1. (14)
при I ≤ 0,1. (14)
Расчет дает f (Ca2+) = f(SO![]() ) = 0,56, ПРр = ПРт / f
) = 0,56, ПРр = ПРт / f![]() = 8,0 ⋅ 10–5 и s1 = = 8,9 ⋅ 10–3 М, что в 1,8 раза больше значения so, вычисленного без учета ионной силы раствора.
= 8,0 ⋅ 10–5 и s1 = = 8,9 ⋅ 10–3 М, что в 1,8 раза больше значения so, вычисленного без учета ионной силы раствора.
Таким образом, при ПРт > 10–6 при расчете растворимости осадков следует учитывать солевой эффект.
Пример 6. Решить задачу в примере 4 с учетом ионной силы раствора.
Решение. Ионную силу раствора вычисляем с учетом ионов добавленного сильного электролита
Na3PO4 → 3Na+ + PO![]()
по формуле I = 1/2 (0,03 ⋅ 12 + 0,01 ⋅ 32) = 0,06 М, а коэффициенты активности ионов Ва2+ и PO![]() по уравнению (14):
по уравнению (14):
f (Ba2+) = 0,65, f (PO![]() ) = 0,38.
) = 0,38.
Тогда реальное произведение растворимости ПРр = ПРт / (f![]() ⋅ f
⋅ f![]() ) =
) =
= 1,5 ⋅ 10–37 = (3s1)3 ⋅ 0,012, а уточненная растворимость s1 составит
3,8 ⋅ 10–12 М, что в ≈ 3 раза превышает значение s, найденное в примере 4 без учета солевого эффекта.
6. ВЛИЯНИЕ КОНКУРИРУЮЩИХ РАВНОВЕСИЙ
ПРОТОНИРОВАНИЯ И КОМПЛЕКСООБРАЗОВАНИЯ
НА РАСТВОРИМОСТЬ ОСАДКОВ
В реальных условиях на равновесие растворения-осаждения могут оказывать существенное или сильное влияние конкурирующие равновесия протонирования и комплексообразования. В результате связывания ионов малорастворимого соединения в виде недиссоциированных форм слабого электролита (кислоты, основания, комплексов) растворимость осадков возрастает.
6.1. Влияние рН кислой водной среды
Если малорастворимое соединение (соль, гидроксид) содержит ионы с выраженными протолитическими свойствами, его растворимость зависит от водородного показателя (рН) кислой водной среды.
Растворимость солей, образованных анионами сильных кислот, возрастает несущественно при понижении рН среды от 7 до 1 благодаря солевому эффекту. Растворимость кристаллических галогенидов серебра и таллия (I) в воде и кислотах-неокислителях возрастает с увеличением степени ионности галогенидов (15 → 70%) в ряду I → Br → Cl → F [5].
Для расчета условного произведения растворимости по уравнению (8) необходимые значения мольной доли xA свободных анионов An– слабой кислоты HnA определяют по обобщенному уравнению
хA = 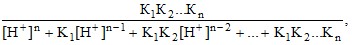 (15)
(15)
где К1, К2,…Кn – ступенчатые константы диссоциации слабой кислоты.
Для гетерогенного равновесия в кислоте-неокислителе
MАn(т) + nH+ (p) ![]() Mn+ (p) + nHA (p),
Mn+ (p) + nHA (p),
термодинамическая константа которого равна К = К![]() , МАn / К
, МАn / К![]() , кислотостойкость солей МАn (A– – F–, CN–, OCN–, NO
, кислотостойкость солей МАn (A– – F–, CN–, OCN–, NO![]() , N
, N![]() и др.) рассчитывается по уравнению
и др.) рассчитывается по уравнению
sn+1 = 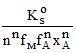 (16)
(16)
с использованием выражения
xA– = 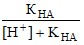 , (15,а)
, (15,а)
а при рН < 3, когда [H+] > KHA, по приближенной формуле
sn+1 ≈ 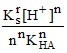 , (17)
, (17)
где ![]() – реальная константа растворимости соли МАn.
– реальная константа растворимости соли МАn.
Пример 7. Вычислить растворимость (моль / л, г / л) кристалла фторида лантана (мембраны фторид-селективного электрода) в чистой воде и в кислоте-неокислителе при рН = 1, если KHF = 6,2 ⋅ 10–4, рК![]() (LaF3) =
(LaF3) =
= 18,40 при 25°С [5].
Решение. Для гетерогенного равновесия в чистой воде
LaF3 (к) ![]() La3+ (р) + 3F– (р)
La3+ (р) + 3F– (р)
so so 3so
растворимость so находим по формуле (4):
so = ![]() = 1,1 ⋅ 10–5 моль / л, или после умножения на молярную массу LаF3 so = 2,2 ⋅ 10–3 г / л. В сильной кислоте (HCl, HClO4) при рН = 1 ионная сила раствора равна 0,1 М, f(La3+) = 0,18 и f (F–) = 0,755 [2], реальное произведение растворимости составит 5,2 ⋅ 10–18 (см. формулу 7).
= 1,1 ⋅ 10–5 моль / л, или после умножения на молярную массу LаF3 so = 2,2 ⋅ 10–3 г / л. В сильной кислоте (HCl, HClO4) при рН = 1 ионная сила раствора равна 0,1 М, f(La3+) = 0,18 и f (F–) = 0,755 [2], реальное произведение растворимости составит 5,2 ⋅ 10–18 (см. формулу 7).
В условиях кислой среды
LaF3 (к) + 3H+ (p) ![]() La3+ (p) + 3 HF (p)
La3+ (p) + 3 HF (p)
при рH = 1, когда [H+] > KHF, растворимость LаF3 вычисляем по формуле (17): s = 9,5 ⋅ 10–4 моль / л, или 0,18 г / л. Полученный результат указывает на невозможность длительного использования мембраны LаF3 в сильнокислой среде.
Для гетерогенного равновесия в кислоте-неокислителе
MmАn(т) + 2nH+ (p) ![]() mM(2n/m)+ (p) + nH2A (p)
mM(2n/m)+ (p) + nH2A (p)
молярную растворимость соли, образованной анионом слабой кислоты Н2А, рассчитывают по уравнению
sm+n = 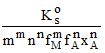 (18)
(18)
с использованием уравнения (15) при n = 2 для молярной доли хА, где А – S2–, CO![]() , SO
, SO![]() , Se2– и др.
, Se2– и др.
Приближенные формулы (табл. 1) расчета растворимости могут быть выведены в зависимости от типа стехиометрии соединения MmAn и соотношения величин рК1 и рК2 слабой кислоты Н2А и рН среды. Например, растворимость малорастворимой соли типа МА, образованной катионом М2+ и анионом А2–, определяют по приближенным формулам:
а) при pH < pK1 (сульфиды MS, карбонаты MCO3)
s ≈ [H+] 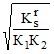 ; (19а)
; (19а)
б) при рК1 < pH < pK2 (сульфиты MSO3, селениты MSeO3)
s ≈ 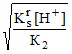 ; (19б)
; (19б)
в) при рК2 < pH (сульфаты MSO4, селенаты MSeO4, дихроматы MСr2O7)
s ≈ ![]() . (19в)
. (19в)
Расчеты показывают, что растворимость сульфидов MS (M – Pb, Cd, Cu, Hg) сильно (в ≈ 107 раз) возрастает при уменьшении рН от 7 до 3 и еще в 200–240 раз при изменении рН от 3 до 1 в основном из-за связывания сульфид-ионов в слабые кислоты HS– и H2S [5]. Растворимость фторидов MF3 (M – Sc, Y, La) при тех же изменениях рН возрастает в 2,3 и 40 раз в основном из-за связывания фторид-ионов в молекулы слабой кислоты HF (см. рисунок).
Пример 8. Какую избыточную концентрацию осадителя Na2C2O4 следует создать при рН 3, чтобы растворимость осадка СаС2О4 (К![]() = 2,3 ⋅ 10–9) не превышала 10–6 моль / л? Ступенчатые константы диссоциации щавелевой кислоты К1 = 5,6 ⋅ 10–2 и К2 = 5,4 ⋅ 10–5 при 25°С. Ионную силу раствора не учитывать.
= 2,3 ⋅ 10–9) не превышала 10–6 моль / л? Ступенчатые константы диссоциации щавелевой кислоты К1 = 5,6 ⋅ 10–2 и К2 = 5,4 ⋅ 10–5 при 25°С. Ионную силу раствора не учитывать.
Т а б л и ц а 1
Приближенные формулы для расчета
молярной растворимости (s) солей в кислых неокислительных средах
Состав соли | Заряд аниона | Формула | Условия |
МА | 1 | s2 ≈ | рH ≤ рК – 1 |
МА2 | s3 ≈ | ||
МА3 | s4 ≈ | ||
М2А | 2 | s3 ≈ | рH ≤ рК1 – 1, рК1 < рК2 |
МА | s2 ≈ | ||
s2 ≈ | рК1 < рН < рК2 | ||
s2 ≈ Ks | РК2 < pH | ||
М3А | 3 | s4 ≈ | рH ≤ рК1 – 1, рК1 < рК2 < рК3 |
М3А2 | s5 ≈ | ||
МА | s2 ≈ |
Примечания к таблице:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |