Расчеты показывают [6], что при увеличении рН или активной щелочности среды молярная растворимость оснований Mg(OH)2, Са(OH)2, Sr(OH)2 и Ва (OH)2 монотонно уменьшается, следуя приближенному уравнению s = Ks / [OH–]2 (см. рисунок, кривые 2 и 3).
При этом эффект сильного понижения растворимости в присутствии общих ОН–-ионов не компенсируется слабым положительным эффектом образования непрочных гидроксокомплексов МОН+ и М(ОН)2.
У Sn (OH)2, как и HgO (рисунок, кривая 6), практически отсутствует эффект общих ионов ОН–. Анализ показывает, что условиями отсутствия этого эффекта являются высокие значения константы устойчивости β2 нейтрального комплекса М(ОН)2 и его молярной доли в чисто водном растворе (х° ≥ 0,9). У Zn(ОН)2 и Со(ОН)2 заметно понижающее (в 2 раза) влияние общих ионов ОН– на растворимость в щелочи, а наиболее сильное влияние (в 350 раз) у Fe(ОН)2 [7].
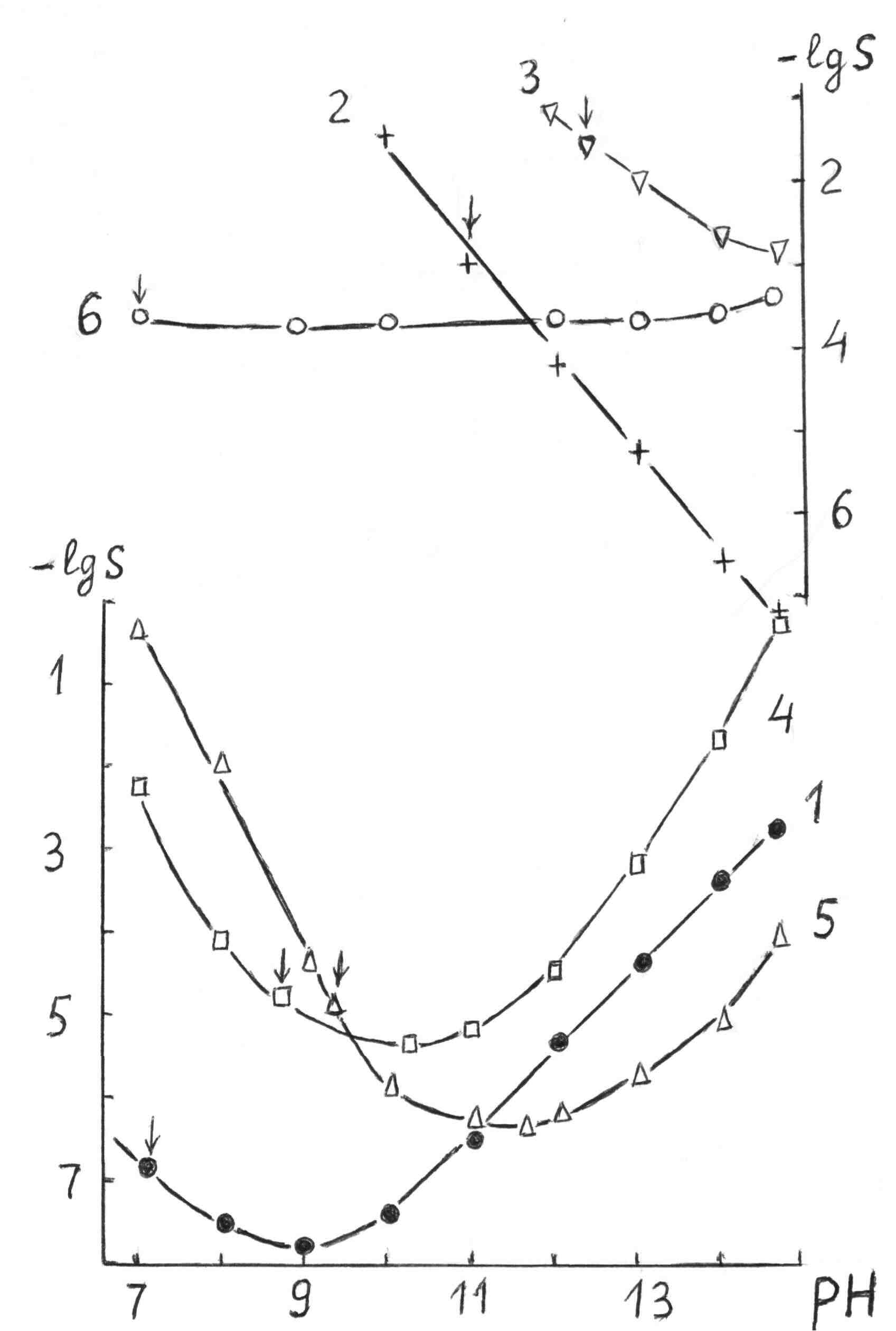
Зависимость растворимости s (моль/л) твердых гидроксидов
от водородного показателя рН водно-щелочной среды при t = 25°C
1 – β-Be(OH)2, 2 – свежеосажденный Mg(OH)2, 3 – Ca(OH)2, 4 – ε-Zn(OH)2,
5 – β-Cd(OH)2, 6 – α-HgO.
7.3. Минимальная растворимость
амфотерных гидроксидов и оксидов
Анализ уравнения (25) приводит к заключению о том, что минимальная растворимость амфотерных гидроксидов М(ОН)n наблюдается при оптимальной концентрации ОН–-ионов, когда среди равновесных частиц в растворе преобладают нейтральные комплексы М(ОН)n. В частности, из условия максимума молярной доли x [M(OH)2] получаем уравнение
2β4 [OH–]4 + β3 [OH–]3 – β1 [OH–] – 2 = 0, (28)
приближенное решение которого с использованием метода Ньютона и констант βi позволяет найти оптимальные значения [OH–]opt и затем smin по формуле (25) [6, 7].
Пример 17. С учетом образования гидроксокомплексов рассчитать рН наиболее полного осаждения, минимальную и собственную растворимость в водно-щелочной среде стабильной модификации ε – Zn (OH)2. K![]() =
=
= 3,3 ⋅ 10–17 [6]. Общие константы устойчивости гидроксокомплексов цинка (II):
β1 = 1,1 ⋅ 106, β2 = 1,3 ⋅ 1011, β3 = 4,0 ⋅ 1013, β4 = 6,3 ⋅ 1014.
Решение. Упрощая уравнение (28), получим приближенное уравнение
x(β3x2 – β1) = 0,
откуда x = [OH–] ≈ 1,66 ⋅ 10–4 М. Уточняя методом Ньютона найденную величину [OH–] в уравнении (27), получим [OH–]opt = 1,67 ⋅ 10–4 М и рНopt =
= 10,22. По уравнению (25) находим smin = 4,9 ⋅ 10–6 моль / л, или 0,5 мг / л. Мольные доли Zn2+, ZnOH+, Zn(OH)2, Zn(OH)![]() и Zn(OH)
и Zn(OH)![]() , вычисленные по формуле типа (21), равны соответственно 0,03, 4,73, 90,45, 4,78 и 0,01 мол. %.
, вычисленные по формуле типа (21), равны соответственно 0,03, 4,73, 90,45, 4,78 и 0,01 мол. %.
Собственная растворимость гидроксида ε – Zn(OH)2, определяемая равновесной молярностью нейтральных комплексов Zn(OH)2 в растворе, равна Ksβ2 = 4,4 ⋅ 10–6 моль / л, или 0,905 smin.
Расчет растворимости ε – (ZnOH)2 при рН = 10,22 по формуле (13) без учета образования гидроксокомплексов дает некорректное значение 1,2 ⋅ 10–9 М (в 3,8 ⋅ 103 раз меньше).
Оксиды как продукты реальной или условной дегидратации гидроксидов сохраняют химические свойства последних. Осньвные оксиды щелочных и щелочноземельных металлов химически реагируют с водой, образуя растворимые гидроксиды. Амфотерные оксиды (ZnO, BeO, SnO, PbO, Al2O3, Cr2O3 и др.) в воде практически нерастворимы, реагируют с кислотами и концентрированными щелочами, полностью или заметно растворяясь. Химическая активность и растворимость аморфных оксидов выше, чем прокаленных и стабильных кристаллических оксидов. Гетерогенное химическое равновесие растворимости твердых оксидов
МОm/2 (т) + ![]() Н2О (ж)
Н2О (ж) ![]() Мm+ (р) + mOH– (p) (29)
Мm+ (р) + mOH– (p) (29)
характеризуется константой K![]() = [Mm+] [OH–]m, как и для гидроксидов.
= [Mm+] [OH–]m, как и для гидроксидов.
Пример 18. Рассчитать растворимость в чистой воде (s°) и минимальную растворимость в водно-щелочной среде (smin) неактивной гексагональной формы ZnO при 25°С, используя константу равновесия K![]() = 1,5 ⋅ 10–17 [1]
= 1,5 ⋅ 10–17 [1]
для реакции
ZnO (к) + H2O (ж) = Zn2+ (р) + 2ОН– (р)
и константы устойчивости гидроксокомплексов цинка (см. пример 17).
Решение. Как и в примере 15, решаем систему трех уравнений (26) с использованием метода Кардано для кубического уравнения. При дискриминанте D = 5,828 ⋅ 10–35 > 0 имеем один действительный корень Z1 = [OH–] =
= 4,78 ⋅ 10–6 М, откуда рН° = 8,68 и s° = 6,0 ⋅ 10–6 М, или 0,5 мг/л. В водном растворе преобладают Zn(OH)+ (57,5 %), Zn(OH)2 (31,5 %) и Zn2+ (10,9 мол. %).
Решая уравнение (28), находим [OH–]opt = 1,67 ⋅ 10–4 М (см. пример 17) и затем по уравнению (25) вычисляем smin = 2,2 ⋅ 10–6 моль / л, или 0,2 мг ZnO / л.
8. КОЛИЧЕСТВЕННАЯ ОЦЕНКА АМФОТЕРНОСТИ
ГИДРОКСИДОВ И ОКСИДОВ В ВОДНЫХ СРЕДАХ
Амфотерные гидроксиды и оксиды с химическими связями М – О, близкими по степени ионности к связи О – Н, реагируют с кислотами и щелочами, присоединяя или отдавая протоны и гидроксид-ионы, например:
М(ОН)2 + Н+ = МОН+ + Н2О,
М(ОН)2 + ОН– = М(ОН)![]() ,
,
Н2МО2 = Н+ + НМО![]() ,
,
М(ОН)2 = МОН+ + ОН–,
МО + 2Н+ = М2+ + Н2О,
МО + 2ОН– = МО![]() + Н2О.
+ Н2О.
Условием амфотерности оксидов МОm/2 и гидроксидов М(ОН)m является неравенство ![]() > m, где
> m, где ![]() – функция Бьеррума, или среднее лигандное число в моноядерных гидроксокомплексах при рН = 15 [6, 7] вычисляется по формуле
– функция Бьеррума, или среднее лигандное число в моноядерных гидроксокомплексах при рН = 15 [6, 7] вычисляется по формуле
![]() =
= ![]() , (30)
, (30)
в которой мольные доли xi комплексов М(ОН)i определяются с использованием констант устойчивости βi и [OH–]. В частности, условие амфотерности ![]() > 2 выполняется для оксидов и гидроксидов Ве, Zn, Cd, Hg, Sn, Pb, Mn – Cu [7] и не выполняется для соединений Mg – Ba [6].
> 2 выполняется для оксидов и гидроксидов Ве, Zn, Cd, Hg, Sn, Pb, Mn – Cu [7] и не выполняется для соединений Mg – Ba [6].
Для количественной оценки амфотерности гидроксидов и оксидов предложено в [6, 7] использовать величину отношения (А > 1) их молярных растворимостей в сильнощелочной среде с рН = 14,7 (5 М раствор NaOH) и в чистой воде (табл. 2).
Пример 19. Оценить параметр амфотерности А неактивной гексагональной формы ZnO (K![]() = 1,5 ⋅ 10–17, s° = 6,0 ⋅ 10–6 М, см. пример 18) в водно-щелочной среде при 25°С.
= 1,5 ⋅ 10–17, s° = 6,0 ⋅ 10–6 М, см. пример 18) в водно-щелочной среде при 25°С.
Решение. Условие амфотерности ZnO и Zn(OH)2 выполнено (![]() =
=
= 3,99 > 2). Для оценки параметра амфотерности А в виде отношения s (рН = 14,7) / s° (H2O) вычислим молярную растворимость ZnO (к) в водной среде с рН = 14,7 по уравнению (25), используя [ОН–] = 5 M, f (Zn2+) ⋅
⋅ f(OH–)2 ≈ 1 и константы устойчивости βi, приведенные в примере 17:
s (рН = 14,7) = 1,5 ⋅ 10–17 (0,04 + 2,2 ⋅ 105 + 1,26 ⋅ 1011 + 1,99 ⋅ 1014 +
+ 1,58 ⋅ 1016) = 0,24 моль / л.
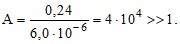
При рН = 14,7 преобладает комплекс Zn(OH)![]() (98,8%).
(98,8%).
Из табл. 2 видно, что параметр амфотерности А гидроксидов М(ОН)2 изменяется в широком диапазоне. Наиболее высокая растворимость при рН = 14,7 у амфотерных гидроксидов олова (II) и цинка (0,76 и 0,52 моль / л при 25°С). Согласно [2] полное растворение выпавшего осадка этих гидроксидов происходит при рН = 13,5 и 12,5, а Al(OH)3 – при рН = 10,8. Несмотря на высокие значения параметра А, растворимость гидроксидов бериллия и меди (II) в 5 М NaOH мала (1 ⋅ 10–3 и 0,015 моль / л) из-за низких величин K![]() и s° (табл. 2).
и s° (табл. 2).
Увеличение растворимости большинства амфотерных гидроксидов наблюдается при нагревании и повышении концентрации щелочи NaOH (до 19 моль / л) или КОН (до 14 моль / л), а также в кислых средах [1, 2].
Т а б л и ц а 2
Рассчитанные термодинамические параметры растворения стабильных
кристаллических гидроксидов в воде и щелочи при 25°С [6, 7]
Гидроксид | рК | Н2О | NaOH | A | |||
x°(M2+), мол. % | рН° | ps° | pHopt | psmin | |||
Sn(OH)2 | 26,20 | 10–5 | 7,02 | 5,26 | 7,11 | 5,26 | 1,3 ⋅ 105 |
Pb(OH)2 | 19,64 | 61 | 7,6 | 6,61 | 10,2 | 8,69 | 8 ⋅ 104 |
ε-Zn(OH)2 | 16,48 | 14 | 8,7 | 4,82 | 10,2 | 5,34 | 4 ⋅ 104 |
Cu(OH)2 | 19,55 | 65 | 7,6 | 6,62 | 9,9 | 8,67 | 6 ⋅ 104 |
β-Be(OH)2 | 22,39 | 2 | 7,1 | 6,86 | 8,9 | 7,89 | 8 ⋅ 103 |
Ni(OH)2 | 17,20 | 96 | 8,4 | 5,93 | 10,2 | 8,10 | 26 |
Mn(OH)2 | 12,76 | 84 | 9,9 | 4,40 | 11,5 | 6,36 | 15 |
β-Co(OH)2 | 15,64 | 80 | 8,8 | 5,16 | 10,9 | 6,22 | 13 |
Fe(OH)2 | 16,38 | 88 | 8,7 | 5,62 | 10,8 | 8,16 | 12 |
β-Cd(OH)2 | 14,27 | 83 | 9,4 | 4,88 | 11,6 | 6,40 | 6 |
β-HgO | 25,55 | 10–3 | 7,02 | 3,71 | 8,9 | 3,72 | 1,6 |
Библиографический список
1. , , Произведения растворимости. Новосибирск: Наука, 1983. 267 с.
2. Справочник по аналитической химии. М.: Химия, 1989. 448 с.
3. , Задачи и вопросы по аналитической химии. М.: Изд. МГУ, 1984. 216 с.
4. Расчеты равновесий в аналитической химии. Л.: Химия. 1984. 184 с.
5. Термодинамический расчет растворимости кристаллических галогенидов и сульфидов в воде и кислых средах // Журнал прикладной химии. 2003. Т. 76. № 11. С. 1785–1787.
6. Термодинамический расчет растворимости твердых гидроксидов М(ОН)2 в воде и щелочных средах // Журнал прикладной химии. 2004. Т. 77. № 8.
С. 1271–1274.
7. Термодинамическая характеристика амфотерности гидроксидов М(ОН)2 в водных средах // Журнал прикладной химии. 2005. Т. 78. № 11. С. 1819–1823.
8. Термодинамические свойства растворов электролитов. М.: Высшая школа, 1982. 320 с.
9. Термодинамические свойства индивидуальных веществ / Под ред. . М.: Наука, 1979–1981. Т. 1–4.
Оглавление
1. Растворимость твердых электролитов в воде 3
2. Произведение растворимости 4
3. Способы выражения произведения растворимости 6
4. Растворимость осадков в присутствии общих ионов 8
5. Растворимость осадков с учетом влияния ионной силы раствора 9
6. Влияние конкурирующих равновесий протонирования
и комплексообразования на растворимость осадков 11
6.1. Влияние рН кислой водной среды 11
6.2. Влияние гидролиза ионов осадка 16
6.3. Влияние комплексообразования катиона 17
7. Термодинамический расчет растворимости
твердых гидроксидов и оксидов в воде и щелочных средах 19
7.1. Растворимость в чистой воде 20
7.2. Растворимость в сильнощелочной среде 21
7.3. Минимальная растворимость амфотерных гидроксидов
и оксидов 23
8. Количественная оценка амфотерности гидроксидов и оксидов
в водных средах 25
Библиографический список 27
Евгений Васильевич Школьников
РАСЧЕТЫ РАСТВОРИМОСТИ
СОЛЕЙ, ГИДРОКСИДОВ И ОКСИДОВ
В ВОДНЫХ СРЕДАХ
Методические указания
по общей, неорганической и аналитической химии
для студентов и аспирантов технологических
и технических специальностей вузов

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



