Пример 14. Рассчитать растворимость свежеосажденного основания Mg(OH)2 (ПРт = 6 ⋅ 10–10) в 0,1 М растворе NaOH с учетом ионной силы раствора и образования гидроксокомплекса MgOH+ (β1 = 3,6 ⋅ 102).
Решение. Растворимость аморфного Mg (OH)2 в чистой воде вычисляем по формуле (4)
s° = (ПРт / 4)1/3 = 5,3 ⋅ 10–4 М.
В щелочном 0,1 М растворе NaOH гетерогенное равновесие
Mg(OH)2 (a) ![]() Mg2+ (p) + 2OH– (p)
Mg2+ (p) + 2OH– (p)
s s 2s + 0,1 ≈ 0,1
сместится влево из-за увеличения концентрации гидроксид-ионов, общих с анионами осадка, и растворимость s основания уменьшится.
Рассчитаем сначала величину s без учета комплексообразования, но с учетом ионной силы раствора с использованием формул (7) и (4):
I = C (NaOH) = 0,1 M, f (Mg2+) = 0,45, f (OH–) = 0,76 [2], ПРр = 6 ⋅ 10–10 /
/ (0,45 ⋅ 0,762) = 2,3 10–9, s = ПРр / [OH–]2 = 2,3 ⋅ 10–7 M << s°.
С учетом гомогенного равновесия в щелочном растворе
Mg2+ + OH– ![]() MgOH+
MgOH+
с константой β1 найдем мольную долю свободных катионов Mg2+ по формуле (21)
x (Mg2+) = 1 / (1 + β1 [OH–] = 2,7 ⋅ 10–2,
условное произведение растворимости Mg(OH)2
ПРу = ПРр / x (Mg2+) = 8,6 ⋅ 10–8
и вычислим растворимость s′ = ПРу / [OH–]2 = 8,6 ⋅ 10–6 М. Полученное значение s′ в 37 раз превышает величину s, вычисленную без учета комплексообразования катиона магния, но в 62 раза меньше растворимости s° в чистой воде (влияние общих ионов ОН– преобладает).
7. ТЕРМОДИНАМИЧЕСКИЙ РАСЧЕТ РАСТВОРИМОСТИ
ТВЕРДЫХ ГИДРОКСИДОВ И ОКСИДОВ В ВОДЕ
И ЩЕЛОЧНЫХ СРЕДАХ
Влияние величины рН на растворимость гидроксидов металлов в водно-щелочной среде представляет интерес при определении условий гидролиза, практически полного осаждения или эффективного маскирования катионов в виде растворимых гидроксокомплексов.
В водном растворе, насыщенном относительно малорастворимого гидроксида M(OH)m, устанавливается гетерогенное химическое равновесие
M (OH)m (т) ![]() Mm+(p) + mOH– (p), (22)
Mm+(p) + mOH– (p), (22)
термодинамическая константа которого определяется выражением
K![]() = ПРт = а (Мm+) am(OH–) = const (Т). (23)
= ПРт = а (Мm+) am(OH–) = const (Т). (23)
Значения константы растворимости находят в справочниках, например [2] или рассчитывают [6, 7] с использованием термодинамического соотношения
lg K![]() = – 0,175 ΔG
= – 0,175 ΔG![]() , (10,а)
, (10,а)
где ΔG![]() – стандартное изменение энергии Гиббса (кДж / моль), которое для процесса растворения (22) вычисляют по уравнению
– стандартное изменение энергии Гиббса (кДж / моль), которое для процесса растворения (22) вычисляют по уравнению
ΔG![]() = ΔG
= ΔG![]() (Mm+) + mΔG
(Mm+) + mΔG![]() (OH–) – ΔG
(OH–) – ΔG![]() [M(OH)m]. (24)
[M(OH)m]. (24)
Значения ΔG![]() образования ионов в водных растворах приведены в работе [8], величины ΔG
образования ионов в водных растворах приведены в работе [8], величины ΔG![]() образования аморфных и кристаллических модификаций гидроксидов при 298 К – в справочнике [9].
образования аморфных и кристаллических модификаций гидроксидов при 298 К – в справочнике [9].
Молярную растворимость M(OH)m в чистой воде и водно-щелочной среде рассчитывают с учетом ионной силы раствора и образования моноядерных гидроксокомплексов [2] по обобщенному уравнению
s = CM = 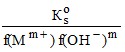
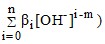 , (25)
, (25)
где СМ – общая молярность всех химических форм М в насыщенном растворе; βо = 1, (β1, β2, … , βi – общие константы устойчивости гидроксокомплексов MOH(m–1)+ , …, М(ОН)![]() .
.
7.1. Растворимость в чистой воде
Концентрацию свободных анионов ОН– и величину рНо насыщенных растворов гидроксидов или оксидов в чистой воде измеряют рН-метром или находят путем решения системы трех (четырех) уравнений [6, 7] например для гироксидов M(OH)2 или оксидов МО:
[M2+] [OH–]2 = K![]() ,
, 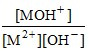 = β1, (26)
= β1, (26)
2 [M2+] + [MOH+] = [OH–]
с использованием метода Кардано для кубического уравнения.
В расчетах для неустойчивых твердых гидроксидов, например для ртути (II), и малорастворимых оксидов МО учитывают химические равновесия
МО (т) + Н2О (ж) ![]() М (ОН)2 (р)
М (ОН)2 (р) ![]() М2+ (p) + 2OH– (p). (27)
М2+ (p) + 2OH– (p). (27)
Пример 15. Вычислить рН° насыщенного раствора и молярную растворимость s° кристаллической β-модификации Cd (OH)2 в чистой воде при 25°С. K![]() (β – Cd (OH)2) = 5,4 ⋅ 10–15 [6]. Общие константы устойчивости гидроксокомплексов кадмия (II): β1 = 8,3 ⋅ 103, β2 = 4,5 ⋅ 107, β3 = 5,0 ⋅ 108,
(β – Cd (OH)2) = 5,4 ⋅ 10–15 [6]. Общие константы устойчивости гидроксокомплексов кадмия (II): β1 = 8,3 ⋅ 103, β2 = 4,5 ⋅ 107, β3 = 5,0 ⋅ 108,
β4 = 4,5 ⋅ 108.
Решение. В водном растворе Cd (OH)2 преобладают катионы Cd2+, комплексы CdOH+ и анионы ОН–. Равновесную молярность [OH–] = Z и рН° найдем, решая систему трех уравнений (26). Получим кубическое уравнение
Z3 + pZ + q = 0,
где р = – K![]() β1, q = –2 K
β1, q = –2 K![]() . Используя метод Кардано, вычисляем дискриминант уравнения D = (p / 3)3 + (q / 2)2. При D = 2,916 ⋅ 10–29 > 0 имеем один действительный корень Z1 = [OH–] = 2,3 ⋅ 10–5 M, откуда рН° = 9,36.
. Используя метод Кардано, вычисляем дискриминант уравнения D = (p / 3)3 + (q / 2)2. При D = 2,916 ⋅ 10–29 > 0 имеем один действительный корень Z1 = [OH–] = 2,3 ⋅ 10–5 M, откуда рН° = 9,36.
Молярную растворимость гидроксида кадмия в чистой воде вычисляем по упрощенной формуле (25), так как I < 10–4 M и fi = 1:
s° = 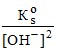 (1 +
(1 + 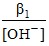 + β2 + β3 [OH–] + β4[OH–]2) = 1,3 ⋅ 10–5 М
+ β2 + β3 [OH–] + β4[OH–]2) = 1,3 ⋅ 10–5 М
Расчет s° без учета комплексообразования по формуле (4) дает 1,1 ⋅ 10–5 М (на 20% меньше).
Растворимость свежеосажденных аморфных гидроксидов выше, чем кристаллических модификаций. Растворимость последних заметно зависит от структуры, уменьшаясь при переходе к стабильным модификациям [6, 7]. Причиной возникновения метастабильных донных фаз с повышенной энергией и растворимостью является кинетическая заторможенность тех или иных стадий формирования равновесных кристаллических осадков [1].
7.2. Растворимость в сильнощелочной среде
Влияние образования гидроксокомплексов на растворимость гидроксидов и оксидов усиливается при добавлении щелочи.
Пример 16. Вычислить молярную растворимость β-Cd(OH)2 в 0,01 М и 1 М растворах NaOH с учетом комплексообразования и ионной силы раствора (см. константы K![]() и βi в примере 15).
и βi в примере 15).
Решение. Из-за влияния общих ионов ОН– в сильнощелочной среде NaOH гетерогенное равновесие растворимости должно сместиться в сторону образования осадка гидроксида кадмия. Противоположное (положительное) влияние на растворимость оказывают солевой эффект и особенно образование гидроксокомплексов кадмия (II). При рН = 12 и K![]() = 9,9 ⋅ 10–15 расчет по формуле s = K
= 9,9 ⋅ 10–15 расчет по формуле s = K![]() / [OH–]2 дает s = 1,1 ⋅ 10–10 М, а по формуле (25) – 5,0 ⋅ 10–7 М (различие в 4,6 ⋅ 103 раз).
/ [OH–]2 дает s = 1,1 ⋅ 10–10 М, а по формуле (25) – 5,0 ⋅ 10–7 М (различие в 4,6 ⋅ 103 раз).
При рН = 14, [OH–] = 1 М и K![]() = 1,06 K
= 1,06 K![]() = 5,7 ⋅ 10–15 расчет растворимости по тем же формулам (4) и (25) дает значения соответственно 5,7 ⋅ 10–15 М и 6 ⋅ 10–6 М (различие в ≈109 раз). Вместе с тем из-за невысокой прочности гидроксокомплексов кадмия (II) растворимость Cd(OH)2 в 0,01
= 5,7 ⋅ 10–15 расчет растворимости по тем же формулам (4) и (25) дает значения соответственно 5,7 ⋅ 10–15 М и 6 ⋅ 10–6 М (различие в ≈109 раз). Вместе с тем из-за невысокой прочности гидроксокомплексов кадмия (II) растворимость Cd(OH)2 в 0,01
и 1 М растворах NaOH меньше растворимости в чистой воде (s° = 1,3 ⋅ 10–5 М). Расчет показывает, что в 5 М растворе NaOH отношение s / s° ≈ 6 [6], т. е. Cd(OH)2 заметно амфотерен, в отличие от Mg(OH)2 (см. рисунок).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



