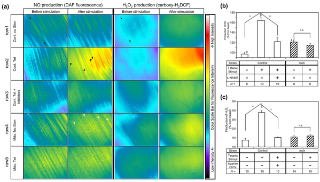
Хотя EDHF не полностью идентифицировали, предыдущие исследования продемонстрировали производство перекиси водорода (H2O2) при помощи флуоресценции карбокси - H2- DCFDA (2 ' ,7 - дихлор-дигидрофлюоресцеина диацетата ), как EDHF функция [22]. В этом исследовании H2O2 производство в грудино-сосцевидной мышце сравнивали между контролем и MDX мышами с помощью карбокси - H2- DCFDA. Прямая тетаническая стимуляция мышцу индуцировала производство H2O2 в миоцитах у контрольных мышей (фиг. 2а и в). Хорошо известно, что фармакологические препараты, включая комбинации апамина и карибдотоксина [34] , ингибируют EDHF путем противодействия активированным кальциево - калиевым каналам эндотелиальных клеток сосудов в естественных условиях [34] , [35] . Производство Н2О2 мышечными волокнами ингибировалось комбинированным применения апамина и карибдотоксина (рис. 2а права третьих панели, 2с 3-я колонка ) . Увеличение количества Н2О2 обнаруженое после тетанической стимуляции уменьшалось у MDX мышей (рис. 2а правой нижней панели, 2с крайней правой колонке ) . Эти эксперименты показывают, что в грудино-сосцевидной мышце контрольных мышей, как NO, так и Н2О2 увеличиваются после тетанических стимулов, в то время как у мышей MDX тетаническая стимуляция не увеличивает производство обеих молекул, что может быть потенциальной причиной нарушенной регуляции потока. Фармакологические изменение функциональной ишемии предотвращает повреждение при физической нагрузке мышечных волокон у MDX мышей. Эксперименты были разработаны, чтобы определить, происходит ли улучшение микроциркуляции путем пополнения NO у мышей MDX (рис. 1б), что может предотвратить сокращение-индуцированную гибель клеток. Использовав DiOC6 ,мембранный потенциал-зависимых красителей, которые включены в митохондриях и эндоплазматической сети (М / ER) только в живых клетках ( рис. 3а) , мы следовали хронологические изменения в морфологии мышечных волокон в естественных условиях и подсчитывали количество поврежденных мышечных волокон. Преимуществом этого метода является то, что волокна уже погибшие до лечения не окрашенны (рис. 3б ), а волокна повреждены после окрашивания могут быть обнаружены (рис. 3в). Таким образом, стало возможным оценить специфический эффект сокращения мышц и / или фармакологического вмешательства.
![]()
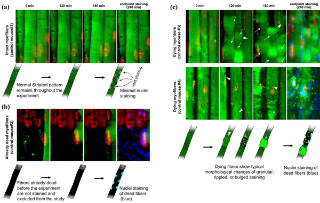
Интактные мышечные волокона показали зеленый флуоресцентный сигнал кластеров M / ER (рис. 3а). Для количественной оценки повреждения мышечных волокон, мы рассчитывали количество поврежденных локусов (локусе), а не количество поврежденных волокон, потому что существуют различные типы повреждений наблюдаемые по всей длине мышечных волокон (см. методы подробно). Смерть локусов мышечных волокон и у мышей показали нарушенный внутриклеточный характер распределения зеленой флуоресценции. Гибель клеток была подтверждена исключением окрашивания красителем (конечная точка синего цвета на фиг.3) и аннексина V-окрашивание (рис. S3, вспомогательную информацию). Это результат в естественных условиях исследования подтверждает ранее проведенный морфологический анализ митохондриальной аномалии в скелетных мышцах при токсин-индуцированной гибели клеток [36], [37] и мышечной дистрофии [38]. Мышечное волокно с признаками повреждения (гранулированный, рябь, и избыточное окрашивание DiOC6) не вернулось к нормальной поперечно-полосатой окраске после длительного покадрового наблюдения до 12 часов. Морфологические изменения указанные выше считаются необратимыми и мышечное волокно, проявляющее эти характеристики, действительно умирает. Процедура окрашивания не влияет на жизнеспособность мышц и сохранность миофибрилл, миофибриллы сохранили свою нормальную поперечно-полосатую модель M / ER во время наблюдения (рис. 3а). Тетаническая стимуляция (6 раз повторяю, продолжительностью 5 секунд при 50 Гц), индуцировала прогрессивное повреждение мышечных волокон у мышей MDX (рис. 4, открытый круг и черную линию, "MDX"), в соответствии с предыдущими докладами о механической слабости мышечных волокон у субъектов с мышечной дистрофией [39]. Через 6 часов после тетанической стимуляции, 67,67 ± 6,57 (± Количество SE) мышечных волокон были повреждены из всей области наблюдения. Общее количество локусов была от 350 до 400 (от 70 до 80 миофибрилл сканирования 5 раз).
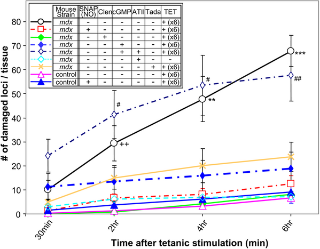
Мы оценили, может ли изменение функциональной ишемии ослаблять это сокращением индуцированное повреждение мышечных волокон. Как показано на рисунке 1b, доноры NO, SNAP могут улучшить кровоток в мышцах MDX мышей. Когда SNAP была локально применена у MDX мышей во время мышечной смерти, гибель клеток была полностью отменена (рис. 4, открытые площади и красные пунктирные линии ", MDX + NO »). Микроскопические изображения этих экспериментов приведены на рисунке S5a (с поддержкой информации).Эти наблюдения из оснастки экспериментов подтверждают гипотезу о том, что функциональные ишемия необходима и играет главную роль в сокращении повреждений мышечных волокон у MDX мышей и может быть предотвращена путем увеличения NO. Для дальнейшего исследования этого цитопротекторного эффекта цГМФ - зависимого пути, эффект 8 - CPT цГМФ был рассмотрен в том же эксперименте гибели клеток, поскольку данный препарат повышает потока эритрацитов у мышей MDX (рис. 1b). Сокращение индуцированного работой
![]()
повреждения мышечных волокон было успешно предотвращено (рис. 4). Защитный эффект 8 - CPT цГМФ вероятно, опосредован его вазорегуляторным потенциалом. Тормозящее действие ATII на цГМФ - опосредованную цитопротекцию, скорее всего, через сосудистую регуляцию, но не его прямые катаболические функции на мышечные волокна, потому ATII сами по себе не имеют цитотоксического действия на мышечные волокна (рис. 4 ) . Когда ?2 - адренергический агонист, кленбутерол, был локально введен вместо этого, до и во время стимуляции, индуцированное сокращением повреждение ослабляется (рис. 4), хотя ?2 - агонисты, как известно, имеют различные механизмы сосудорасширяющего действия от NO / EDHF [32]. Предыдущие исследования сообщали о повышенной активности PDE5 в скелетных мышцах образцов у мышей MDX [40] и снижение цГМФ производства [10], мы предположили, что введение ингибитора PDE5 увеличит количество цГМФ, и, следовательно, предотвратить повреждение мышечных волокон, как предсказано на основе данных с 8 - CPTcGMP. Тадалафил (4 мг / kgBW ) вводили MDX мышам через желудочный зонд за 60 минут до начала тетанической стимуляции. Лечение тадалафилом снизило объем повреждений мышечных волокон (рис. 4). Плацебо не помешало повреждению мышечных волокон (данные не показаны). Функциональной ишемии достаточно, чтобы вызвать индуцированное сокращением повреждения мышечных волокон. Эксперименты были разработаны, чтобы оценить, насколько на скелетных мышечных клетках, подобных наблюдаемым у мышей MDX, можно имитировать искусственную функциональную ишемиею у животных дикого типа. Только тогда, когда введены L-NAME (ингибирование NO производства), плюс апамин карибдотоксин (ингибирование EDHF ) и сосудистый спазм, учитывая одновременно двенадцатикратное повторение тетанических стимулов производят 56,2 ± 13,69 (число ± SE) поврежденых локусов мышечных волокон через 6 часов после стимуляции (на рисунке 5). Сопоставимые повреждения мышечных волокон не наблюдались в отсутствие одного из следующих реактивов / вмешательства : L-NAME (рис. 5), апамин плюс карибдотоксин, сосудистые угнетение или тетаническую стимуляцию. Тетаническая стимуляция и угнетение сосудистого тонуса сами по себе не вызывает повреждения мышечных волокон. Повторение шести тетанических стимулов вызывает меньшее количество повреждений мышечных волокон через 6 часов. Подробные микроскопические изображения каждой группы представлены в S5b. Наши фармакологические вмешательства не возвращали аномальную фрагментированную морфологию NMJs у мышей MDX (рис. S5a, красное окрашивание) к нормальной форме (см. рис S5b ) , или наоборот, у контрольных мышей, в течение 6 часов наблюдения.
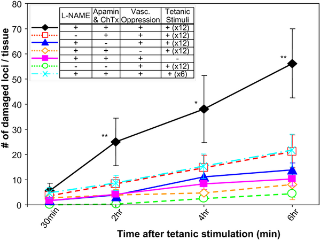
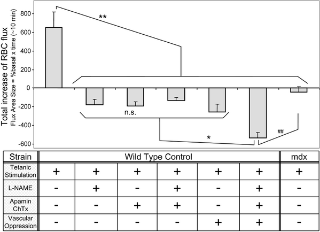
Количество функциональной ишемии достигнутое путем различных обработок было количественно измерено путем интеграции общего изменения потока эритроцитов в течение 10 минут после тетанической стимуляции (расчеты показаны во вспомогательной информации, рисунок S6), и того чтобы оценить функциональную ишемию было достаточно. Функциональная ишемия определяется как патологическое состояние, когда есть отсутствие нормальной реакции кровотока в пост-сокращении мышц: в нашем эксперименте MDX мыши не показывают увеличение потока в ответ на тетаническую стимуляцию (рис. 6). Лечение контрольных мышей L-NAME, апамин плюс карибдотоксином, или сосудистое угнетение индивидуальная функциональная ишемия в одинаковой степени наблюдается у MDX мышей, но вызывало большее снижение потока, когда все они были объединены (рис. 6). В некоторых случаях сочетание лечения вызвало значительное падение потока, например патологическое состояние, которое вписывается в определение "тяжелой ишемии", а не функциональной ишемии. Теоретически, полная обструкция артериол под наблюдением приведет к отрицательным значениям. В наших экспериментах мы наблюдали ишемию с отрицательными значениями (рис. 6, все комбинации препаратов, 2-я колонка справа) и по-прежнему поддерживали определенный уровень кровотока. Эти эксперименты показывают, что функциональная ишемия сама по себе не достаточна, чтобы вызвать повреждения мышечных
![]()
волокон.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




