Московский ордена Ленина, ордена Октябрьской Революции и ордена Трудового Красного Знамени Государственный Университет
имени
Химический факультет
Кафедра химии природных соединений
Лаборатория им.
Курсовая работа:
Поиск новых антибиотиков, замедляющих трансляцию, в культуральных жидкостях почвенных микроорганизмов.
Научный руководитель:
к. х.н.
Москва ? 2015
Оглавление:
Введение……………………………………………………………3 Терминология……………………………………………….4 Литературный обзор……………………………………………….6 Репортёрная система CER/RFP…………………………….8 Экспериментальная часть………………………………………..10 Результаты………………………………………………………...12 Выводы…………………………………………………………….13 Список литературы……………………………………………….141.Введение
В последнее время по всему миру регистрируются случаи значительной устойчивости возбудителей различных заболеваний к антибиотикам. Антимикробная резистентность является естественным биологическим ответом на частое, повсеместное использование антибиотиков, которое способствует отбору, выживанию и размножению устойчивых штаммов микроорганизмов. Резистентность, в свою очередь, значительно повышает выживаемость данного вида, способствует его размножению. Появление резистентных патогенов является причиной все большего беспокойства, так как глобальная смертность от лекарственно устойчивых бактериальных инфекций продолжает увеличиваться ежегодно. Например, только в Соединённых Штатах Америки каждый год умирает свыше 23.000 человек непосредственно от подобных инфекций, а около 14.000 ? от полученных осложнений. Ещё 2 миллиона человек получают тяжёлые осложнения. По некоторым данным, смертность достигает отметки в 100.000 граждан [1].
В таких условиях поиск новых антибиотиков и экспрессное определение механизма их действия крайне актуальны. Около половины антибиотиков, применяемых в настоящее время, действуют на рибосому [2] и являются очень перспективными, так как от трансляции напрямую зависит жизнедеятельность бактерии. Механизмы действия могу быть различными: некоторые антибиотики вызывают ошибки в ходе синтеза белка, другие замедляют скорость трансляции всех белков или их части или блокируют рибосому на различных стадиях её функционального цикла. Таким образом, диапазон возможных антибактериальных средств, влияющих на трансляцию довольно широк.
Целью нашей работы являлся поиск новых потенциальных антибиотиков, взаимодействующих с рибосомой, с помощью дикого штамма Escherichia coli.
Терминология:
Секвенирование ? определение последовательности нуклеотидов в гене.
Геномика ? наука, изучающая все гены и их роль в структуре организма, как в нормальном состоянии, так и при заболевании
Трансляция белка ? синтез полипептидных цепей белков по матрице мРНК согласно генетическому коду.
Ингибиторы ? вещества, подавляющие каталитическую активность отдельных ферментов или ферментных систем.
In vitro (лат.) ? в пробирке; в лабораторных условиях.
In vivo (лат.) ? в естественных условиях; на живом организме.
Сублетальная концентрация ? концентрация антибиотика, когда с бактерией уже произошли существенные изменения, но она всё ещё жива.
Плазмида ? кольцевая ДНК, способная стабильно существовать в клетке в автономном, не связанном с хромосомами, состоянии.
Экспрессия ? перенос генетической информации от ДНК через мРНК к полипептидам и белкам.
Репортёрная система ? система генов, вводимая в клетку для исследования их проявлений в культурах клеток.
Агар ? агар-агар, полисахаридный препарат, получаемый из некоторых красных морских водорослей. Состоит из агарозы. Один из лучших природных гелеобразователей. Используется в качестве одного из компонентов питательной среды.
Библиотека (банк) генов ? представляет собой совокупность культур микроорганизмов (бактерий, дрожжей), в каждую клетку которых введён вектор, несущий один из фрагментов генома организма.
Скрининг ? поиск нужного гена в библиотеке генов.
Оперон ? участок генетического материала, транскрипция которого осуществляется на одну молекулу мРНК под контролем белка-репрессора.
Кодон ? участок мРНК, состоящий из трёх остатков нуклеотидов. Кодирует один аминокислотный остаток или служит сигналом для завершения или начала белкового синтеза.
Триптофан, аланин ? незаменимые аминокислоты.
Механизм аттенюации ? Механизм регуляции транскрипции генов, известный у ряда бактерий; является следствием преждевременной терминации синтеза мРНК в определённом участке гена – аттенюаторе.
Терминация ? остановка синтеза полипептидной цепи при достижении терминирующего кодона в мРНК; также завершение синтеза РНК в процессе транскрипции или ДНК в процессе репликации.
Аминоацилирование ? Вторая реакция процесса активации аминокислот, в результате которой происходит замещение АМФ в аминоациладенилате молекулой тРНК с образованием аминоацил-тРНК
Аликвота — небольшое количество вещества в растворе точно известного объёма.
2.Литературный обзор
В 1928 году Александр Флеминг открыл антибактериальные свойства пенициллиновых плесневых грибов. Они оказывали своё действие только на грамм-положительные штаммы бактерий, однако, в отличие от аналогичных химических антисептиков, не уничтожал человеческие лейкоциты и даже в неочищенном и сильно разбавленном состоянии отличался большей эффективностью. Изначально пенициллин предполагалось использовать только местно и наружно. Попыткой очистить и выделить пенициллин занимались Чейн и Флори в Оксфорде в 1940 году, а уже в 1944 было налажено массовое производство антибиотика.
Может возникнуть вопрос: зачем нужны новые антибиотики, если лекарство изобретено свыше 70 лет назад? Всё дело в таком явлении, как резистентность, ? ставшая наследственной устойчивость к вредным для бактерии веществам. Повсеместное использование антибиотиков (даже там, где эта мера является излишней или попросту бесполезной (например, от головной боли, вызванной сменой давления)) привело к тому, что новые лекарственные препараты устаревают в течение нескольких лет.
Изначально поиск новых антибиотиков ограничивался общеклеточным скринингом. Он по-прежнему используется для скрининга больших библиотек соединений, однако более чем за последние 40 лет этим способом не выделено ни одного важного образца [3][4]. Явление резистентности снижает до нуля действенность известных ранее антибиотиков, поэтому для поддержания их эффективности необходимо модернизировать химическую структуру действующего вещества. Однако это лишь временное решение проблемы. Дело в том, что устойчивость к исходной молекуле действующего вещества является также неплохой защитой и от её модификаций.
В последние годы в поиске антибактериальных препаратов используется стратегия идентификации мишеней, важных для роста и выживания бактерий. Анализ бактериальной биологии и метаболизма, а также сиквенс большого количества генов способствовали определению новых мишеней. В этом методе выбираются индивидуальные белки, важные для жизнедеятельности клетки, а затем подбираются ингибиторы данных белков в высокопропускном формате. Таким образом, можно нанести точечный смертельный удар со скоростью, которая не позволит бактерии вывести антибиотик или быстро приспособиться к нему всей популяции. Развитие таких методов сильно возросло с осуществлением сиквенса бактериального генома.
Секвенирование геномов более 200 различных организмов, включая большое количество важных патогенов для медицины, способствовало формированию убеждения, что новые мишени для антибиотиков распространены в клетке повсюду. В попытках найти «идеальную» цель, например, её наличие в исследуемом организме в достаточном количестве или её доступностью для атаки, исследователи разработали множество приёмов для извлечения нужной генетической информации из клетки. Так, например, были найдены участки нуклеотидной цепи, которые присутствуют во всех бактериальных геномах и играют важную роль в росте и выживании клеток. Такие подходы привели к открытию ингибиторов жизненно важных для клетки веществ. Хотя бактериальная геномика и связанные с ней технологии считались основой для новой эры в исследовании антибиотиков, до сих пор нет антибактериальных агентов, подвергшихся клиническим испытаниям, которые возникли бы исключительно из подходов геномики [5]. Впрочем, она всё ещё имеет высокий потенциал, так как существует ещё множество других ненайденных и неисследованных антибактериальных целей и механизмов действия, требующих открытия.
Может показаться, что все антибиотики действуют по простому механизму, включающему отдельные цели. Однако это не так, по крайней мере, для бактерицидных антибиотиков. Скорее всего, механизмы действия антибиотиков являются результатом воздействия на множество целей, что и приводит к бактериальному ингибированию. Это могут быть цели, приводящие напрямую к ингибированию бактериального роста или же способствующие общему ингибирующему действию косвенно. Именно геномные методы пролили свет на сложность действия антибактериальных препаратов и на причины, которые препятствуют открытию новых лекарств.
Как уже было сказано выше, около половины применяемых в настоящее время антибиотиков действуют на рибосому. Механизмы действия могу быть различными: некоторые антибиотики вызывают ошибки в ходе синтеза белка, другие замедляют скорость трансляции или блокируют рибосому на различных стадиях её функционального цикла. Без определения механизма действия невозможно создание лекарственного препарата. Также, это важно для понимания фундаментальных основ взаимодействия антибиотиков с рибосомой. Стандартный способ проверки антибактериальной активности ? это измерение уровня ингибирования клеточного роста, но данный подход имеет несколько недостатков: во-первых, необходимы большие концентрации антибиотика, чтобы увидеть заметное снижение роста, а, во-вторых, при таком способе скрининга невозможно определить механизм действия антибиотика. Методы для определения механизма существуют, но большинство из них требует in vitro экспериментов и выделения потенциальных мишеней антибиотиков из клетки, что делает их малоподходящими для широкомасштабного поиска. Поэтому создание высокопроизводительно метода скрининга механизма действия антибиотиков, позволяющего проводить поиск in vivo, является крайне актуальным. [2]
Репортёрная система CER/RFP
В Московском Государственном Университете имени была разработана система детектирования сублетальных концентраций антибиотиков, вызывающих торможение рибосомы [6].
Готовая плазмида обладает следующими характеристиками:
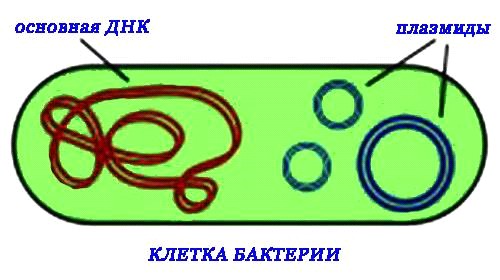
• содержит ген устойчивости к ампициллину (Ампициллин был выбран, так как он не затрагивает работу рибосомы.);
• использует в качестве флуоресцентных белков следующие: Red Fluorescence protein (RFP) (красный флуоресцентный белок) и Cerulean (CER) (зелёный флуоресцентный белок). (Среди всех флуоресцентных белков эти два были выбраны так, чтобы их спектры поглощения и испускания практически не перекрывались между собой, и таким образом уровни их экспрессии можно было бы детектировать независимо.)
В двойной репортёрной системе CER/RFP экспрессия CER была поставлена в зависимость от скорости трансляции, в то время как RFP продолжал выполнять функции внутреннего контроля. Использование флюоресценции в качестве сигнала позволяет проводить все исследования в живых клетках без их разрушения: в жидкой среде или на чашках с агаром, что значительно облегчает и ускоряет процесс скрининга больших библиотек потенциальных антибиотиков.
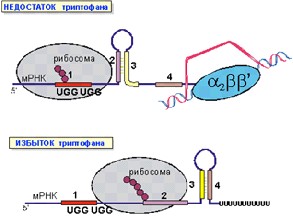
Регуляция экспрессии гена, основанная на скорости трансляции, встречается и в природе, классический пример – триптофановый оперон E. coli, регулируемый по механизму аттенюации. В начале оперона trpLEDCBA закодирован короткий пептид trpL, содержащий два идущих подряд кодона триптофана. Если в клетке избыток триптофана, то рибосома быстро транслирует этот участок и идёт дальше, что приводит к образованию вторичной структуры, стимулирующей преждевременную терминацию транскрипции, в результате чего оперон не экспрессируется. (Рис.1)
Рис.1. Схема регуляции триптофаного оперона, образование шпильки 3-4 приводит к терминации транскрипции, альтернативная шпилька 2-3 не мешает РНК-полимеразе.
При недостатке триптофана рибосома надолго останавливается на этих двух кодонах из-за отсутствия соответствующих аминоацилированных тРНК, и образуется альтернативная вторичная структура, которая не мешает РНК-полимеразе продолжить транскрипцию оперона. В результате образуются белки, необходимые для биосинтеза триптофана.
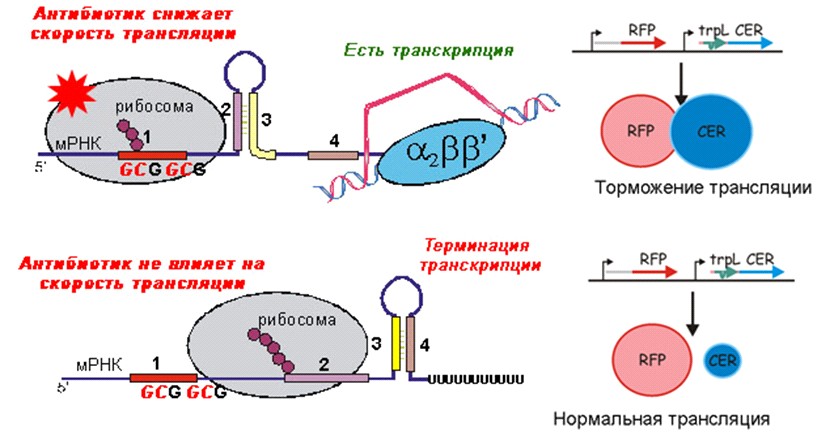
В данной конструкции последовательность лидерного пептида trpL помещена началом гена CER, два триптофановых кодона заменены на два аланиновых, которые рибосома всегда транслирует быстро. При обычных условиях это приводит к ингибированию экспрессии CER. В присутствии же антибиотика, замедляющего трансляцию (в сублетальной концентрации), рибосома будет все равно медленно транслировать участок с двумя аланиновыми кодонами, что приведёт к сворачиванию альтернативной вторичной структуры и увеличению экспрессии CER. (Рис.2)
Этот метод не даёт ложноположительных результатов.
Рис.2. Схема работы репортёра, детектирующего присутствие веществ, замедляющих трансляцию.
Данная плазмида трансформировалась в штамм E. coli, содержащий нокаут гена белка TolC. Белок TolC отвечает за экспорт различных метаболитов из клетки, в том числе он экспортирует и антибиотики. Использование штамма ?tolC позволило снизить минимальную ингибирующую концентрацию и определить механизм антибиотиков, которые не действуют на обычный штамм E. coli дикого типа. Штамм E. coli, несущий ?tolC аллель, может служить своеобразной моделью грамположительной бактерии благодаря тому, что обладает повышенной чувствительностью к некоторым антибиотикам.

3.Экспериментальная часть
Аппаратура:
Ламинар, термостат «Гном», набор пипетманов переменного объёма (Eppendorf), ультрафиолетовая лампа (254 нм), детектор люминесценции Victor X.
Реагенты:

Ампициллин; эритромицин (Sigma); агар (Helicon); LB (Amresco) (1% пептон; дрожжевой экстракт 0,5%, NaCl 1%), дистиллированная вода.
Манипуляции с клетками:
Трансформация компетентных клеток E. coli.

Пробирку с компетентными клетками размораживали во льду, добавляли 1–5 мкл раствора плазмидной ДНК (~ 0,01 мкг) в буферном растворе EB (Qiagen) или в дистиллированной воде, инкубировали 30 мин при 0ОС. Затем прогревали смесь в течение 40–50 секунд при 42ОС, охлаждали до 0ОС, добавляли 800 мкл среды LB и инкубировали 1 час при 37ОС. Аликвоту 100–200 мкл (в случае плазмидной ДНК) трансформационной смеси высевали на чашку Петри с твёрдой средой LB, содержавшей ампициллин. Инкубировали чашку при 37ОС в течение 16 ч.

Приготовление ночной культуры.
Добавляли одну колонию с чашки с трансформированными клетками в 2 мл среды LB с ампициллином. Ставили в термостат на 16 часов.

Использование двойной репортёрной системы для анализа механизма действия антибиотиков на чашках с агаром.
Ночную культуру штамма дикого типа BW25113 или ?tolC, трансформированных плазмидами pRFPCER-TrpL2A, разбавляли в два раза свежей средой LB и выливали на чашки с агаром, средой LB и ампициллином (50 мкг/мл). Затем на поверхность высохших чашек делали углубления диаметром 5 мм, потом наносили образцы (50 мкл экстрактов, ery эритромицин ? 50 мкл раствора 0,1 мг/мл, lev левофлаксацин 50 мкл 0.1 мкг/мл). После культивирования в течение ночи при 37ОС полученные чашки документировались при помощи цифровой камеры при освещении их ультрафиолетом (254 нм).
In vitro трансляция.
Для in vitro трансляции использовали мРНК люцеферазы сверчка, S30 экстракт E. coli, реакцию осуществляли по описанной методике [7]. Активность синтезированной люцеферазы определяли через 10 минут. Концентрации антибиотиков указаны в разделе «Результаты».
4.Результаты
In vivo анализ образцов.
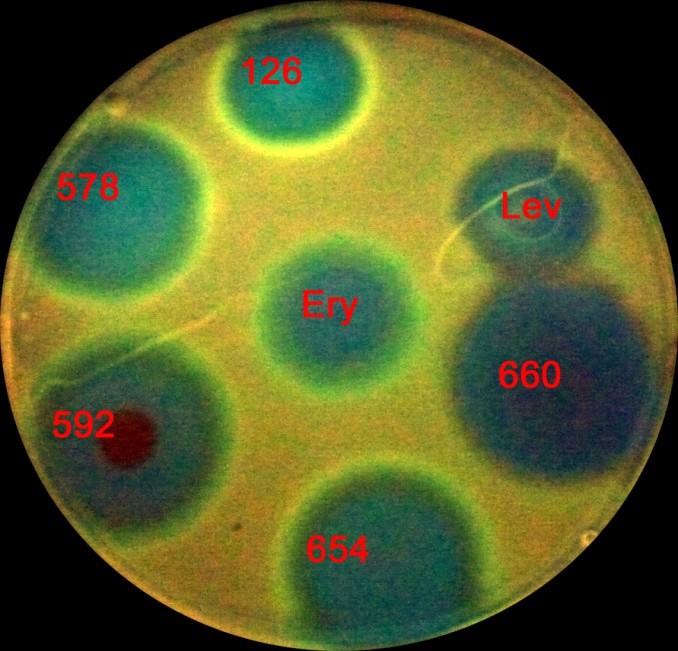
В ходе работы было протестировано пять экстрактов из культуральных жидкостей почвенных микроорганизмов. В результате скрининга с использованием двойной репортёрной конструкции RFP/GFP была детектирована антибактериальная активность, замедляющая трансляцию, у ряда образцов (рис 3).
Рис.3. Тестирование влияния антибиотиков на экспрессию CER в клетках дикого типа, трансформированных плазмидами: pRFPCER-TrpL2A, на чашках с агаром. Обозначения антибиотиков: эритромицин (Ery), левофлаксацин (Lev), номера тестируемых образцов.
In vitro анализ образцов.
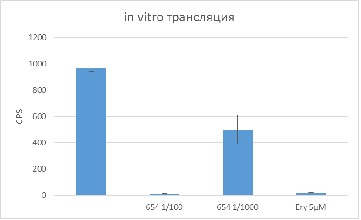
Для одного из образцов (654) ингибирование синтеза белка подтверждено при помощи in vitro трансляции (Рис.4). Эффективность действия данного образца сопоставима с хорошо известным ингибитором трансляции эритромицином. В дальнейшем необходимо разделить смесь 654, чтобы обнаружить индивидуальное вещество, обладающее антибактериальной активностью.
Рис.4. In vitro ингибирование трансляции мРНК люцеферазы, выраженное во вспышках в секунду (CPS) в присутствии эритромицина и экстракта 654.
5.Вывод
- С использованием высокопроизводительного метода определения механизма действия антибиотиков была детектирована антибактериальная активность, замедляющая трансляцию, культуральной жидкости у образцов 126, 578, 592 и 654. Для образца 654 получено подтверждение ингибирования трансляции в системе in vitro.
6.Список литературы
Boucher H. W., Talbot G. H., Bradley J. S. et al. Bad bugs, no drugs: no ESKAPE! // Clin. Infect. Dis. 2009. V. 48. P. 1–12. Новая система для широкомасштабного анализа сайтов инициации и реинициации трансляции Escherichia coli. Дис….канд. хим. наук. Москва: МГУ им. , 2012.110 с. Overbye K. M., Barrett J. F. Today Antibiotics: where did we go wrong? // Drug Discov. 2005. V. 10. P. 45–52. Bax R. P., Anderson R., Crew J. et al. Antibiotic resistance–what can we do? // Nat. Med. 1998. V. 4. P. 545–546. Coates A.,Yanmin H., Bax R. et al. The future challenges facing the development of new antimicrobial drugs // Nat. Rev. Drug Discov. 2002. V. 1. P. 895–910. Osterman I. A., Prokhorova I. V., Sysoev V. O., Boykova YV, Efremenkova O. V., Svetlov M. S., Kolb V. A., Bogdanov A. A., Sergiev P. V., and Dontsova O. A. Attenuation-based dual-fluorescent-protein reporter for screening translation inhibitors. // Antimicrob Agents Chemother. 2012 56, №4, p. 1774-83. Svetlov, M. S., A. Kommer, V. A. Kolb, and A. S. Spirin, Effective cotranslational folding of firefly luciferase without chaperones of the Hsp70 family. Protein Sci, 2006. 15(2): p. 242-7.


