![]()
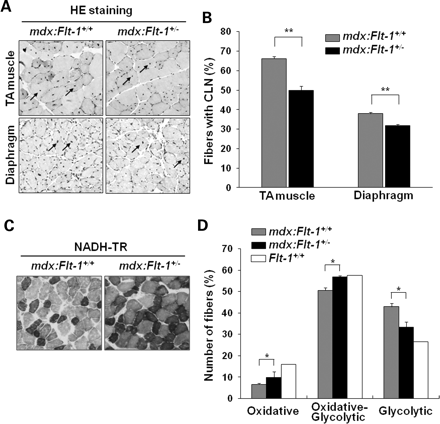
Изменения типа мышечных волокон и развитие гипертрофии были зарегистрированы в MDX мышцах в качестве компенсации за счет потери генерирующих силу мощностей существующих мышц. Для определения окислительного профиля мышц срезы окрашивали НАДH - тетразолия редуктазой (TR) . MDX: Flt1 + / - мыши ( окислительный : 9,8 ± 2,6 , окислительно - гликолитических : 56,9 ± 0,4 , гликолитических : 33,2 ± 2,5 ) показали увеличение количества окислительных и окислительно - гликолитических волокон и уменьшение гликолитических волокон по сравнению с контролем MDX : Flt1 + / + мышей ( окислительный : 6,58 ± 0,5 , окислительно - гликолитических : 50,5 ± 1,3 , гликолитический : 42,8 ± 1,7 ) (рис. 5С и D) . Иммуноокрашивание с использованием антител против изоформ тяжелой цепи миозина ( МНС ) ( 28,29 ) выявило увеличение окислительного типа мышечных волокон ( MDX : Flt1 + / -: 1,74 ± 0,4 , MDX : Flt1 + / + : 0,6 ± 0,2 ) (Дополнительный материал, рис. S1A и B). Мы также обнаружили, что среднее распределение волокон по размерам диаметра MDX: Flt1 + / - мышей перекошено в сторону меньшего размера волокон ( Дополнительный материал, рис S1C и D ). Это уменьшение размера может быть связано с переключением типа волокна от гликолитических на окислительный тип.
MDX : Flt1 + / - мыши обнаруживают повышенное кровоснабжение.
Чтобы оценить, насколько произошло увеличение плотности сосудов, увеличение перфузии в скелетных мышцах, мы измерили поток лазерной доплерографией ( LDF ) в ПБ мышце. Среднее количество единиц перфузии (ПУ) в соответствии с рекомендациями производителя (рис. 6а) . Flt - 1 + / - ( 54,8 ± 1,2 ) и MDX: Flt - 1 + / - ( 62,6 ± 4,7 ) показало увеличение потока эритроцитов (RBC) по сравнению с диким типом Flt - 1 + / + ( 46,1 ± 1.1) и MDX: Flt - 1 + / + ( 48,1 ± 3,3 ), соответственно. Это согласуется с увеличением плотности кровеносных сосудов в ПБ мышце и может компенсировать функциональный ишемический фенотип, наблюдаемый у MDX мышей.
![]()
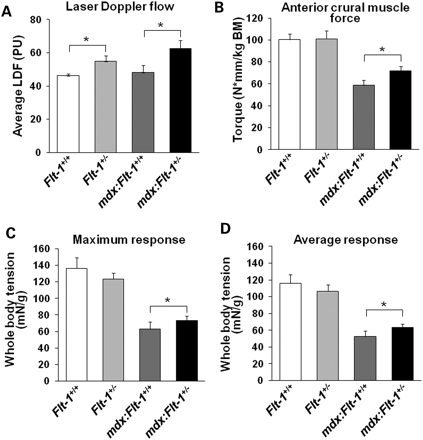
MDX : Fit - 1 + / - мыши обнаруживают улучшенную сократительную функцию мышц.
Чтобы изучить вопрос гистологического улучшения переведенного в функциональное улучшение, измерялась производство силы в задней конечности. Максимальный изометрический момент измеряли путем количественного определения крутящего момента, когда малоберцовый нерв стимулировался для вызова сокращения передней мышцы голени. Максимальная мощность была нормирована на массу тела мыши. Хотя не было никакого существенного различия между Fit - 1 + / - ( 101,0 ± 7,2 ) и диким типом Fit - 1 + / + мышей ( 100,3 ± 4,9 ), MDX : Fit - 1 + / - мыши (71,7 ± 4.3) генерируют больший крутящий момент по сравнению с контрольными MDX: Flt - 1 + / + мышами (58,5 ± 4,7 ) (фиг.6В ). Чтобы оценить системное производство силы, проводили анализ напряжения всего тела у дикого типа Flt - 1 + / +, Flt - 1 + / - , MDX: Flt - 1 + / + и MDX: Flt - 1 + / - мышей. MDX : Fit - 1 + / - мыши показали улучшение максимальной силы тяги и среднего тягового усилия (максимум : 73.49 ± 4,85 и среднего : 63.47 ± 4,00 ) по сравнению с контрольными MDX: Fit - 1 + / + мышами ( максимальной : 62.83 ± 8.88 и средний: 52.52 ± 6.74 ) (рис. 6С и D) . Однако это улучшение было только скромным по сравнению с силой, создаваемой диким типом Flt - 1 + / + мышей.
Оценка MDX: utrn - / - : Fit - 1 + / - тройных мутантных мышей.
Хотя MDX мыши, генетически схожи с МДД, но они не проявляют патологию с тяжестью МДД. Кроме того, MDX мышей не показывают существенной разницы в их жизни по сравнению с мышами дикого типа. Одна из причин относительно мягкого фенотипа MDX мышей является регуляция атрофина, который может компенсировать недостающие функции дистрофина. MDX мыши, несущие мутации гена атрофина ( utrn - / -) отображают более тяжелый фенотип, чем у MDX мышей ( 23,30 ) . Эти мыши обнаруживают заметный кифоз и обычно умирают в течение 5 месяцев. Таким образом, они служат в качестве лучшей животной модели для МДД. Так как мы не обнаружили различий в размере атрофина между MDX: Fit - 1 + / - и MDX : Fit - 1 + / + мышей с помощью вестерн-блоттинга (рис. 3C и Е ) , мы приступили к созданию тройного мутанта MDX: utrn - / - : Fit - 1 + / - и контроля MDX : utrn - / - : Fit - 1 + / +. MDX: utrn - / -: Flt - 1 + / - мыши были жизнеспособными, и потомство имело ожидаемое менделевское соотношение (данные не показаны ). Потеря дистрофина и атрофина приводит к очень тяжелому мышечному фенотипу с очень высоким содержанием соединительной ткани. Однако гистологические оценки ПБ мышцы показало уменьшение количества CLN у MDX: utrn - / -: Flt - 1 + / - мышей ( 73,28 ± 1,94 ) по сравнению с контрольными MDX: utrn - / -: Flt - 1 + / + ( 85.09 ± 1.99 )-животными (рис. 7 , б). MDX: utrn - / -: Flt - 1 + / - мыши также продемонстрировали значительное увеличение массы тела по сравнению с контрольной MDX: utrn - / -: Flt - 1 + / + мышей ( фиг. 7С) .
![]()
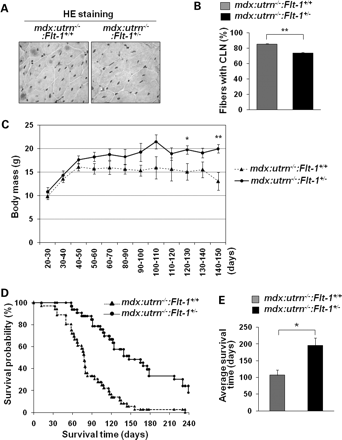
Важно отметить, что средняя продолжительность жизни MDX: utrn - / - : Fit - 1 + / - мышей была значительно увеличена ( 177,88 дней ± 17,60 ) по сравнению с контрольными MDX: utrn - / - : Fit - 1 + / + мышами ( 91,76 дней ± 10,22 ) (рис. 7D и Е). Оба генотипа стабильны в течение всего 30-50 дней, после чего MDX : utrn -/ - : Fit - 1 + / + мыши показывают резкое снижение жизнеспособности по сравнению с более постепенной летальностью MDX: utrn - / - : FLT - 1 + / - мышей. Тестом на выживание Каплана-Мейера показал значительную разницу между двумя генотипами ( рис. 7D). Эти данные убедительно свидетельствуют, что Fit - 1 + / - фон ослабляет фенотип мышечной дистрофии MDX: utrn - / - дважды мутантных мышей, чтобы продлить их срок жизни, возможно, за счет увеличения плотности сосудов. Взятые вместе, эти данные показывают, что сразвитие увеличения ангиогенеза и сосудистой плотности может частично улучшить дистрофический фенотип вумодельных мышей с МДД.
Не было изменений в воспалительной реакции у MDX: Fit - 1 + / - мышей.
Воспаление, как известно, способствует мышечному заживлению и регенерации. Кроме того, сообщается, что Flt - 1 также экспрессируется в макрофагах (31). Таким образом, мы сравнили степень воспаления в ПБ мышце, выделенной из MDX: Fit - 1 + / - мыши и контрольных MDX : Fit - 1 + / + мышей. Иммуноокрашивание для Mac -1 ( маркером моноцитов и макрофагов ) и GR-1 (маркера для моноцитов и гранулоцитов ) показало, что не было никакого существенного различия в количестве клеток воспаления, которые наблюдались в ПБ мышцах между MDX: Fit - 1 + / - мышами и контролем MDX: Fit - 1 + / + (Дополнительный материал, рис S2 . ). Спутниковые клетки являются негативными для VEGF рецепторов Flt - 1 и Flk - 1. Несколько сообщений рассказывают, что распространение спутниковых клеток и миграцию клеток под влиянием VEGF, возможно, через его рецепторы, Flk - 1 и Flt - 1 (15). Для выяснения того, что сателлитные клетки могут экспрессировать FLT-1 и FLK - 1 и изучить любые потенциальные клеточные автономные эффекты, мы сначала характеризуем экспрессию LacZ в мышцах Fit - 1 + / - ( Fit - 1- LacZ ) (14) , Flk -1- LacZ (32) и Myf5 + / nLacZ мышей (33,34) . Эта экспрессия LacZ резюмирует эндогенную экспрессию FLT - 1 , Flk - 1 и Myf5. Очевидно, что LacZ - позитивные клетки были обнаружены вокруг сосудов, расположеных за пределами ламинин-положительной базальной пластинки мышечных волокон у Flt -1- LacZ и мышей Flk -1- LacZ ( Дополнительный материал, рис. S3A ) . В противоположность этому, LacZ - позитивные клетки-сателлиты были обнаружены в ламинин - положительной базальной пластинке мышечных волокон у мышей Myf5 + / nLacZ, указывая, что покоящиеся клетки-сателлиты и мышечные волокна не экспрессируют FLT-1 или Flk - 1 (Дополнительный материал, рис. S3A ) . Далее, мы выделили мышечные волокна и от FLT-1 - LacZ и от Flk -1- LacZ мышей наряду с контролем Myf5 + / nLacZ ( Дополнительный материал, рис. S3B ). Как и ожидалось, спутниковые клетки начали
![]()
пролиферировать на 2-й день и на 5 день ( 35 ). Тем не менее, ни одна из культур от FLT-1 - LacZ или мышей Flk -1- LacZ не окрашивались позитивно на LacZ, указывая, что нет ни спутниковых клеток в покое, ни клеток, экспрессирюющих FLT - 1 или FLK - 1. Кроме того, ни одна из мышечных трубок дифференцированных из миобластов, выделенных из FLT-1 - LacZ и мышей Flk -1- LacZ не окрашивались позитивно на LacZ. В противоположность этому, клетки-сателлиты и полученные спутниковые миобласты имели явно положительный результат при окрашивании на LacZ в культурах мышей Myf5 + / nLacZ. Кроме того, иммунное окрашивание ясно показало, что десмин - позитивные миобласты отрицательны для Flt -1 или FLK - 1 , тогда как человеческие эндотелиальные клетки пупочной вены ( HUVECs ) положительны на наличие обоих рецепторов ( дополнительный материал, рис. S3C ). Таким образом, эти результаты сильно указали, что неклеточные автономные эффекты улучшили фенотип мышц у MDX: Fit - 1 + / - мышей.
Увеличение распространения миогенных клеток-предшественников в повышенной сосудистой нише.
Эксперименты с мышечными волокнами исключили возможность, что гетерозиготные Fit - 1 клетки автономно влияют на происхождение пролиферации миогенных предшественников спутниковых клеток или дифференциацию. Мышцы MDX мышей способны эффективно восстановиться на ранних стадиях в связи с распространением сателлитных клеток в бассейне. Тем не менее, по мере старения мышц, количество спутниковых клеток уменьшается, что приводит к нарушению регенерации мышц (28). Чтобы исследовать, влияет ли количество спутниковых клеток и клеток-предшественников на MDX: Flt - 1 + / - мышей по сравнению с контрольными MDX: Flt - 1 + / + мышами, мы провели анализ FACS диссоциированных клеток из ПБ мышц ( рис. 8, а и б). Интересно, что хотя общее количество SM/C-2.6 + сателлитных клеток и миогенных клеток - предшественников, выделенных из ПБ мышцы Flt - 1 + / - мышей, не показали значительной разницы по сравнению диким типом Flt - 1 + / + мышей, эти клеточные популяции были заметно увеличены у MDX: Flt - 1 + / - мышей по сравнению с контрольными MDX: Flt - 1 + / + мышами. Увеличение числа Pax7 + сателлитных клеток, расположенных под базальной пластинкой ( ламинином +) у MDX: Fit - 1 + / - мышей были также обнаружены в мышечных секциях ПБ мышце ( рис. 8 и D). Таким образом, вполне возможно, что повышение сосудистой ниши может способствовать пролиферации и / или выживанию миогенных клеток предшественников.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |


