
Fit-1 недостаточность улучшает мышечный фенотип дистрофии путем повышения ангиогенеза у MDX мышей
ВВЕДЕНИЕ
Мышечная дистрофия Дюшенна (МДД ) является Х-хромосомным мышечным заболеванием, возникая у одного из 3000 детей, когда ген, который кодирует белок дистрофин, мутирует (1) . Дистрофин стабилизирует мембраны и является частью белкового дистрофин-ассоциированного комплекса который защищает целостность мембраны в ответ на повреждения, вызванные сокращением(2). В дистрофических мышцах, где эта связь нарушается, мышечные волокна развиваются нормально, но могут выйти из строя. Поврежденные мышечные волокна вырождаются, и новые волокна развиваются из сателлитных клеток. Тем не менее, регенерация является неэффективной, так последовательные раунды вырождения приводят к постепенной замене мышцы соединительной тканью. Аномальный кровоток, как ожидается, вызвает повреждение мышц как впервые показал Mendell др.(3). Эта группа показала, что ишемия микрососудов миокарда производит группировку некротических волокон. Недавние исследования показывают, что дистрофин также обнаружен в гладких мышцах сосудов мышей (4,5). Отсутствие дистрофина у MDX мышей (6) , животной модели для МДД, приводит к сосудистым аномалиям, которые могут повлиять на приток крови. Это зависит от системы оксида азота (NO), эндотелий-индуцированной дилатации, экспрессии эндотелиальной NO - синтазы и нейронной NO - синтазы, а также пониженной плотности сосудов (7,8 ) . Кроме того, также сообщалось, что атрофин, гомолог дистрофина, экспрессируется в эндотелии (9). Кроме того, нарушение функций комплекса саркогликана, который связан с дистрофином в гладких мышцах сосудов, нарушает функцию сосудов. Это вызывает кардиомиопатию и обостряет мышечную дистрофию (10). Таким образом, регулирование притока крови может быть нарушено при МДД, возможно увеличение повреждения мышц. Последние работы элегантно демонстрирует важность экспрессии дистрофина в гладких мышцах сосудов для функции мышц MDX мышей. Ито и др.(5) генерировали SMTG / MDX мышей, которые показали восстановление NO - зависимой модуляции б - адренорецепторов и частично улучшенный фенотип мышц. Взятые вместе, эти доклады свидетельствуют о том, что нарушение сосудистой функции, связанное с мышечной патологией при МДД. Таким образом, МДД характеризуется повышенным повреждением мышц и ненормальным кровотоком после сокращения мышц. Это называется состоянием функциональной ишемии. Гипотеза предлагает патогенные дефекты в дистрофин-гликопротеиновом комплексе при мышечной дистрофии (11) : первый удар заключается в снижении NO - опосредованной защиты от ишемии в дистрофических мышцах, а второй удар заключается в увеличении клеточной восприимчивости к метаболическому стрессу. Однако взаимосвязь развития между мышечной дистрофией и ангиогенезом до сих пор не обнаружены. Окончательное лечение мышечной дистрофии, вероятно, потребует того, что белковый комплекс дистрофина восстанавливается во всех пострадавших группах мышц, а также улучшает сосудистую функцию мышц. Фактор роста эндотелия сосудов (VEGF) регулирует ангиогенез путем поощрения роста эндотелиальных клеток, их выживания и миграции. VEGF взаимодействует с его рецепторами VEGFR - 1 ( Flt - 1) и VEGFR - 2 ( FLK - 1 ), которые экспрессирюутся в гемангиобластах и эндотелиальных клеточных линий во время стадии развития и регенерации тканей ( 13,14 ). FLT - 1 является типичным рецептором тирозинкиназы, а также область FLT-1 обладает значительно более слабую активность, чем у Flk-1. В дополнение к полнометражным рецепторам, растворимая форма FLT-1 производится с помощью альтернативного сплайсинга. И полная и растворимая форма FLT - 1 обладают сильной аффинностью связывания с VEGF (15). Мыши, лишенные Fit - 1 гена имеют раннюю эмбриональную летальность вследствие чрезмерного роста эндотелиальных клеток и дезорганизации кровеносных сосудов(13-15). В противоположность этому, гетерозиготные Fit - 1 мыши доживали до взрослого возраста и отображали относительно нормальное развитие. Керни и др. . (16) показали, что гетерозиготные и гомозиготные Flt - 1 мыши отображают повышенную дифференцировку эндотелиальных клеток в культурах эмбриональных стволовых клеток. Эти наблюдения предположили, что Flt - 1 является негативным регулятором роста и дифференцировки эндотелия в процессе разработки. Несколько работ показывают, что администрация VEGF способствует ангиогенезу в мышцах после ишемии (17). Кроме того, введение VEGF может способствовать росту миогенных волокон, защитить миогенные клетки от апоптоза и в конечном итоге стимулировать регенерацию мышц (18). У MDX мышей введение VEGF может улучшить гистологию и функции (19) мышц. Тем не менее, остается неясным, влияет ли активируемый ангиогенез на мышечной фенотип дистрофии. Для решения, можно ли компенсировать состояние функциональной ишемии в мышцах MDX мышей по уровню развития увеличения плотности сосудов, мы скрестили MDX мышей с гетерозиготными Fit - 1 мышами ( Fit - 1 + / -). Затем мы сравнили дистрофические фенотипы MDX: Fit - 1 + / - и контрольных MDX: Fit - 1 + / + мышей.
РЕЗУЛЬТАТЫ
Гетерозиготные мыши с отсутствием Flt - 1 показывают увеличение плотности сосудов.
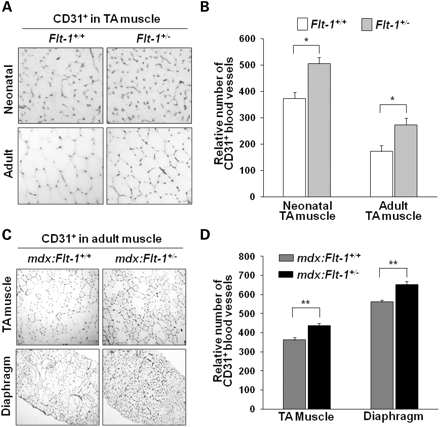
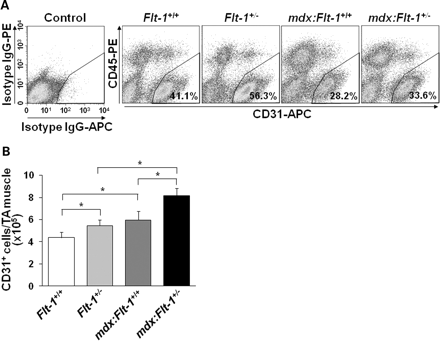
Мыши, лишенные Flt - 1 гена путем вставки гена в - галактозидазы ( Flt -1- / -) в начале имеют высокую эмбриональную летальность из-за чрезмерного роста эндотелиальных клеток и дезорганизации сосудов (13-15 ). Текущая работа показала, что гетерозиготные Fit - 1 + / - мыши не доживали до взрослого возраста и не проявляют очевидного фенотипа. Мы сравнили сосудистую плотность между диким типом ( Fit - 1 + / + ) и гетерозиготными Fit - 1 + / - новорожденными и взрослыми мышами. Fit - 1 + / - новорожденные и взрослые мыши ( 505,5 ± 24,5 и 273,7 ± 14,4 , соответственно) четко показали повышенную сосудистую плотность в передней большеберцовой (ПБ) мышце по сравнению с диким типом ( Fit - 1 + / + ) ( 373,5 ± 23,5 и 172,6 ± 13,3 , соответственно), экспрессирюющих маркер CD31 эндотелиальных клеток в поперечном сечении (фиг. 1A и B). Флуоресцентный анализ (FACS ) также подтвердил увеличенние CD31 + эндотелиальных клеток в ПБ мышце Flt - 1 + / - мышей по сравнению с диким типом Flt - 1 + / + мышей (рис. 2а, б). Эти результаты позволяют предположить, что Fit - 1 + / - мыши обнаруживают повышенный ангиогенез во время послеродового развития мышц. Это наблюдение согласуется с опубликованной работой, что развитие сосудов увеличивается в FLT - 1 + / - культурах эмбриональных стволовых клеток и что Flt - 1 негативно регулирует ангиогенез в процессе развития (16).
![]()
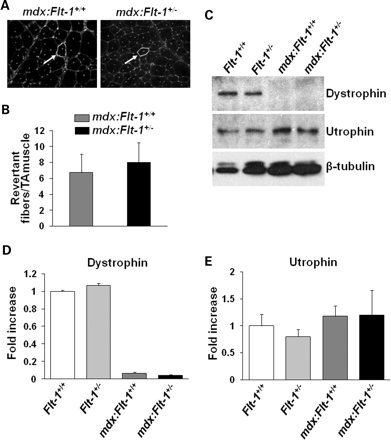
MDX мыши постоянно отображают дегенерацию и регенерацию с последующими отложениями кальция и фиброза в их мышцах (20,21). Важно, чтобы определить, влияет ли ангиогенез на мышечную патологию и функции. Для этой цели мы создали двойных мутантных MDX мышей с гетерозиготным аллелем для Fit - 1 ( MDX: Fit - 1 + / -) и сравнили их с их однопометниками MDX мышей дикого типа с Fit - 1 аллелями ( MDX : Fit - 1 + / + ). Контроль MDX : Fit - 1 + / + мыши имели в среднем 362 ± 12 и 562 ± 12 капилляров в поле зрения для ПБ мышцы и диафрагмы, соответственно. MDX : Fit - 1 + / - мыши имели более высокие средние 438 ± 10 и 653 ± 17 для мышц ПБ и диафрагмы, соответственно (рис. 1C и D). Относительно частое появление дистрофин-положительных ревертантных мышечных волокон наблюдаются у MDX мышей. У MDX - 5CV мышей, используемых в этом исследовании, в ~ 10 раз меньше ревертантов, чем у оригинальных MDX мышей (22). Вестерн-блот анализ и иммуноокрашивание экстрактов и секций ПБ мышцы проводились, чтобы подтвердить, что экспрессия дистрофина и дистрофин-положительных ревертантных волокон не были изменены у MDX: Fit - 1 + / + и MDX: Flt1 + / - мыши (рис. 3А - D) .
![]()
Известно, что в отсутствие дистрофина экспрессия атрофина усиливается для компенсации нестабильности мембраны у MDX мышей (23). Экспрессия атрофина оценивали по вестерн-блоттингу экстракта ПБ мышцы. Как и ожидалось, экспрессия атрофина была активирована в MDX: Flt - 1 + / + и MDX: Flt1 + / - мышах по сравнению с диким типом ( рис. 3C и E) . Таким образом, MDX : Fit - 1 + / - мыши и контроль MDX : Fit - 1 + / + мышей были использованы для дальнейшего сравнения взаимосвязи между мышечной дистрофией и ангиогенезом у MDX мышей.
Морфология и гистология мышц были улучшены у MDX: Fit - 1 + / - мышей.
Поглощение синего красителя Эванса (EBD) используется как мера проницаемости мембраны ( 24,25 ) . MDX : Fit - 1 + / + мыши четко показали некоторые EBD - положительные дегенерирующие мышечные волокна в ПБ мышцах ( 3.30 % ± 1,11 ) и в диафрагме ( 3.02 % ± 0,66 ) (рис. 4 , б). С другой стороны, MDX: Flt - 1 + / - мыши показали более низкие EBD - положительные мышечные волокна в ПБ мышцах( 0,021 % ± 0,05 ) и в диафрагме (1,25% ± 0,25 ). Эти данные убедительно свидетельствуют, что мышечные волокна в MDX: Fit - 1 + / - мыши являются более стабильными и менее дегенеративнвми, чем в контрольной MDX: Fit - 1 + / + мышей.
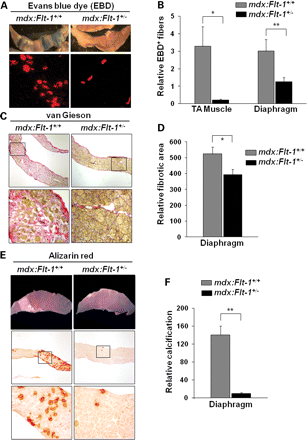
Гистологические фенотипы, обычно связанные с МДД, включают чрезмерный фиброз и кальциноз. Фиброз является заменой мышечных волокон, которая не только уменьшает количество генераторов силы, но и препятствует силе, генерируемой другими мышцами из-за неупругих свойств ( 21,26 ). Диафрагма показала уменьшение фиброза в MDX: Fit - 1 + / - мышей ( 524,8 ± 43,4 ) по сравнению с контрольными MDX: Fit - 1 + / + мышей ( 372,4 ± 34,7 ) ( рис. 4, и D). Кроме того, мембрана в контрольных MDX: Flt - 1 + / + мыши показали большое накопление кальция, которое можно увидеть макроскопически, которое в основном отсутствует у MDX: Flt - 1 + / - мышей ( фиг. 4E и F ). Красное окрашивание Ализарином подтвердило, что MDX: Flt - 1 + / - имели гораздо меньше отложений кальция, которые также обычно меньше по размеру по сравнению с контрольными MDX: Flt - 1 + / + мышами. В противоположность этому, как сообщалось ранее (21), фиброз и кальциноз не так остро проявляются в ПБ мышцах MDX: Flt - 1 + / + мышей ( данные не показаны). Расположеные в центре ядра (CLN ) в мышечных волокнах являются типичным фенотипическим признаком, связаным со многими различными типами мышечных дистрофий (21). MDX : Flt1 + / - мыши отображают 50,00 % ± 1,05 волокон, как имеющие CLN по сравнению с контрольными MDX: + / + мышами Flt1 , которые показали 66,16 % ± 2,06 волокон с CLN (рис. 5а и B). Это значение аналогично тому, что было обнаружено другими в течение MDX мышей (27). Падение CLN у MDX: Flt1 + / - мышей, также рассматривалось в диафрагме по сравнению с контрольными MDX: + / + мышами Flt1 ( 31,97 ± 0,77 против 38,01 ± 0,50 ) . Таким образом, снижение CLN у MDX: Flt1 + / - мышей свидетельствует о понижении дегенерации волокон и повышенной стабильностью мышечных волокон.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |


