Оставшийся на дне пробирки беловатый осадок растворяют в 2-3 каплях воды и добавляют 1 каплю раствора фенолфталеина. Отмечают происходящие изменения.
Опыт № 4. Окисление спирта оксидом меди.
В сухую пробирку помещают 2-3 капли этанола. Спираль из медной проволоки нагревают в пламени спиртовки до появления черного налета оксида меди, раскаленную спираль быстро опускают в пробирку со спиртом. Отмечают происходящие изменения. Повторяют опыт 2-3 раза (пробирку со спиртом оставляют ту же самую). Сравнивают запах исходного спирта и реакционной смеси.
Опыт № 5. Взаимодействие глицерина с гидроксидом меди (II).
В пробирку помещают 1-2 капли раствора сульфата меди (II), 2-3 капли раствора гидроксида натрия и перемешивают. Отмечают происходящие изменения. Добавляют 2-3 капли глицерина и взбалтывают содержимое пробирки. Что наблюдается? Нагревают содержимое пробирки до кипения (но не кипятят). Что наблюдается?
Опыт № 6. Взаимодействие фенола с бромной водой.
В пробирку помещают 2-3 капли бромной воды и добавляют 1-2 капли раствора фенола. Что наблюдается? Изменяется ли окраска и прозрачность раствора?
Опыт № 7. Цветная реакция фенола с хлоридом железа (III).
В пробирку помещают 2 капли раствора фенола в воде, 3 капли воды и добавляют 1 каплю раствора хлорида железа. Содержимое пробирки взбалтывают и отмечают изменение окраски.
Реакции с бромной водой и с хлорным железом являются качественными реакциями для определения фенолов.
Все наблюдения и уравнения реакций записать.
Выполняемая операция | Прибавляемый реактив | Условия опыта | Наблюдения |
Контрольные вопросы
1. Какие вещества называют спиртами?
2. Каковы общие формулы: а) предельных одноатомных спиртов; б) многоатомных спиртов;
в) фенолов?
3. Приведите примеры различных классификаций спиртов.
4. Какие виды изомерии характерны для: а) предельных одноатомных спиртов; б) многоатомных спиртов; в) фенолов?
5. Каков алгоритм составления названий спиртов?
6. Какие виды химических связей есть в спиртах?
7. Каковы причины возникновения водородной связи в спиртах и каково ее влияние на физические свойства спиртов?
8. Каковы химические свойства: а) предельных одноатомных спиртов; б) многоатомных спиртов; в) фенолов?
9. В чем сходство и отличие химических свойств: а) одноатомных и многоатомных спиртов;
б) одноатомных спиртов и фенола; в) бензола и фенола?
10. В чем сходство и отличие (по строению и химическим свойствам) фенола и ароматических спиртов?
11. Каковы качественные реакции на: а) многоатомные спирты; б) фенолы?
12. Каковы способы получения: а) спиртов; б) фенола?
13. Дайте определения, что такое: первичные (вторичные, третичные) спирты, водородная связь, реакция этерификации, реакция поликонденсации, простые эфиры, сложные эфиры, ароматические спирты.
2.10 ЛАБОРАТОРНАЯ РАБОТА № 10 «ОБРАЗОВАНИЕ ДИЭТИЛОВОГО ЭФИРА»
ЦЕЛЬ: Изучить образование диэтилового эфира
РЕАКТИВЫ: этиловый спирт, концентрированная серная кислота
ОБОРУДОВАНИЕ: пипетка, мерный цилиндр, спиртовка, пробирка
ХОД РАБОТЫ
Смешать в пробирке 1 мл этилового спирта и 1 мл Н2SO4 (кислоту необходимо приливать к спирту небольшими порциями при взбалтывании). Сильно разогревшуюся смесь осторожно нагреть до начала кипения. При этом не обнаруживается ни образования горючих паров, ни появление запаха эфира.
Погасить спиртовку, в нагретую смесь очень осторожно прилить еще 5 – 10 капель этилового спирта.
Сразу же появляется запах диэтилового эфира.
Выполняемая операция | Прибавляемый реактив | Условия опыта | Наблюдения |
Контрольные вопросы:
1. Какие вещества называют сложными эфирами?
2. Как называют реакцию получения сложных эфиров? Номенклатура сложных эфиров.
3. Каковы физические свойства сложных эфиров?
4. Каковы основные области применения сложных эфиров?
5. Какие виды жиров известны?
6. Какова структура жиров?
7. Какие кислоты могут входить в состав жиров?
8. Каковы химические свойства:
а) твердых жиров;
б) жидких жиров?
9. Превращения жиров в организме.
10. Каковы основные области применения жиров?
Задания:
1. Составить структурные формулы веществ:
а) стеарат натрия;
б) этилбутаноат;
д) изоамилацетат;
е) пропилформиат.
2. Составить уравнения реакций:
а) гидролиза пропилового эфира бензойной кислоты;
б) получения пропилбутаноата;
в) гидролиза тристеарата глицерина;
3. Осуществить превращения:
этилацетат ацетат натрия метан метилформиат.
4. Сколько граммов 90%-го раствора уксусной кислоты потребуется для получения 8,8 г этилацетата? Ответ. 6,67 г.
2.11 ЛАБОРАТОРНАЯ РАБОТА № 11 «РАСТВОРИМОСТЬ В ВОДЕ КАРБОНОВЫХ КИСЛОТ И ИХ СОЛЕЙ. ОТНОШЕНИЕ КИСЛОТ К ИНДИКАТОРАМ»
ЦЕЛЬ: Изучить растворимость в воде карбоновых кислот и их солей. отношение кислот к индикаторам
РЕАКТИВЫ: уксусная, стеариновая, щавелевая, бензойная кислоты, дистиллированная вода, раствор NaOH
ОБОРУДОВАНИЕ: универсальная индикаторная бумага, 4 пробирки, держатель для пробирок, спиртовка
ХОД РАБОТЫ
Несколько капель или кристалликов каждой из кислот смешать с 1 - 2 мл воды в пробирке. Если кислота не растворяется при нормальной температуре, смесь нагреть.
По капле полученных растворов органических кислот нанести на полоску универсальной индикаторной бумаги, определить рН полученных растворов.
Нагретые смеси охладить, отметить, выделяются ли снова кристаллики кислоты.
В пробирки, содержащие осадок малорастворимой кислоты, добавить по 2 – 3 капли раствора NaOH, встряхнуть, отметить происходящие изменения.
Выполняемая операция | Прибавляемый реактив | Условия опыта | Наблюдения |
Контрольные вопросы:
1. Какие классы соединений с карбонильной группой известны?
2. Каковы общие формулы альдегидов, кетонов и карбоновых кислот?
3. Какие виды изомерии характерны для альдегидов и кетонов?
4. Каковы тривиальные названия первых семи гомологов альдегидов?
5. В чем различие физических свойств спиртов, альдегидов и кетонов? Каковы причины этих различий?
6. Каковы способы получения альдегидов и кетонов?
7. Каковы химические свойства предельных альдегидов?
8. Сравните альдегиды и кетоны по:
а) физическим свойствам;
б) составу;
в) химическим свойствам;
г) реакционной способности.
9. Какие вещества называют карбоновыми кислотами?
10. Какова классификация карбоновых кислот?
11. Какие виды изомерии характерны для предельных одноосновных карбоновых кислот?
12. Особенности номенклатуры предельных одноосновных карбоновых кислот.
13. Каковы способы получения предельных одноосновных карбоновых кислот?
14. Каковы физические свойства карбоновых кислот в сравнении со спиртами и альдегидами?
15. Каково строение карбоновых кислот?
2.12 ЛАБОРАТОРНАЯ РАБОТА № 12 «ОКИСЛЕНИЕ АНИЛИНА»
ЦЕЛЬ: Изучить свойства анилина
РЕАКТИВЫ: анилин, дистиллированная вода, растворы H2SO4 и K2Cr2O7
ОБОРУДОВАНИЕ: пипетка, пробирка
ХОД РАБОТЫ
К водной эмульсии анилина добавить 2 – 3 капли раствора K2Cr2O7 и 0,5 мл разбавленного раствора H2SO4.
Отметить все наблюдаемые изменения и написать уравнения реакций.
Выполняемая операция | Прибавляемый реактив | Условия опыта | Наблюдения |
Контрольные вопросы:
1. Что такое амины?
2. Какие виды аминов известны?
3. Какие виды изомерии характерны для аминов?
4. Каковы физические свойства предельных аминов и анилина?
5. В чем сходство и отличие химических свойств: аммиака и предельных аминов, предельных аминов и анилина?
6. Каковы области применения аминов?
7. Какие соединения называют гетероциклическими?
8. Каковы классификация и номенклатура гетероциклов?
9. Приведите примеры гетероциклов, которые:
а) являются основаниями;
б) не являются основаниями.
10. Какие химические свойства подтверждают ароматичность гетероциклов?
11. Обладает ли продукт гидрирования пиридина:
а) ароматическими свойствами;
б) свойствами основания? Почему?
12. Какое основание сильнее: пиррол или пирролидин? Почему?
13. Почему пиридин хорошо растворяется в воде, а пиррол плохо?
2.13 ЛАБОРАТОРНАЯ РАБОТА № 13 «БРОМИРОВАНИЕ АНИЛИНА»
ЦЕЛЬ: Изучить свойства анилина
РЕАКТИВЫ: анилин, дистиллированная вода, бромная вода
ОБОРУДОВАНИЕ: пипетка, пробирка, резиновые пробки
ХОД РАБОТЫ
К 5 мл воды добавить 1 каплю анилина, встряхивать до растворения, затем добавлять по каплям бромную воду до помутнения раствора.
Отметить все наблюдаемые изменения, написать уравнение и механизм основной реакции.
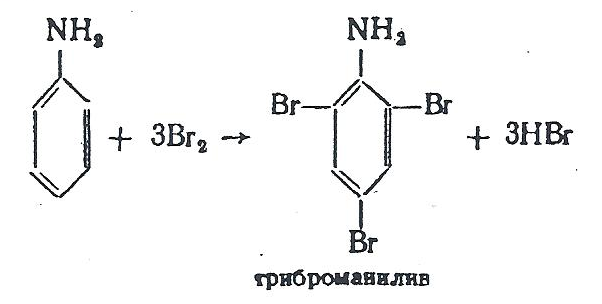
Являясь электронодонорным заместителем, аминогруппа повышает электронную плотность в ароматическом ядре, облегчая этим реакции электрофильного замещения.
Вместо анилина можно использовать для этого опыта соли анилина. Они бромируются так же легко, как и сам анилин.
Выполняемая операция | Прибавляемый реактив | Условия опыта | Наблюдения |
Контрольные вопросы:
Строение аминов. Изомерия аминов. Номенклатура аминов. Физические свойства аминов. Способы получения аминов. Амины — органические основания. Химические свойства аминов. Реакции азотной кислотой. Цветные реакции анилина.СПИСОК ЛИТЕРАТУРЫ
, , Органическая химия. СПб.: Иван Федоров, 2005. Органическая химия. Т.1 и 2. М,: Академкнига, 2005. , Биоорганическая химия. М.: Дрофа, 2005. Стереотип 2005. , , . Органическая химия в 4 томах. Для студентов вузов по направлению и специализации. Химия, М.: Бином, 2004 , Основы теоретической химии процессов органических веществ и нефтепереработки. Учебник для вузов. СПб.:Химиздат, 2005. , . Курс современной органической химии. Учебное пособие для вузов, 2-е изд. М: Высшая школа, 2003. , , Органическая химия. Учебник для вузов, 3-е изд. Стереотип, в 2 кн., М.: Дрофа. 2004. Справочник по органической химии. Учебное пособие, СПб: Паритет, 2002. Органическая химия. Учебник для студентов вузов, обучающихся по агрономическим специальностям. 5-е изд. М. : Стереотип-Дрофа,2002. Органическая химия,2-е изд. М.: Медицина, 2002. В. И.,Основы химии живого. Учебник для вузов: М. Химиздат,2004. глубленный курс органической химии, 2-а тома, М: Химия,1981, Органическая химия, М.: Химия 1979, Робертс Дж., Основы органической химии, 2-а тома, М: Мир, 1978 Механизмы реакций в органической химии М.: Химия, 1973. овременная органическая химия. Т. 1 и 2. М.: Химия, 1981.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |




