Ткани и плазма.
Трицепс голени был тщательно расчленен и взвешен для расчета CSA. Камбаловидная и EDL с левой стороны, нестимулированные мышцы иссекали и замораживали в изопентане охлажденном жидким азотом. Блоки хранили при -80 ° C до обработки для гистологии. Кровь, которую собирали из грудной полости через аорту, была сокращена. Плазму приготовили и храненили при -80 ° С до измерения общего потенциала антиоксидантов. Гистологическая оценка.
Поперечные срезы (толщиной 10 мкм) камбаловидной мышцы и EDL были получены из криостата (модель HM 560M, Microm, Volketswil, Швейцария), окрашены гематоксилином и эозином в соответствии с классическими процедурами. Фотографии с высоким разрешением были сделаны AxioCam MRC цифровой камерой (Zeiss, Feldbach, Швейцария), соединенной с инвертированным микроскопом (Zeiss Axiovert 35М). Одно сечение было проанализировано у каждого из 7-10 животных в каждой группе. Некроз (NRS) определяли с помощью программного обеспечения Metamorph (Visitron Systems, Puchheim, Germany) путем измерения поверхности всех здоровых тканей от всего поперечного сечения мышцы. Вся поверхность поперечного сечения также была измерена. NRS в конечном итоге выражали как процент от общей площади поперечного сечения поверхности. Образцы были закодированы и проанализированы наблюдателем, который не знал деталей исследования. Определение общего антиоксидантного потенциала в плазмы.
Общий антиоксидантный потенциал плазмы оценивали с помощью коммерческого набора ( Антиоксидантный статус, Randox лаборатории, Ардморе, UK) в соответствии с инструкциями производителя. Общий потенциал антиоксиданта (в ммоль / л) определяли путем сравнения с контрольной сывороткой известного антиоксидантного статуса (Randox).
Статистический анализ.
Статистический анализ проводился с использованием двустороннего непарного теста Стьюдента, контрольная группа mdx5Cv использовать в качестве опорной для сравнения с любой другой группой. Различия со значениями P ≤ 0,05 считались значимыми.
РЕЗУЛЬТАТЫ
Эффекты ГТЕ, ЭГКГ, и ПTК от веса мыши и приема пищи.
Трех-недельные мыши имели средний вес тела 8,6 (SD 0,7) г. Как показано на рис. 1А, животные, которые получили 0,25% ГТЕ и 0,1% ЭГКГ были немного легче, чем необработанные mdx5Cv мышеи, когда они вошли в протокол. Затем средний вес тела был одинаковым во всех группах в течение следующих 4 недель. На пятой неделе лечения необработанные мыши mdx5Cv прибавили в весе быстрее, чем другие животные. Мыши стали значительно тяжелее, чем нормальные мышей и mdx5Cv мыши, получавшие низкую дозу ГТЕ или ПTК (фиг. 1А).
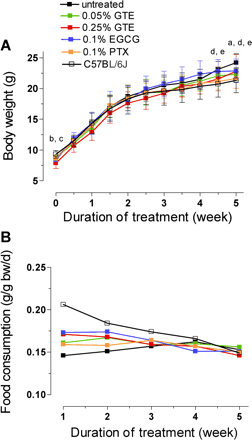
![]()
После первой недели лечения, индекс потребления пищи варьировался от 0,146 (необработанные mdx5Cv) до 0,206 г / г массы тела / день (нормальные мыши) (фиг. 1B ). Индекс потребления продуктов питания нормирован после этого к значению ~ 0,150 г / г веса тела / день. Это соответствует суточной дозе препарата 75 и 375 мг / кг массы тела для групп, и 0,05% и 0,25% ГТЕ, соответственно, и 150 мг / кг массы тела у получавших ЕГКГ 0,1% и 0,1% ПТХ.
Эффекты ГТЕ, ЭГКГ, и ПТК на плазменный общий антиоксидантный потенциал.
Общий антиоксидантный потенциал измеряли в плазме обоих обработанных и необработанных животных. Не было найдено существенных отличий между группами после 1 недели диеты (рис. 2). Однако, после 5 недель диетотерапии, все четыре группы представили небольшое, но значимое увеличение антиоксидантного потенциала плазмы (рис. 2). Значения (ммоль / л) варьировали от 1,72 (SD 0,16) для необработанных животных mdx5Cv до 2,35 (SD 0,55) для животных, которые получали ЭГКГ или ПТК. Доза ГТЕ повышает потенциал плазмы до ~ 2,10. Нормальные мыши имели антиоксидантный потенциал 1,85 (SD 0,35).
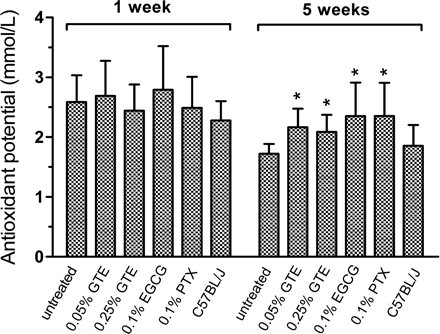
Эффекты ГТЕ, ЭГКГ, и ПТК на гистологию мышц.
Поперечные срезы EDL и камбаловидной мышцы окрашивали гематоксилином и эозином. Здоровые и регенерирующие мышечные волокна было легко определить по наличию либо периферических или центральных ядер соответственно (рис. 3). Очаги некротических волокон были выделены наличием плотно расположенных иммунных клеток, а вновь образованные регенерирующие миотубы определялись как мелкокалиберные клетки с повышенной эозинофилией и большими центральными ядрами (фиг. 3, и D).
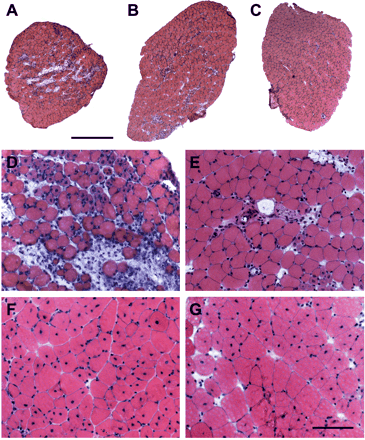
Фракции мышц, пострадавших от некроза и регенерации показаны на рис. 4. EDL мышцы необработанных дистрофических мышей в 4-недельном возрасте имели ~ 30% NRS (рис. 3, А и D). Напротив, у мышей, которых
![]()
кормили в течение 1 недели с высокой дозой ГТЕ, ЭГКГ, или ПТК (рис. 3, В и Е;. Рис. 4), часть некротических областей EDL мышцы упала до 17-20%. Это соответствует 31-42% защиты по сравнению с необработанными мышами mdx5Cv. Камбаловидная мышца более затронуты, NRS значение 45-53% во всех группах после 1 недели диетотерапии.
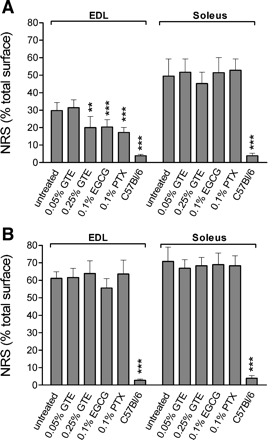
Через 5 недель приема пищевых добавок, NRS значения были сходными во всех группах мышей с дистрофией, независимо от лечения. NRS значения достигли 56-64% для EDL мышц и 67-71% для камбаловидной мышцы (рис. 4). В то время эти фракции состояли главным образом из полностью регенерировавших зарождающихся волокон с несколькими признаками некротических волокон или проникновением иммунных клеток (рис. 3, F и G).
Эффекты ГТЕ, ЭГКГ, и ПТК на трицепс голени.
После 1 недели кормления стандартным кормом, CSA нормальных трицепсов голени была значительно ниже, чем у мышей mdx5Cv (табл. 1). Это свидетельствует о гипертрофии дистрофических мышц, как сообщает Сакко и соавт. (36). Примечательно, за исключением низких доз ГТЕ, каждое из тестируемых соединений уменьшает CSA трицепсов почти до нормальных значений. В 8-недельном возрасте животных различие между нормальными и дистрофическими мышцами больше не видел. Mdx5Cv мыши, получавшие низкие дозы ГТЕ или ПТК, однако, снизили CSA значения.
Эффекты ГТЕ, ЭГКГ, и ПТК на параметры изометрической силы.
В таблице 1 приведены конкретные уровни напряжения трехглавой мышцы голени. Этот параметр считается физиологически более актуальным, чем абсолютное напряжение, которое находится под влиянием изменений в абсолютной мышечной массе и оптимальной длины. В тот же период времени, необработанные мышцы mdx5Cv отображает весьма значительное снижение пика напряжения по сравнению с нормальными мышами (Pt = 33,2 против 60,2 mN/mm2 и 35,3 против 67,4 mN/mm2, через 1 и 5 недель, соответственно). После 1 недели, низкие дозы ГТЕ увеличили Pt на 22%, но это не существенно отличается от необработанных животных. Высокие дозы ГТЕ, ЭГКГ, и ПТК добавки в течение 1 нед заметно дополнили Pt (+60% +94% и +66% соответственно, таблица 1) до значений, близких к нормальным мышам. Когда питание было продлено в течение 5 недель последовательно увеличена Pt от 42 до 59% по сравнению с необработанными дистрофическими животными (табл. 1). Аналогичным образом, максимальное тетаническое напряжение Po было значительно выше у нормальных мышей, чем у необработанных дистрофических мышей в обеих временных точках (+55% до +35% через 1 и 5 недель лечения соответственно). Кроме того, высокие дозы ГТЕ, ЭГКГ, и ПТК за 1 неделю увеличили Po (+21 до +36% по сравнению с необработанными дистрофическими мышами). Тем не менее, увеличение было статистически значимым для ПТК-группы (табл. 1). В противоположность этому, после 5 недель лечения, тестируемые вещества больше не изменяли Ро, которое изменяется в пределах от -10% до +10% по сравнению со значениями необработанных мышей. После 1 и 5 недель лечения, Po значения были неизменными у нормальных мышей (335 и 347 mN/mm2, соответственно). За тот же период, Po значения были увеличены с 216 до 257 mN/mm2 в необработанных mdx5Cv (табл. 1).Интересно, что в результате изменений Pt и Ро после диет, соотношение фазового к тетанического напряжения были значительно повышены всеми веществами по сравнению с необработанными mdx5Cv (+24 до +59%), что привело к почти нормальным значениям в течение 5 недель (табл. 1). Кривые, соединяющие тетаническое напряжение и частоту стимуляции, были созданы (рис. 5). Фракцию максимального усилия, развиваемого у необработанных дистрофических животных на низкой частоте стимуляции (т. е. в условиях неполной столбняк), была меньше, чем их нормальные аналоги. При 20 Гц, доля от максимальной силы была разработана 20 против 24% (т. е. +20%) после 1 недели и 17 против 22% (т. е. +28%) после 5 недель для дистрофических против контрольных мышей, соответственно. После лечения значения дистрофических животных были сдвинуты вверх и стали аналогичным контрольным животным (рис. 5), особенно при высоких дозах ГТЕ, ЭГКГ, и ПТК. Этот эффект хорошо видно после 1 недели, а через 5 недель набранные силы во всех четырех группах животных mdx5Cv стали значительно выше, чем у необработанных мышей mdx5Cv, приближая значения к здоровым необработанным контрольным животным.
![]()
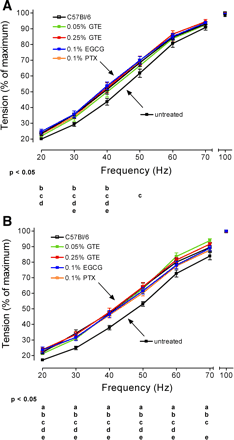
Эффекты ГТЕ, ЭГКГ, и ПТК на сокращение и расслабление.
Время до пика (ТТП) и время полу - релаксации от пика (RT1 / 2) (таблица 1) были определены из оптимальных фазовых следов подергивания. ВДП составило ~ 40-41 мс для нормальных и необработанных животных в любом возрасте. Диета в течение 1 недели существенно не изменяет этот параметр. Кормление животных в течение 5 недель ГТЕ, ЭГКГ, или ПТК уменьшили ТТП от 2 до 10%, что свидетельствует о более быстром сокращении. Статистическая значимость была достигнута у животных, которые получали ЭГКГ и ПТК, но не ГТЕ (табл. 1). Четырехнедельные нормальные и дистрофические животные, которых кормили стандартной диетой, имели сходные RT1 / 2 значения (табл. 1). Никаких существенных изменений не было замечено при кормлении добавками, хотя ЭГКГ это значение увеличил на 22% по сравнению с необработанными мышами. В отличие от этого, трицепс голени от нормальных 8-WK-старых животных расслабился намного быстрее, чем у соответствующего возраста дистрофических животных. Интересно, что RT1 / 2 значение мышей mdx5Cv обработанных любым из тестируемых веществ было значительно уменьшено по сравнению с необработанными животными mdx5Cv, падая до значений, аналогичные нормальных животных (табл. 1).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |


