Решение. 17 баллов
Это алюминий. 1 балл |
Применение. 6 баллов.
|
2KOH(конц.) + 6H2O(гор) + 2Al = 2K[Al(OH)4] + 3H2↑ t 2Al + 6KOH = К3AlO3 + 3H2↑ 8Al + 18 H2O + 5 KOH (конц.)+ 3KNO3 = 8K[Al(OH)4] + NH3↑ По 2 балла за каждое уравнение |
Задание 5. Изомеры.
Два углеводорода содержат 85,72 % углерода, а их относительная плотность по водороду при нормальных условиях равна 21 и 28. Составьте структурные формулы всех изомеров этих веществ, назовите их. Предложите способы получения двух любых изомеров каждого из двух веществ. (13 баллов).
Задание 3.
| Находим молярные массы углеводородов: М1(СхНу) = D(Н2) • M(Н2) = 21 • 2 = 42 г/моль М2(СхНу) = D(Н2) • M(Н2) = 28 • 2 = 56 г/моль | 1 балл |
Массовая доля водорода: 100-85,72=14,28 Находим формулу вещества: х : у = 85,72/12 : 14,28/1 = 1 : 2Простейшая формула веществ (СН2)n | 1 балл |
| Устанавливаем формулы углеводородов: M(СН2) = 14 г/моль; 42/14=3, формула первого вещества C3H6; второго: 56/14=4, C4H8 C3H6 - пропен или циклопропан C4H8 – бутен-2, бутен-2, 2-метилпропен-1, циклобутан, метилциклопропан, цис-бутен-2, транс-бутен-2 | 2 балла по 0,5 балла за название и по 0,5 балла за формулу |
13 баллов.
Задание 6. Закончите уравнения реакций.
Восстановите левую или правую часть уравнений, следующих химических реакций:
1) … → MnBr2 + Br2 + 2H2O
2) … → 2CaCO3↓ + 2H2O
3) … → 4Fe(OH)3↓ + 4Na2SO4
4) CuS + 4H2O2 → …
5) 6HNO3 + P2O5 → …
Решение:
1) MnO2 + 4HBr = MnBr2 + Br2 + 2H2O
2) Ca(OH)2 + Ca(HCO3)2 = 2 CaCO3↓ + 2H2O
3) 4FeSO4 + 8NaOH + O2 + 2H2O = 4Fe(OH)3↓ + 4Na2SO4
4) CuS + 4H2O2 = CuSO4 + 4H2O
5) 6HNO3 + P2O5 = 3N2O5 + 2H3PO4
За каждое уравнение по 2 балла, всего 10 баллов.
. ШКОЛЬНЫЙ ЭТАП.
2016-2017 учебный год.
ХИМИЯ. 11 КЛАСС.
120 минут.
Дорогие ребята! Поздравляем с участием в олимпиаде школьников! Отвечая на вопросы и выполняя задания, – не спешите, так как ответы не всегда очевидны и требуют применения не только химических знаний, но и общей эрудиции.
Успехов Вам в работе!
Задание 1. Ученые-химики.
При подготовке к экзамену по химии юный химик написал себе шпаргалку в форме таблицы, однако в спешке перепутал имена и достижения ученых-химиков. Приведите записи в соответствие. В ответе укажите цифру и букву, соответствующую правильному ответу.
Фамилия | Достижение |
1 Николай Зинин | А Провѐл фундаментальные исследования в области цепных реакций, единственный Нобелевский лауреат по химии в России. |
2 Михаил Кучеров | Б Синтезировал мочевину из неорганических веществ |
3 Генри Кавендиш | В Экспериментально подтвердил закон сохранения массы |
4 Сергей Лебедев | Г Открыл метод гидратации соединений ацетиленового ряда в присутствии ртутных солей |
5 Михаил Ломоносов | Д Сформулировал теорию строения органических веществ |
6 Сванте Аррениус | Е Установил состав основных компонентов воздуха |
7 Фридрих Вѐлер | Ж Впервые получил водород |
8 Антуан Лавуазье | З Сформулировал теорию электролитической диссоциации |
9 Александр Бутлеров | И Впервые получил синтетический каучук в СССР |
10 Николай Семенов | К Осуществил превращение нитробензола в анилин |
10 баллов
Задание 2. Неизвестное вещество.
Вещество А состоит из двух однозарядных ионов. Положительный ион содержит одно ядро и 18 электронов. Отрицательный ион состоит из четырѐх ядер и 32 электронов. При нагревании А образуется два вещества – твѐрдое вещество В и газ С, молекула которого со стоит из двух одинаковых ядер и 16 электронов. Вещества А и В имеют одинаковый качественный состав.
Определите вещества А, В, С и напишите уравнение разложения вещества А.
10 баллов
Задание 3. Цепочка превращений.
Для приведенной ниже схемы превращений определите вещества А — Е, изобразите их
структурные формулы. Для реакций (1), (2) и (3) укажите реагенты и условия протекания.
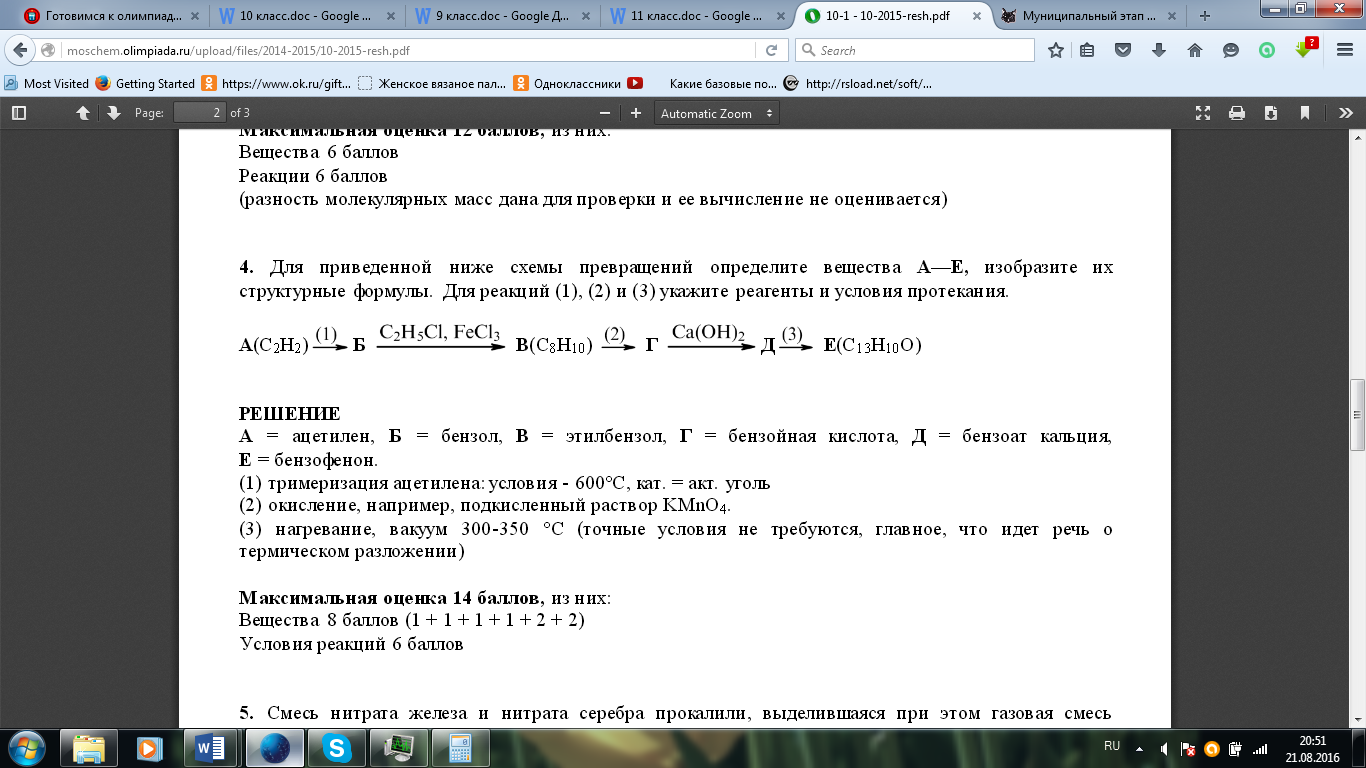
14 баллов
Задание 4. Расшифруйте вещества А – Е.
Соль А — сильный окислитель, окрашивает пламя в фиолетовый цвет. При нагревании А
разлагается с образованием солей Б и В. При термическом разложении А в присутствии катализатора
образуется соль В и газ Г (простое вещество). При электролизе расплава или раствора соли В на
аноде выделяется газ Д. При взаимодействии Д со щелочью Е можно получить исходную соль А.
Напишите уравнения упомянутых реакций и укажите условия их протекания.
Известно, что разность молекулярных масс солей Б и В составляет 64.
12 баллов
Задание 5. Определите элементы.
Определите возможные элементы (X, Y, Z), соединения которых участвуют в схемах превращений:
XO3 + H2O → H2XO4, Y2O3 + HCl → YCl3 + H2O, Z2O7 + NaOH → NaZO4 + H2O,а) если зашифрованы p-элементы,
б) если зашифрованы d-элементы.
Запишите уравнения соответствующих реакций. 12 балов
Задание 6. Загадочный раствор.
В 5 склянках без этикеток находятся растворы следующих веществ: KOH, Na2CO3, HCl, Al2(SO4)3, KCl.
Опишите, как распознать растворы этих веществ, не используя других химических реактивов (последовательность действий, наблюдения, выводы).б) Один из осадков, получаемых при взаимодействии этих растворов, растворяется в избытке одного из исходных веществ. Что это за осадок и как объяснить растворение осадка (уравнение реакции). 20 баллов
. ШКОЛЬНЫЙ ЭТАП. ХИМИЯ. 11 КЛАСС.
2016-2017 учебный год.
Ответы на задания. 78 баллов.
Задание 1. Ученые-химики.
При подготовке к экзамену по химии юный химик написал себе шпаргалку в форме таблицы, однако в спешке перепутал имена и достижения ученых-химиков. Приведите записи в соответствие. В ответе укажите цифру и букву, соответствующую правильному ответу.
1) 1К (Николай Зинин - осуществил превращение нитробензола в анилин)
2) 2Г (Михаил Кучеров - открыл метод гидратации соединений ацетиленового ряда в
присутствии ртутных солей)
3) 3Ж (Генри Кавендиш – впервые получил водород)
4) 4И (Сергей Лебедев - впервые получил синтетический каучук в СССР)
5) 5В (Михаил Ломоносов - экспериментально подтвердил закон сохранения массы)
6) 6З (Сванте Аррениус - сформулировал теорию электролитической диссоциации)
7) 7Б (Фридрих Вѐлер - синтезировал мочевину из неорганических веществ)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |




