8) 8Е (Антуан Лавуазье - установил состав основных компонентов воздуха)
9) 9Д (Александр Бутлеров - сформулировал теорию строения органических веществ)
10) 10А (Николай Семенов - провѐл фундаментальные исследования в области цепных
реакций, единственный гражданин России – Нобелевский лауреат по химии)
10 баллов
Задание 2. Неизвестное вещество.
Вещество А состоит из двух однозарядных ионов. Положительный ион содержит одно ядро и 18 электронов. Отрицательный ион состоит из четырѐх ядер и 32 электронов. При нагревании А образуется два вещества – твѐрдое вещество В и газ С, молекула которого со стоит из двух одинаковых ядер и 16 электронов. Вещества А и В имеют одинаковый качественный состав.
Определите вещества А, В, С и напишите уравнение разложения вещества А.
1. Проведено рассуждение: газ С представляет собой простое вещество, образованное химическим элементом, электронная оболочка которого состоит из 8-ми электронов. Этот элемент – кислород, следовательно газ С – кислород O2.
2. Проведено рассуждение. положительный ион, входящий в состав вещества А – это К+, так как атом калия содержит 19 электронов, а ион К+- 18 электронов.
3. Проведено рассуждение. Вещество А – соль калия, при нагревании выделяющая кислород. Очевидно, что в состав аниона входят атомы кислорода и какого-то другого элемента. Определим этот элемент. Составим уравнение баланса по количествам атомов и электронов в анионе соли А:
N(O)·8 + N(X)·N(з в Х) + 1з= 32, где N(O) – количество атомов кислорода, N(X) – количество атомов неизвестного элемента, N(з в Х) – количество атомов в элементе Х
4. Если N(O) =1, тогда N(X) = 4-1 = 3, а N(з в Х) – не целое число – решений нет.
Если N(O) =2, тогда N(X) = 4-2 = 2, а N(з в Х) – не целое число – решений нет.
Если N(O) =3, тогда N(X) = 4-3 = 1, а N(з в Х) = 7 – это азот.
Следовательно вещество А – нитрат калия KNO3
5. Составлено уравнение реакции разложения нитрата калия: 2KNO3 → KNO2 + O2↑
Вещество А – нитрат калия KNO3, В – нитрит калия KNO2, С – кислород O2 .
Итого 10 баллов
Задание 3. Цепочка превращений.
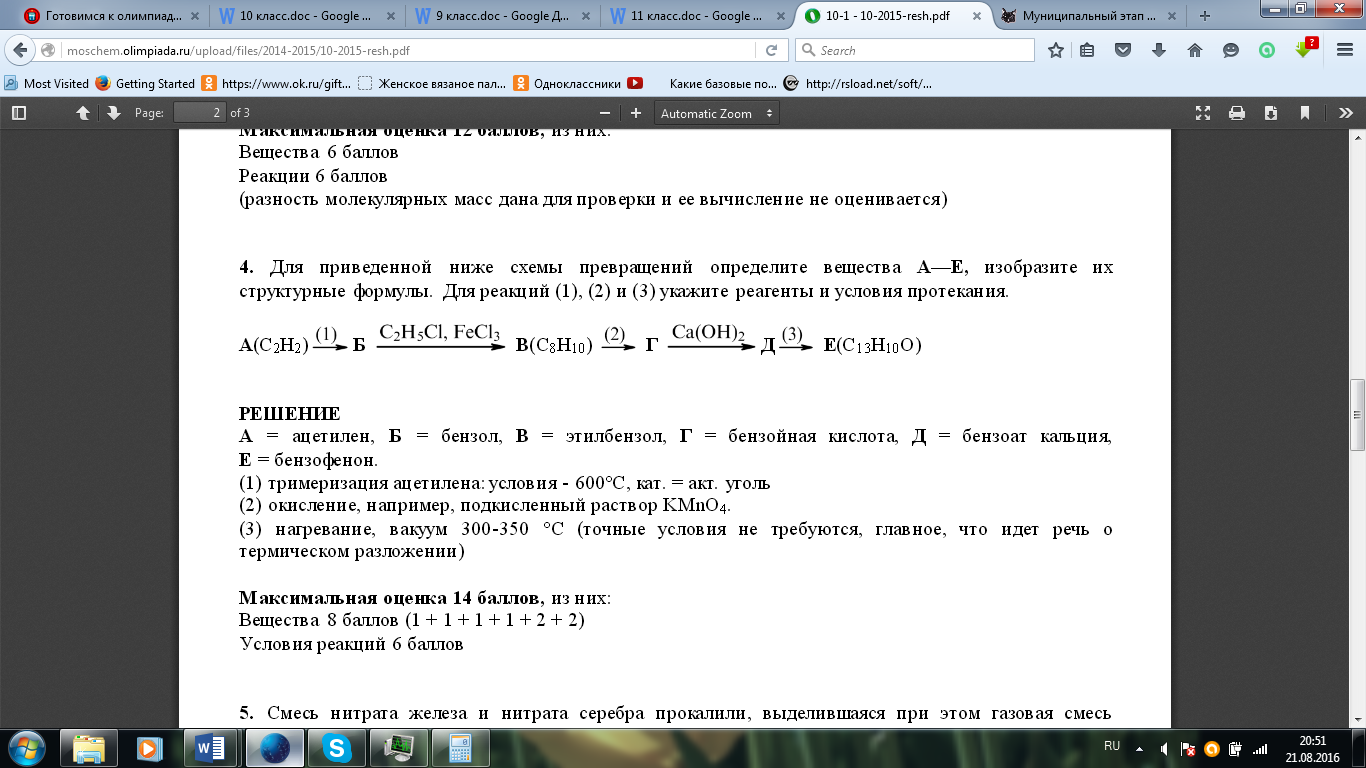
Для приведенной ниже схемы превращений определите вещества А — Е, изобразите их
структурные формулы. Для реакций (1), (2) и (3) укажите реагенты и условия протекания.
14 баллов
РЕШЕНИЕ
А = ацетилен,
Б = бензол,
В = этилбензол,
Г = бензойная кислота,
Д = бензоат кальция,
Е = бензофенон.
тримеризация ацетилена: условия - 600°С, кат. = акт. Уголь (2) окисление, например, подкисленный раствор KMnO4.(3) нагревание, вакуум 300 - 350°С (точные условия не требуются, главное, что идет речь о
термическом разложении)
Максимальная оценка 14 баллов, из них:
Вещества 8 баллов (1 + 1 + 1 + 1 + 2 + 2)
Условия реакций 6 баллов
Задание 4. Расшифруйте вещества А – Е.
Соль А — сильный окислитель, окрашивает пламя в фиолетовый цвет. При нагревании А
разлагается с образованием солей Б и В. При термическом разложении А в присутствии катализатора
образуется соль В и газ Г (простое вещество). При электролизе расплава или раствора соли В на
аноде выделяется газ Д. При взаимодействии Д со щелочью Е можно получить исходную соль А.
Напишите уравнения упомянутых реакций и укажите условия их протекания.
Известно, что разность молекулярных масс солей Б и В составляет 64.
12 баллов
РЕШЕНИЕ
Вещества: А = KClO3, Б = KClO4, В = KCl, Г = O2, Д = Cl2, Е = KOH
Реакции:
4KClO3 = 3KClO4 + KCl
2KClO3 = 2KCl + 3O2 (катализатор MnO2)
2KCl (электролиз расплава) = 2K + Cl2
2KCl + 2H2O (электролиз раствора) = H2+ 2KOH + Cl2
KOH + 3Cl2= KClO3 + 5KCl (горячий раствор!)
Максимальная оценка 12 баллов, из них:
вещества 6 баллов,
реакции 6 баллов (разность молекулярных масс дана для проверки и ее вычисление не оценивается)
Задание 5. Определите элементы.
Определите возможные элементы (X, Y, Z), соединения которых участвуют в схемах превращений:
XO3 + H2O → H2XO4, Y2O3 + HCl → YCl3 + H2O, Z2O7 + NaOH → NaZO4 + H2O,а) если зашифрованы p-элементы,
б) если зашифрованы d-элементы.
Запишите уравнения соответствующих реакций.
За каждое уравнение по 1 баллу.
Вариантов решения задания несколько. Приведен один из них. |
а) если зашифрованы p-элементы: 1. SO3+H2O=H2SO4 |
б) если зашифрованы d-элементы. 1. 3CrO3 + H2O= 2H2CrO4 2. Fe2O3+6HCl=2FeCl3+3H2O 3. Mn2O7 + 2NаOH = 2NаMnO4 + H2O |
Задание 6. Загадочный раствор.
В 5 склянках без этикеток находятся растворы следующих веществ: KOH, Na2CO3, HCl, Al2(SO4)3, KCl.
Опишите, как распознать растворы этих веществ, не используя других химических реактивов (последовательность действий, наблюдения, выводы).б) Один из осадков, получаемых при взаимодействии этих растворов, растворяется в избытке одного из исходных веществ. Что это за осадок и как объяснить растворение осадка (уравнение реакции). 20 баллов
Проведём мысленный эксперимент. Рассмотрим содержимое пробирок. Вещества визуально неразличимы – это бесцветные прозрачные растворы.
Составим таблицу возможных попарных взаимодействий веществ, в результате которых мы будем (или не будем) наблюдать определённые признаки реакций.
KOH | Na2CO3 | HCl | Al2(SO4)3 | KCl | |
KOH | х | - | - | ос.(р) | - |
Na2CO3 | - | х | газ | ос.+газ | - |
HCl | - | газ | х | - | - |
Al2(SO4)3 | ос.(р) | ос.+газ | - | х | - |
KCl | - | - | - | - | х |
Итог | ос.(p) | газ, | газ | ос.(p), | нет |
Определение веществ – 10 баллов.
Уравнение реакции в молекулярном виде – по 1 баллу, в сокращенном ионном – по 1 баллу.
6KOH + Al2(SO4)3 = 2Al(OН)3↓ + 3К2SO4
Al(OH)3 + 3 NaOH = Na3[Al(OH)6]
Na2CO3 + 2 HCl = 2 NaCl + CO2 + Н2О
Al2(SO4)3 + 3Na2CO3 + 3H2O = 2Al(OH)3 + 3Na2SO4 + 3CO2
Карбонат натрия должен в одном случае дать реакцию с выделением газа, и в другом - реакцию с одновременным выпадением осадка и выделением газа (это результат полного гидролиза при взаимодействии растворов карбоната натрия и сульфата алюминия – 2 балла.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



