![]()
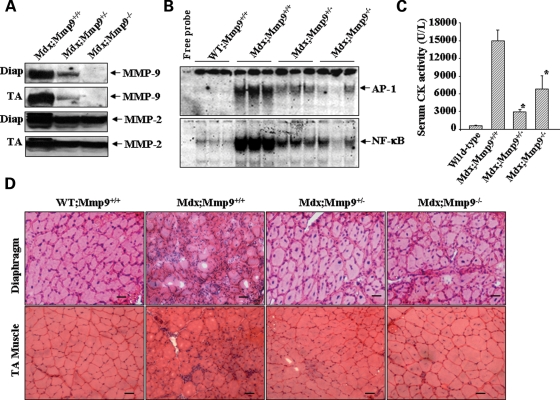
Для изучения эффекта ингибирования ММП-9 на патогенез в скелетных мышцах у MDX мышей, мы измерили уровень сывороточной креатинкиназы (CK) у 8-недельных мышей WT, MDX; ММП9 + / +, MDX; ММП9 + / - и MDX, ММП9-/ - мышей. Как показано на рисунке 3C, CK уровни были значительно ниже в MDX; ММР9 + / - и MDX; ММР9-/ - по сравнению с однопометница MDX; ММР9 + / + мышей, обеспечивая тем самым начальную доказательства того, что ингибирование MMP-9 подавляет активность скелетной травмой мышцы в MDX мышей. Поскольку миопатия у мышей MDX связана с значительными нарушениями ЭЦM, мы изучали эффекты ингибирования ММП-9 деятельности на структуру скелетных мышц у MDX мышей. Диафрагма и TA мышцы WT/MМП9 + / +, MDX; ММП9 + / +, MDX; ММП9 + / - и MDX; ММП9-/ - мыши были выделены и криосекции (10 мкм) окрашивали гематоксилином и эозином (H & E). Тем не менее, MDX; ММП9 + / + мышей показало типичные черты мышечной дистрофии, характеризующиеся слоем волокон переменного диаметра, центральным зарождением ядер и появления темно окрашенных ядер клеток воспаления между соседними волокнами (рис. 3D). В отличие от скелетных мышц MDX; ММП9 + / - и MDX; ММП9-/ - мыши показали значительное улучшение мышечной структуры, диаметр волокна был более равномерным и количество воспалительных клеток между соседними волокнами резко сократилось (рис. 3D).Гетерозиготное или гомозиготное удаление MMП-9 ослабляет накопление макрофагов, некроз волокон и улучшает силу в скелетных мышцах мышей MDX. MMП-9 является главным медиатором воспалительного ответа, в следующий раз мы исследовали, может ли ингибирование MMП-9 влиять на инфильтрацию макрофагов в скелетных мышцах мышей MDX. Икроножная мышца 7 - 8-недельных WT; ММП9 + / +, MDX; ММП9 + / +, MDX; ММП9 + / - и MDX; ММП9-/ - мыши были окрашены для выявления макрофагов с использованием антимышиных F4/80 (ABD Serotec). Объем образца мышцы рассчитывается как произведение площади сечения и толщины (10 мкм). Концентрация макрофагов была выражена как число клеток на кубический миллиметр (мм3). Интересно, что концентрация F4/80 позитивных клеток была значительно сокращена в икроножной мышце MDX; ММП9 + / - и MDX; ММП9-/ - мышей по сравнению с MDX; ММП9 + / + мышей (рис. 4, Б).
![]()
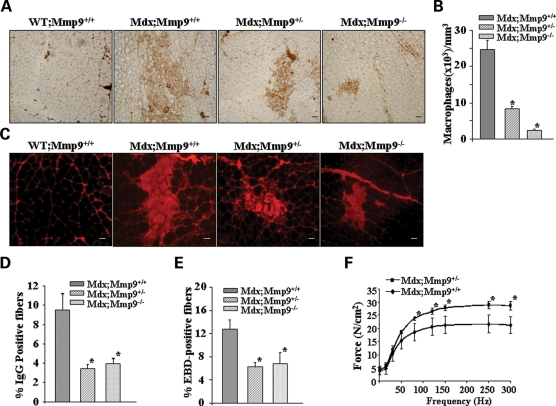
Потому что некроз является основным механизмом смерти скелетных мышечных волокон у мышей MDX и пациентов с МДД (32), мы исследовали, может ли генетические абляции MMП-9 влиять на некроз волокон скелетных мышц мышей MDX. Мыши WT контроля не показали внутриклеточного окрашивания волокна с анти-IgG (рис. 4C). В отличие от них MDX ММП9 + / + мыши показали внутриклеточное окрашивание для IgG в части их мышечных волокон (рис. 4в). Тем не менее, количество некротических (заполненных) волокон в икроножной мышце значительно сократилось в MDX; ММП9 + / - и MDX; ММП9-/ - мышей по сравнению с MDX; ММП9 + / + мышей (рис. 4в и D).Мы также использовали Эванс синий краситель (EBD), чтобы определить проницаемость скелетных мышц, что были повреждены в результате мышечной дистрофии (26). Как и некроз, процент EBD-позитивных волокон был значительно снижен в скелетных мышцах MDX; ММП9 + / - и MDX; ММП9-/ - мышей по сравнению с однопометницами MDX; ММП9 + / + мышей (рис. 4E).Наконец, мы исследовали влияние генетических абляций MMП-9 на силу скелетных мышц у многомерных мышей. Сила, возникающая в камбаловидной мышце при изометрических сокращениях была значительно выше у MDX; ММП9 + / - по сравнению с однопометницами MDX; ММП9 + / + мышей (рис. 4е). Взятые вместе, эти данные убедительно показывают, что ингибирование MMП-9 улучшает деятельность скелетных мышц и улучшается сократительная функция мышц у многомерных мышей.
Генетическое удаление MMП-9 ослабляет фиброз в диафрагме MDX мышей.
Фиброз является важной патологической особенностью дистрофических мышц MDX мышей и пациентов с МДД (2-4). Для того чтобы понять роль ММП-9 в процессах фиброза у MDX мышей, мы изучали накопление коллагеновых волокон в диафрагме с использованием метода окрашивания Трихром Массона. Как показано на рисунке 5А, уровень коллагена(Синего цвета) был значительно ниже у MDX; ММП9 + / - или MDX; ММП9-/ - мышей по сравнению с однопометниками MDX; ММП9 + / +. Хотя скелетные мышцы могут содержать много типов коллагена, коллаген I и III являются основными, которые находятся в ЭЦM скелетных мышц (33), и резко возросло в дистрофических мышцах мышей MDX (34). В отличие от коллагена IV, который присутствует в основном в базальной мембране мышечных волокон (33). Иммуногистохимический и вестерн-блот анализ показал, что уровни типа I и типа III коллагена были значительно сокращены у MDX; ММП9 + / - и MDX; ММП9-/ - мышей по сравнению с однопометниками MDX; ММП9 + / + мышей (рис. 5B иC). Интересно, что среди MDX; ММП9 + / - и MDX; ММП9-/ - мышей, уровень коллагена I и III был значительно ниже у MDX; ММП9 + / - мышей по сравнению с MDX; ММП9-/ - мышами (рис. 5B C). Хотя точный механизм остается неизвестным, вполне возможно, что небольшое количество MMП-9 может быть необходимо для метаболизма коллагена в целях предотвращения фиброза в скелетных мышцах мышей MDX. Тем не менее, снижение уровня коллагена I и III в диафрагме MDX; ММП9 + / - и MDX; ММП9-/ - мыши явно показывают, что ММП-9 вносит свой вклад в фиброз. В отличие от коллагена I и III, уровень коллагена IV значительно увеличился в MDX; ММП9 + / - и MDX; ММП9-/ - мышей по сравнению с однопометниками MDX; ММП9 + / + мышей (рис. 5B и C).
![]()
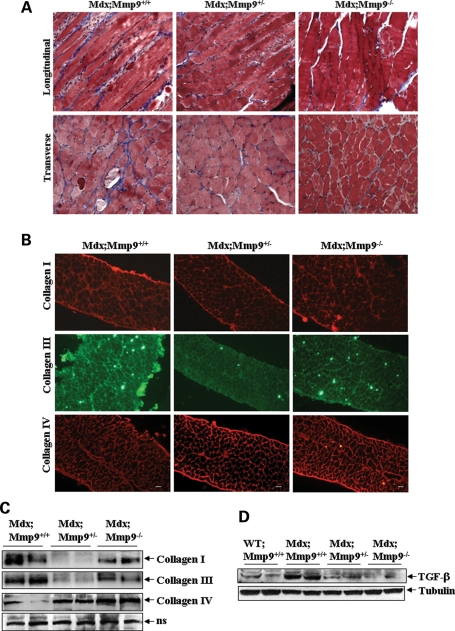
TGF-в является преобладающим посредником фиброза (35). Повышение уровня TGF-в было обнаружено в дистрофических мышцах мышей MDX (36,37) и пациентов с МДД (38). MMП-9 как известно, вызывает активацию скрытых TGF-в в зрелые формы протеолитическим удалением его ингибирующей области (13,39). Чтобы определить механизмы, с помощью которых повышенные уровни MMП-9 приводят к фиброзу у многомерных мышей, мы определили уровень активного TGF-в белка в мышцах диафрагмы методом вестерн-блотта. Существовало незначительное количество активного TGF-в белков в скелетных мышцах WT контрольных мышей (данные не показаны). Тем не менее, диафрагма MDX; ММП9 + / + мышей содержала большое количество TGF-в. Интересно, что по сравнению с MDX; ММП9 + / + мышами, уровни TGF-в белков были значительно сокращены у MDX; ММП9 + / - или MDX; ММП9-/ - мышей (рис. 5б). Эти результаты показывают, что ММП-9 может увеличивать фиброз путем увеличения количества активного TGF-в в скелетных мышцах мышей MDX.
Генетические абляции MMП-9 улучшают сарколемму и увеличивает клеточный уровни в-дистрогликана и ННО в скелетных мышцах мышей MDX.
Для более глубокого понимания механизмов действия MMП-9 в скелетных мышцах мышей MDX, мы изучали влияние ингибирования ММП-9 иммунными антителами с ламинином на мембрану скелетных мышц (29). По сравнению с четко определенной мембраной каждого мышечного волокна в икроножной мышце от мышей дикого типа, сарколеммы у мышей MDX была морщинистая (рис. 6а). Интересно, что эти нарушения в мышечной оболочке значительно ослабляются у MDX; ММП9 + / - или MDX; ММП9-/ - мыши (рис. 6а, верхние панели). Это явление было также подтверждено электронноммикроскопическим анализом сечения икроножной мышцы. Как показано на рисунке 6а, были значительные улучшения в сарколемме, а также в миофибриллярной структуре в MDX; ММП9 + / - и MDX; ММП9-/ - мышей по сравнению с однопометницами mdx/MМП9 + / + мышей. Эти данные, таким образом, показывают, что увеличение производства MMП-9 вносит свой вклад в нарушения сарколеммы у MDX мышей.
![]()
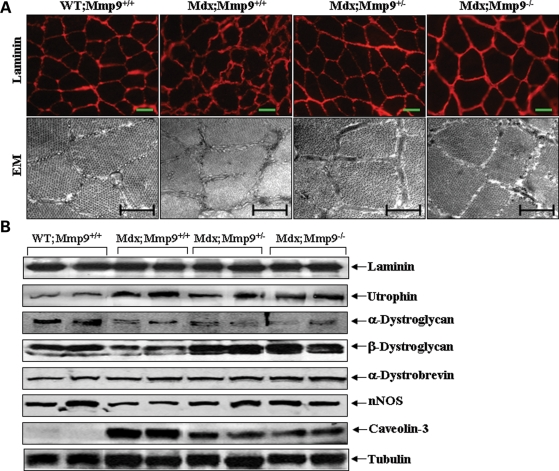
Данные литературы показывают, что, кроме дистрофина, ряд других белков ДГПК страдают в скелетных мышцах мышей MDX (40). Интересно, что недавно было сообщено, что в-дистрогликан является одной из наиболее важных целей протеолитических MMП-9 (41,42). Кроме того, возможно, MMП-9 вызывает деградацию ламинином-2 (13). В соответствии с опубликованным отчетом, мы обнаружили, что увеличились уровни белка атрофина (гомолога дистрофина) и кавеолина-3, а также снижение уровня б-дистрогликана, в-дистрогликана и нервной синтазы окиси азота (NO) у MDX мышей по сравнению с мышами WT ( Рис. 6B). Тем не менее, нет никакой разницы в уровне ламинина, атрофина, б-дистрогликана и б-дистробревина в скелетных мышцах MDX; ММП9 + / +, MDX; ММП9 + / - и MDX; ММП9-/ - мыши (рис. 6В, Верхняя панель). В отличие от этого, уровень белка в-дистрогликана и NО был увеличен, в то время как уровни кавеолина-3 были уменьшены в икроножной мышце MDX; ММП9 + / - и MDX; ММП9-/ - мышей по сравнению с однопометницами MDX; ММП9 + / + мышей (рис. 6б).
Генетические абляции MMП-9 увеличивает регенерацию мышечных волокон у многомерных мышей.
Далее мы исследовали, может ли MMП-9 не иметь никакой роли в регенерации скелетных мышц у многомерных мышей. Регенерация мышечных волокон контролировалась путем подсчета числа централизованно зарождающихся волокон (ЦЗВ) в H & E-окрашенной икроножной мышцы и с антителоми, которые распознают эмбриональные тяжелые цепи миозина (E-MyHC) (Клон F1.652, Банк гибридомы, университет штата Айова). Интересно, что удаление либо одного или обоих аллелей гена ММП9 значительно увеличило количество ЦЗВ в икроножной мышце 8-недельных мышей MDX (рис. 7аи B). Валовой анализ H & E-окрашенных срезов мышц показал, что в то время как mdx/MМП9 + / +, содержащие значительное количество областей, имели некротические волокна, некротические области должны быть заполнены вновь образованными мышечными волокнами, которые были меньше по размеру и имели центральную нуклеацию у mdx/MМП9 + / - и mdx/MМП 9-/- мышей (рис. 7а, выделенной области), что свидетельствует о том, что ингибирование MMП-9 ускоряет регенерацию мышечных волокон. Кроме того, количество E-MyHC окрашенных мышечных волокон было также установлено и резко возросло как у MDX; ММП9 + / - так и MDX; ММП9-/ - мышей по сравнению с однопометницами MDX; ММП9 + / + (рис. 7а и С). Кроме того, мы обнаружили, что уровень Pax-7белка, маркера клеток-сателлитов (43), также был увеличен в икроножной мышце MDX; ММП9 + / - или MDX; ММП9-/ - мышей (рис. 7).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |


