![]()
Фармакологическое ингибирование MMП-9 снижает патологию в скелетных мышцах и увеличивает регенерацию у MDX мышей.
Хотя наши эксперименты с мышами наводят на роль MMП-9 в мышцах многомерных мышей, есть вероятность, что некоторые из очевидных последствий дефицита MMП-9 у мышей MDX могут не отражать измененной физиологии. В целом, результаты, полученные с животными с генетической недостаточностью, которые могут воспроизводятся фармакологическими агентами, предлагают самые сильные доказательства участия каких-либо специфических белков в определенном процессе болезни. (2R) -2 - [(4-бифеннилилсулфонил) амино]-3-фенилпропионовая кислота (также известная как MMП-2/MMП-9 ингибитор I), как известно, специфически ингибирует MMП-9 и при более высокой концентрации ММП-2 тоже (44). Было показано, что он обеспечивает защитный эффект при заболеваниях с участием ММП-9 (44,45). Для дальнейшего подтверждения роли MMП-9 при миопатии, мы исследовали влияние длительного лечения MMП-2/MMП-9 ингибитора на скелетные мышцы в патогенезе MDX мышей. Интересно, что лечение ингибиторами MMП-2/MMП-9 улучшило мышечную структуру (рис. 8А, верхняя панель) и снижение некроза (рис. 8Б, средняя часть) в икроножной мышце MDX мышей. Кроме того, регенерация скелетных мышц видна по увеличению числа CNF (рис. 8) и E-MyHC-положительных волокон (рис. 8Б, нижняя панель и рис.8D). Улучшенние мышц также нашло свое отражение в значительном сокращении КФК в сыворотке крови у мышей MDX при обработке MMП-2/MMП-9 ингибитора I (рис. 8E). Наконец, лечение ингибиторами MMП-2/MMП-9. 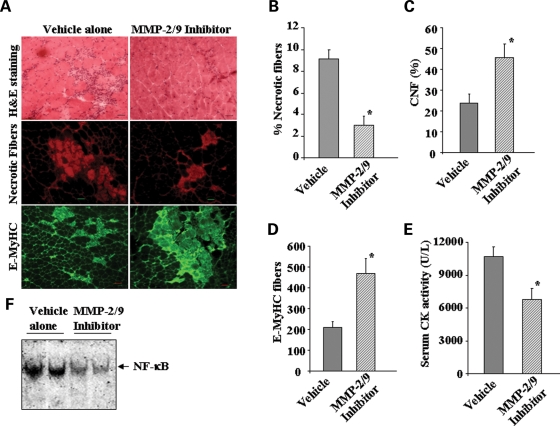
![]()
ОБСУЖДЕНИЕ
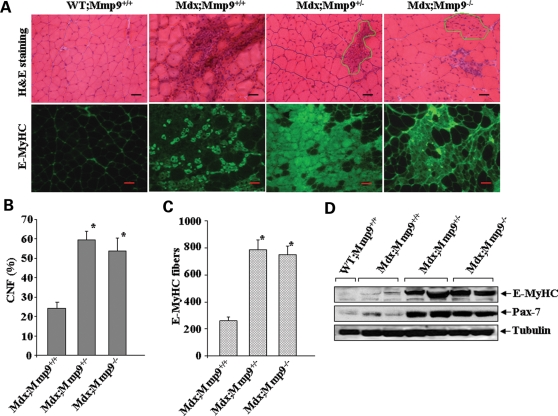
Хотя дистрофин отсутствует при рождении, клинические симптомы не проявляются до 2-3 лет после рождения пациентов с МДД и 2,5 недель у мышей MDX (2-4), что позволяет предположить, что потеря дистрофина приводит к специфическим биохимическим изменениям в скелетных мышцах, что приводит в конечном итоге к увличению повреждения при физической активности. Накопленные данные убедительно показывают, что хроническая воспалительная реакция и фиброз в скелетных мышцах является одними из важных патологических последствий для прогрессивания дисфункции и слабости у пациентов с МДД (5,10,46). В этом исследовании мы определили MMП-9 в качестве важного посредника миопатии у многомерных мышей. Наши данные ясно показывают, что повышенные уровни MMП-9 усугубляют дистрофинопатию путем увеличения некроза волокон, деградации ЭЦМ, воспаления и фиброза. MMП-9 представляет собой один из наиболее важных внеклеточных протеаз, увеличение производства которого может радикально изменить микроокружение скелетных мышц в естественных условиях (19,29,30). В соответствии с установленной ролью MMП-9 в воспалении и восстановлении ЭЦМ, мы обнаружили, что ингибирование MMП-9 значительно улучшает структуру скелетных мышц у мышей MDX (рис. 3D). Кроме того, сывороточный уровень КФК, накопление макрофагов, некроз волокон и повреждение сарколеммы были также резко сокращены после гетерозиготного и гомозиготного удаления гена ММП9 у мышей MDX (рис. 3 иand4) 4) позволяет предположить, что повышенные уровни MMП-9 белка способствуют патологии скелетных мышц у MDX мышей несколькими механизмами (рис. 4). Одним из интригующих аспектов нашего исследования является то, что удаление одного аллеля гена ММП9 было достаточно для снижения уровня белка ММП-9 в скелетных мышцах (рис. 3А) и ослабление патогенеза мышц в большей степени (рис.3 иand4) .4). Резкое сокращение ММП-9 в скелетной мышечной ткани из-за удаления одного аллеля ММП9 у мышей MDX (рис. 3А) предполагает, что ММП-9, регулирующий его собственную экспрессию , возможно, преувеличивал накопление воспалительных клеток и / или увеличивал активность различных провоспалительных молекул. Это утверждение подтверждается нашими данными, которые демонстрируют, что гетерозиготное удаление гена ММП9 значительно ингибирует активацию провоспалительных факторов транскрипции AP-1 и NF-kB (рис. 3В) и уменьшается накопление макрофагов (рис.4А и Б) в дистрофических мышцах MDX мышей. Кроме того, наряду с MMП-9, уровни MMП-2 белка также снизились в скелетных мышцах MDX; ММП9 + / - и MDX; ММП9-/ - мыши (рис. 3А) о том, что ММП-9 также вносит свой вклад в повышение экспрессии MMП-2. Действительно, накопление доказательств наводит на мысль, что есть кооперативное взаимодействие между различными ММП, чтобы способствовать эффективной деградации ткани (11-13). Однако, это также возможно, что уменьшение количества MMП-2 в MDX; ММП9 + / - или MDX; ММП9-/ - мышей является результатом снижения концентрации воспалительных клеток (рис. 4а и б) в дистрофических мышцах многомерных мышей в ответ на ингибирование MMP-9 деятельности. Скелетные мышцы пациентов с МДД и MDX мышей показывают рост соединительной ткани между мышечными волокнами (фиброз) и жировую инфильтрацию (36-38). Диафрагма мышей MDX является первой мышцой, обладающей прогрессирующей дегенерацией, фиброзом и функциональной недостаточности аналогичной тому, которое наблюдалось в ММД мышцах (47,48). Тем не менее, основные механизмы, приводящие к накоплению компонентов матрицы в дистрофических мышцах, остаются плохо понятыми. Общее мнение состоит в том, что снижение стабильности мышечных волокон, в связи с отсутствием дистрофина, приводит к дегенерации мышечных волокон и последующему вторжению в мышечные ткани воспалительных клеток, таких как макрофаги, нейтрофилы и Т-лимфоциты, что повышает фиброз (48,49) . В самом деле, истощение макрофагов и лимфоцитов приводит к снижению дегенерации мышц и фиброза у мышей MDX (34,49,50). Интересно, что MMП-9 является одним из наиболее важных медиаторов воспаления и сильно вовлечены в реконструкцию ЭЦМ, что приводит к фиброзу и в ряде других тканей (51,52). MMП-9 также участвует в обработке протеолитическими провоспалительными цитокинами, в том числе регуляции и активации TGF-в (13,39), главный медиатор фиброза при дистрофинопатии (38). Наши результаты демонстрируют значительное снижение активности AP-1 и NF-kB транскрипционных факторов, и снижение концентрации воспалительных клеток (рис. 3C и and4A4A и B) с сопутствующим снижением фиброза (рис.5A-C) в MDX; ММП9 + / - иMDX; ММП9-/ - мыши убедительно свидетельствуют, что ММП-9 вносит свой вклад в накопление фиброзной ткани у MDX мышей. Кроме того, уровень активного TGF-в белка также значительно снижается в скелетных мышцах MDX; ММП9 + / - или MDX; ММП9-/ - мыши (рис. 5D) о том, что ММП-9 участвует в протеолитической обработке латентных TGF-в в активную форму в дистрофических мышцах. Хотя точные механизмы, посредством которых MMП-9 вызывает патологию мышц, могут быть довольно сложными. Наши результаты показывают, что повышение протеолиза конкретных компонентов цитоскелета ЭЦМ-сети является одним из потенциальных механизмов, с помощью которых MMП-9 усиливают патологию. Это утверждение опирается на наши данные, демонстрирующие, что структура сарколеммы была значительно улучшена в скелетных мышцах MDX; ММП9 + / - или MDX; ММП9-/ - мышей по сравнению с MDX; ММП9 + / + мышей (рис. 6а). Кроме того, генетические абляции ММП-9 у мышей MDX также увеличили уровни белка коллагена IV (рис. 5), в-дистрогликана и NО (рис.6В) без влияющих на уровни ряда других ДГПК-родственных белков (рис. 6б). Так как коллаген IV и б-дистрогликан являются известными физиологическими субстратами MMП-9 (12,13,41), их повышенный уровень у MDX; ММП9 + / - и MDX; ММП9-/ - является ожидаемым. Тем не менее, остается загадкой как MMП-9 торможение увеличивает уровни белка NО в мышечных волокнах многомерных мышей. Кроме того, мы обнаружили, что генетическая
![]()
абляция MMП-9 снижает уровень кавеолина-3 (белок малого молекулярного веса локализованый в сарколемме) в скелетных мышцах мышей MDX (рис. 6б). Интересно, что кавеолин-3 непосредственно взаимодействует с NО и подавляет его каталитическую активность (53). Кроме того, как снижение уровня белка NО (26) и повышенная экспрессия кавеолинf-3 (54,55) связана с патогенезом скелетных мышц у MDX мышей. В совокупности эти результаты позволяют предположить, что помимо непосредственно вызваного протеолиза конкретных ЭЦМ-белков цитоскелета, повышенные уровни MMП-9 могут также вызвать патогенез косвенных механизмов, которые включают в себя изменение в уровнях белка. Интересное наблюдение настоящего исследования – генетическая абляция или фармакологическое ингибирование ММП-9 значительно улучшило регенерацию скелетных мышц у мышей MDX (рис. 7,and8) .8). Кроме того, экспрессия Pax-7, специфического маркера клеточной поверхности для клеток-сателлитов (43), была значительно увеличена в скелетных мышцах MDX; ММП9 + / - и MDX; ММП9-/ - мышей по сравнению с MDX; ММП9 + / + мышей (рис. 7D) о том, что расширение регенерации мышечных волокон стало результатом увеличения спутниковых клеток. Несмотря на истощение клеток-сателлитов из-за чрезмерной активации циклов дегенерации и регенерации была предложена в качестве основных причин недостаточной регенерации мышечных волокон при ММД (4,56), утрата регенерационной способности при ММД также может быть связана с другими факторами, такими как прогрессивное увеличение мышечного интерстициального фиброза, который может помешать наличию факторов роста и миграции миогенных клеток, необходимых для формирования миофибрилл (57,58). Увеличение количества провоспалительных цитокинов, таких как TNF-б и IL-1в, которые находятся в дистрофических мышцах(6,27), могут также ингибировать слияние миобластов в поврежденных мышечных волокнах. Кроме того, поскольку базальная мембрана имеет важное значение для скелетных мышц и регенерации формирования нервно-мышечных соединений (59), обширная деградация базальной мембраны мышечных волокон в дистрофических тканях также может повлиять на способность скелетных мышц к регенерации. В недавнем докладе также предполагается, что увеличение активации NF-kB вмешивается в регенерацию скелетных мышц у мышей MDX (27). Потому что ингибирование MMП-9 значительно ингибирует активность воспалительного ответа (рис. 3 иand4A4Aи B), фиброз (рис. 5) и активацию NF-kB фактора (рис.3В иand8F), 8F), и ослабление аномалий мембраны мышечных волокон (рис. 6а), увеличивая регенерацию скелетных мышц у MDX; ММП9 + / - и MDX; ММП9-/ - мышей может быть результатом некоторых из этих эффектов ингибирования ММП-9.Недавние сообщения нашей и других групп показывают, что деятельность различных провоспалительных факторов транскрипции, таких как NF-kB и АР-1 значительно повышены в скелетных мышцах мышей MDX (6,7,27). Кроме того, фармакологические или генетические ингибирование NF-kB, как сообщалось, ослабление патогенеза скелетных мышц у мышей MDX (27). Мы также показали, что экспрессия ММП-9 в ответ на различные провоспалительные цитокины осуществляется с помощью транскрипционной активации NF-kB и АР-1 в скелетной мышце (29,30). Кроме того, наши данные показывают, что в естественных условиях лечение ингибиторами NF-kB (т. е. NBD) уменьшает количество MMП-9 белка в скелетных мышцах мышей MDX (рис. 2). Интересно, что Ачарья и соавт. (27) недавно сообщили, что в естественных условиях лечение NBD-пептидом предотвращает мышечную патологию и улучшает регенерацию скелетных мышц у MDX мышей. Поскольку MMП-9 является видным регулируемым геном NF-kB (28), вполне возможно, что NF-kB вызывает патологию мышц у мышей MDX через повышение экспрессии ММП-9 белка. Активация NF-kB (6,27) и уровня ММП-9 белка (рис. 1В)остаются повышенными после 2 недель у мышей MDX; (II) генетическое или фармакологическое ингибирование либо NF-kB (27) или ММП-9 (рис. 3,, 44 иand8) 8) ингибирует различне параметры скелетных мышц, такие как некроз волокон и воспаления у MDX мышей, и (III) ингибирование либо NF-kB (27) или ММП-9 (рис. 7,and8) 8) улучшает регенерацию скелетных мышц у MDX мышей. В более раннем исследовании, Чен и соавт. (60) сообщили, что NF-kB сильно индуцируется в скелетных мышцах пациентов с МДД сразу после рождения. Тем не менее, на более поздних стадиях развития болезни, активация TGF-в увеличивается (60) о том, что активированный NF-kB может активировать TGF-в пути за счет повышения экспрессии ММП-9, который преобразует скрытые TGF-в в активной форме (13).Таким образом, наше исследование предоставляет убедительные доказательства того, что увеличение производства MMП-9 вносит свой вклад в скелетные мышцы в патогенезе дистрофин-дефицитных скелетных мышц. Основываясь на результатах этого исследования, которое показывает, что даже частичное ингибирование MMП-9 эффективно снижает активность скелетных мышц в патогенезе MDX мышей, мы считаем, что ММП-9 будет служить важной молекулярной мишенью для смягчения повреждения скелетных мышц в патогенезе пациентов МДД в будущем.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |


