Блокада матричной металлопротеиназы-9 улучшает регенерацию скелетных мышц при мышечной дистрофии

Блокада матричной металлопротеиназы-9 улучшает регенерацию скелетных мышц при мышечной дистрофии
ВВЕДЕНИЕ
Мышечная дистрофия Дюшенна (МДД) является одним из наиболее распространенных и смертельных форм мышечной дистрофии, которая поражает 0,03% всех новорожденных мальчиков (1). Инактивация гена дистрофина является основной причиной МДД у людей и мышей MDX (мышиной модели МДД) (2-4). Дистрофин является неотъемлемым компонентом комплекса трансмембранных белков, известного как дистрофина-гликопротеиновый комплекс (ДГК), который не только обеспечивает механическую стабильность мышечных волокон во время сокращения, но и служит важным звеном сигнализации от внеклеточного матрикса (ЭЦM) на цитоскелет ( 5). Потеря функционального белка дистрофина приводит к большей механической нестабильности сарколеммы и аберрантной внутриклеточной сигнализации, что ведет к прогрессирующей дегенерации мышц и слабости (5-8). Хотя скелетные мышцы имеют замечательную способность к регенерации после травмы, регенерации мышечных волокон значительно снижается при МДД (2,9). Накопленные данные наводит на мысль, что основной дефицит дистрофина приводит к активации ряда вторичных процессов, таких как воспаление, деградации ЭЦМ, хронической дегенерации и регенерации волокон и фиброзу, которые усугубляют прогрессирование заболевания (1). Лучшее понимание и управление этими вторичными процессами даст огромный потенциал для улучшения качества жизни и продления жизни пациентов с МДД (10).Матричные металлопротеиназы (ММП) представляют собой семейство цинк-содержащих ферментов, которые участвуют в деградации и реконструкции компонентов ЭЦМ как в физиологических, так и при патофизиологических условиях (11,12). Эти протеазы синтезируются в виде секретируемых и трансмембранных проферментов и обрабатываются в активную форму путем удаления амино-терминального пропептида. Экспрессия ММП быстро увеличивается на повреждение тканей, предлагая их возможную роль в процессе восстановления, высвобождения факторов роста и модуляции ЭЦМ для миграции клеток (11-13). Однако, наличие большого количества ММП, и, в частности MMП-9 (желатиназа B), вносит свой вклад в разрушение тканей при многих патологических состояниях, в том числе хронических ранах, сердечной недостаточности, ревматоидном артрите, фиброзе легких, дилатационной кардиомиопатии, язвенной болезни желудка, рассеянном склерозе, астме и раке (13-18). Протеолитическая активность ММП жестко контролируется их взаимодействием с эндогенными тканевыми ингибиторами матричных металлопротеиназ (ТИМП), которые специфично ингибируют активные формы ММП и в некоторых случаях неактивные ММП (11-13). Баланс между ММП и ТИМП играет важную роль в поддержании целостности тканей (13). Повышенные уровни MMП-9 были обнаружены в скелетной мышечной ткани после повреждения нерва, сердечной недостаточности и воспалительных миопатиях (19-22). Кроме того, фармакологическое ингибирование активности ММП было использовано для ослабления патогенеза у мышиной модели окулофарингеальной мышечной дистрофии (23). Несмотря на то, что MMП-9, по-видимому, играет важную роль в ремоделировании скелетных мышц при различных патологических состояниях, прямых доказательств в отношении роли MMП-9 в патологии скелетных мышц до сих пор нет. В этом исследовании, с помощью генетических и фармакологических подходов, мы исследовали роль и лежащие в основе механизмы, с помощью которых увеличивается производство MMП-9, как причины развития патологии мышц у мышей MDX. Наши исследования показывают, что ингибирование MMП-9 резко снижает структурное ухудшение скелетных мышц, воспаление, некроз и фиброз и повышает сократительную функцию скелетных мышц у MDX мышей. Кроме того, ингибирование MMП-9 также значительно улучшает регенерацию скелетных мышц у MDX мышей.
РЕЗУЛЬТАТЫ
Дерегулирование экспрессии MMП-9 во время постнатального развития MDX мышей.
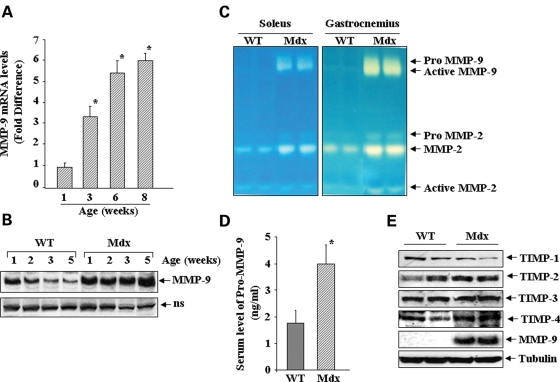
Сначала мы изучали мРНК и уровни MMП-9 в мышцах диафрагмы нормальных и MDX мышей количественным ПЦР в реальном времени (QRT-PCR) и вестерн-блоттом. Уровни мРНК MMП-9 оказались значительно выше в мышцах диафрагмы у 3 -, 6 - и 8-недельных MDX мышей по сравнению с соответствующего возраста C57BL/10 контрольными мышами (рис. 1А). Несмотря на то, что повышенные уровни MMП-9 наблюдалось в контрольной группе и MDX мышей через 1 или 2 недели после рождения, содержание MMП-9 белков значительно снижается через 2 недели у контрольных мышей. В отличие от этого, уровни MMП-9 белка остаются аномально высокими в диафрагме 3 - и 5-недельных мышей MDX (рис. 1б). Чтобы оценить обладает ли MMП-9 в скелетных мышцах мышей MDX ферментативной активностью, желатиновая зимография была выполнена. Резкое увеличение разжижающей желатин активности MMП-9 наблюдалась в камбаловидной и икроножной мышце 8-недельных мышей MDX по сравнению с соответствующим возрастом контрольных мышей (рис. 1в).Похожее увеличение уровня MМП-9 и разжижающей желатин активности наблюдалась в диафрагме, камбаловидной, икроножной и четырехглавой мышце (данные не показаны). Кроме того, количество MMП-2 несколько увеличивается в скелетных мышцах мышей MDX (рис. 1в). Эти данные согласуются с другими опубликованными отчетами, подтверждающими повышение уровня ММП-9 в скелетных мышцах мышей MDX (24,25). Мы также сравнили уровни MMП-9 в сыворотке контроля и MDX мышей с использованием коммерчески доступных ИФА (R & D Systems). Как показано на рисунке 1D, обнаружено примерно 2-кратное увеличение в сыворотке крови уровня ММП-9 у 6-недельных мышей MDX по сравнению с соответствующими по возрасту контрольными мышами (рис. 1D). Кроме того, поскольку протеолитическая активность MMП-9 регулируется с помощью их взаимодействия с TIMPs (11-13), мы также исследовали, может ли экспрессия TIMP изменяться в скелетных мышцах MDX мышей по сравнению с контрольными мышами. Не существовало никаких существенных различий в уровнях TIMP-1, -2, -3, -4 между 8-недельными мышами контроля и MDX (рис. 1E), что свидетельствует о нарушении баланса между ММП-9 и TIMP в скелетных мышцах мышей MDX.
Поскольку дистрофические мышцы мышей MDX содержат иммунные клетки - макрофаги (26,27), мы исследовали, может ли MMP-9 производится скелетными мышцами, макрофагами, или и теми и другими. Криосекции скелетных мышц икроножной мышцы мышей MDX были подвергнуты иммунному окрашиванию для MMP-9 и CD68 (маркер клеточной поверхности для активированных макрофагов). Ядра окрашивали 4 ',6-диамидино-2-фенилиндола (DAPI). MMП-9 увеличен в областях, где концентрация макрофагов была выше (рис. 2). Для дальнейшего подтверждения роли иммуноцитов в экспрессии MMП-9 у MDX мышей, мы измерили MMП-9 белка в других иммунных (например, селезенке и тимусе) и не иммунных (например, печени) органах 8-недельных контрольных и MDX мышей. Интересно, что в дополнение к скелетным мышцам, уровень ММП-9 также значительно увеличился в селезенке и вилочковой железе, но не в печени мышей MDX (рис. 2В).
![]()
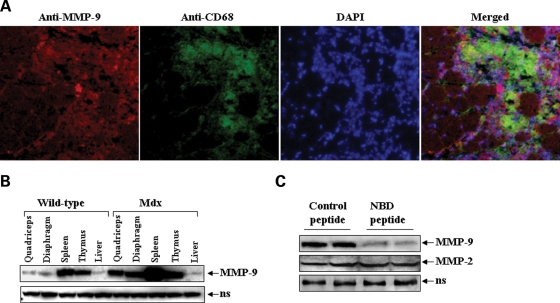
Ранее мы уже сообщали о том, что активность ядерного фактора каппа-В (NF-kB) регулируется в скелетных мышцах мышей MDX (6). Поскольку промоторная область MMП-9 содержит обязательную последовательность для NF-kB, а активация NF-kB является необходимым условием для экспрессии MMП-9 в ответ на различные раздражители (28-30), мы исследовали, может ли активация NF-kB отвечать за повышенную экспрессию MMП-9 в скелетных мышцах мышей MDX. Как показано на рисунке 2C, в естественных условиях клетки проницаемы для NF-kB модификатора (NEMO)-связывающего домен(NBD) пептида, селективного ингибитора NF-kB (27,31), значительно сократили объемы MMП-9 белка в диафрагме MDX мышей. В отличие от лечения NBD пептидом, которое не влияют на уровень MMП в скелетных мышцах мышей MDX (рис. 2). Взятые вместе, эти результаты показывают, что скелетные мышцы и иммуноциты (например, макрофаги) вносят вклад в повышение уровня ММП-9 и экспрессия MMП-9 регулируется путем активации NF-kB в скелетных мышцах мышей MDX. Генетическая абляция MMП-9 ингибирует активацию фактора активатора протеина-1 (AP-1) и NF-kB транскрипцию, снижает сывороточный уровень креатинкиназы (КФK) и улучшает структуру скелетных мышц мышей MDX. Для того чтобы понять роль ММП-9 в патогенезе мышей MDX, мужские особи ММП9-нокаутных мышей были скрещены с самками мышей MDX для создания многомерных + / -; ММП9 + / - и MDX; ММП9 + / - мышей. Выполняя вестерн-блоттинг, мы впервые подтвердили, что удаление одного аллеля ММП9 (т. е. в Mdx; ММР9 + / -) снизило уровни белка ММП-9 в скелетных мышцах MDX мышей и не было обнаружено уровня ММП-9 белка у MDX; ММП9-/ - мыши (рис. 3А). Интересно, что вместо ожидаемого 50% снижения, удаление одного аллеля MMП-9 (т. е. MDX; ММР9 + / -) более резко (> 80%) снизило уровень ММП-9 белка в скелетных мышцах мышей MDX. Кроме того, уровень ММП белка также приводит к снижению у MDX; ММП9 + / - или MDX; ММП9-/ - мышей по сравнению с MDX; ММП9 + / + мышей (рис. 3А),о том, что увеличение производства MMП-9 также модулирует экспрессию / деятельность других ММП в скелетных мышцах мышей MDX. Опубликованные доклады свидетельствуют о том, что, кроме NF-kB, транскрипционная активация промоутера ММП-9 также включает в себя активацию активатора протеина-1 (AP-1) (28-30). Мы исследовали возможность того, что MMП-9 влияет на его собственную экспрессию в скелетных мышцах мышей MDX через положительную обратную связь, которая может включать в себя активацию АР-1 и NF-kB. Интересно, что активация и AP-1 и NF-kB была значительно снижена в передней большеберцовой мышце (TA) MDX; ММП9 + / - или MDX; ММП9-/ - мышей по сравнению с MDX; ММП9 + / + мышей (рис. 3В) .

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |


