На правах рукописи
СЯ ЮЙ
ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ В АНАЛИЗЕ ВОДОРАСТВОРИМЫХ ВИТАМИНОВ
(СРАВНИТЕЛЬНАЯ ОЦЕНКА)
14.04.02 – фармацевтическая химия, фармакогнозия
Автореферат
диссертации на соискание ученой степени
кандидата фармацевтических наук
Москва – 2010
Работа выполнена в ГОУ ВПО Первый Московский государственный медицинский университет имени
Научные руководители:
доктор фармацевтических наук, академик РАМН, профессор
доктор фармацевтических наук, профессор
Официальные оппоненты:
доктор фармацевтических наук, профессор
доктор фармацевтических наук, профессор
Ведущая организация:
Научно-исследовательский институт фармакологии имени РАМН
Защита состоится «______»_________________2010 г. в _____ часов на заседании Диссертационного совета (Д 208.040.09) при Первом Московском государственном медицинском университете имени Москва, Никитский бульвар, 13.
С диссертацией можно ознакомиться в библиотеке Первого МГМУ им. Москва, Нахимовский проспект, 49.
Автореферат разослан «______»_________________ 2010 г.
Ученый секретарь диссертационного
совета Д 208.040.09
доктор фармацевтических наук,
профессор
Общая характеристика работы
Актуальность темы. Возрастающие требования к безопасности, эффективно-сти и качеству лекарственных средств обусловливают необходимость разрабатывать новые и совершенствовать существующие методы их анализа.
Витамины являются незаменимыми веществами, необходимыми для роста, развития и жизнедеятельности человека. Большинство витаминов в организме не синтезируется, источником их обычно является внешняя среда. Традиционно разли-чают водорастворимые и жирорастворимые витамины.
Витаминные препараты широко используютсят для стимуляции и регуляции физиологических процессов, профилактики и лечения ряда заболеваний при гипо - и авитаминозах, повышения общей устойчивости организма к экзогенным и эндоген-ным неблагоприятным факторам.
На сегодняшний день рынок переполнен витаминными препаратами, они имеют различные составные элементы и выпускаются в разных лекарственных формах. На фармацевтическом рынке существует большое количество дженериков или многоисточниковых препаратов, содержащих витамины.
Качество препаратов-дженериков обеспечивается комплексом аналитических методов, позволяющих подтвердить их подлинность, определить чистоту и количе-ственное содержание действующего вещества. Используемые для этого методы и методики нуждаются в постоянном совершенствовании. Необходимо также учиты-вать сохраняюшуюся проблему фальсификации лекарственных средств. Учитывая вышеизложенное, актуальной является проблеме сравнительного изучения физико-химических методов, используемых для анализа лекарственных средств водораство-римых витаминов.
Цель и задачи исследования. Целью исследования являлось сравнительное изучение современных физико-химических методов анализа лекарственных средств водорастворимых витаминов.
Для достижения поставленной цели решали следующие задачи:
- провести анализ состояния методов стандартизации и контроля качества лекарственных средств, включая международные программы и зарубежные фармакопеи;
- разработать унифицированную методику анализа субстануий и препаратов во-дорастворимых витаминов методом БИК-спектроскопии в средней области и составить атлас БИК-спектров;
- разработать методики устоновления подлинности и количественного опреде-ления субстанций и препаратов водорастворимых витаминов методами ИК-спектроскопии в ближней областях;
- разработать методики устоновления подлинности и количественного опреде-ления лекарственных средств водорастворимых витаминов методами УФ-спектроскопии;
- изучить хроматографические характеристики и разработать унифицированную методику установления подлинности водорастворимых витаминов методом
ТСХ;
- изучить хроматографические характеристики и разработать методику уста-новления подлинности и количественного определения витаминов группы В методом ВЭЖХ.
Научная новизна исследования. Составлен атлас ИК-спектров субстанций и лекарственных препаратов водорастворимых витаминов различных производителей в вазелиновом масле. Изучены спектральные характеристики лекарственных средств кислоты аскорбиновой в средней и ближней инфракрасных областях.
Показана возможность использования метода БИК-спектроскопии для устано-вления подлинности субстанций и препаратов кислоты аскорбиновой.
Построены модели для таблеток кислоты аскорбиновой, позволяющие иденти-фицировать производителя субстанции или препарата методом БИК-спектроскопии.
Впервые построена калибровочная модель, позволяющая определять процент-ное содержание кислоты аскорбиновой в таблетках методом БИК-спектроскопии. Установлено, что при идентификации и количественном определении таблеток кис-лоты аскорбиновой методом БИК-спектроскопии, содержащие действующего веще-ства в них должно составлять не менее 25%.
Впервые разработаны унифицированные методики установления подлинности тиамина гидрохлорида, рибофлавина, пиридоксина гидрохлорида, никотинамида и фолиевой кислоты методами ТСХ и ВЭЖХ.
Разработаны методики пробоподготовки субстанций и лекарственных препа-ратов водорастворимых витаминов для анализа методами ТСХ и ВЭЖХ. Изучено влияние подвижных фаз различного состава на хроматографические характеристики водорастворимых витаминов при их анализе данными методами.
Предложены новые условия подтверждения подлинности водорастворимых витаминов в субстанциях и лекарственных препаратах с использованием российских пластин «Сорбфил» для высокоэффективной тонкослойной хроматографии.
Практическая значимость работы. Полученные ИК-спектры в средней и ближней областях и УФ-спектры могут быть использованы при стандартизции и контроле качества по разделу «подлинность» соответствующей НД на субстанции и лекарственные препараты водорастворимых витаминов.
Методики установления подлинности и количественного определения мето-дами УФ - и БИК-спектрофотометрии, методика установления подлинности водо-растворимых витаминов методами ТСХ и ВЭЖХ предлагаются для стандартизации и контроля качества субстанций и лекарственных препаратов данной группы лекар-ственных средств с последующим их включением в соответствующие разделы НД.
Разработанные методики внедрены и используютсяв испытательной лаборатории Московского областного центра сертификациии контроля качества лекарственных средств (акт внедрения от 10 июня 2010 г.).
Апробация работы. Основные положения диссертационной работы доло-жены и обсуждены на XVII Российском национальном конгрессе «Человек и лекарство» (Москва, 2010 г.). Апробация работы проведена на научнопрактическом заседании кафедры фармацевтической химии с курсом токсикологической химии фармацевтического факультета Первого МГМУ им. 14 июня 2010 г.
Публикации. По материалам диссертации опубликовано 4 печатных работ.
Связь исследований с проблемным планом фармацевтических наук. Диссертационная работа выполнена в рамках комплексной темы кафедры фармацев-тической химии Первого МГМУ им. «Совершенствование контроля качества лекарственных средств» (гос. регистрация № 01.200.110545).
Объем и структура диссертации. Диссертация изложена на 141 страницах машинописного текста (без приложения) и состоит из введения, обзора литературы, экспериментальной части (материалы и методы, результаты исследования и их обсуждение), выводов, списка литературы, а также отдельно включает в себя 3 приложения. Работа иллюстрирована 31 таблицами и 30 рисунками. Библиографиче-ский указатель литературы включает 115 источников, из них 74 − иностранные.
Основные положения, выносимые на защиту.
- результаты исследования лекарственных субстанций и препаратов водораство-римых витаминов методом ИК-спектроскопии в средней области;
- результаты прменения ИК-спектроскопии в ближнем диапазоне для идентифи-кации и количественного определения лекарственных средств водораствори-мых витаминов;
- результаты исследования водорастворимых витаминов методами УФ-спектро-фотометрии;
- результаты изучения водорастворимых витаминов методами ТСХ и ВЭЖХ.
Содержание работы
1. ОБЪЕКТЫ ИССЛЕДОВАНИЯ
Объектами исследования являлись стандартные образцы, субстанции и препа-раты водорастворимых витаминов, зарегистрированных в РФ.
Табл. 1. Изучаемые водорастворимые витамины.
Фармацевтическая субстанция | Структурная формула | Химическое название, молекулярная формула, М. м. |
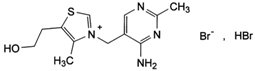
Тиамина гидробромид Thiamine Hydrobromide |
| 3-[(4-амино-2-метил-5- пиримидинил)метил]-5- (2-гидроксиэтил)-4-метил-тиазолий бромид гидробромид C12H17BrN4OS∙HBr М. м. 426,2 |
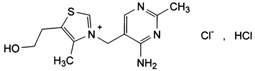
Тиамина гидрохлорид Thiamine Hydrochloride |
| 3-[(4-амино-2-метил-5- пиримидинил)метил]-5- (2-гидроксиэтил)-4-метил-тиазолий хлорид гидрохлорид C12H17ClN4OS∙HCl М. м. 337,3 |
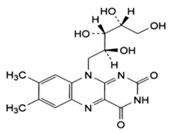
Рибофлавин Riboflavin |
| 7,8-диметил-10-(D-1-рибитил) изоаллоксазин C17H20N4O6 М. м. 376,4 |
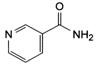
Никотинамид Nicotinamide |
| 3-пиридинкарбоксамид C6H6N2O М. м. 122.1 |
Пиридоксина гидрохлорид Pyridoxine Hydrochloride |
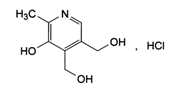
| 4,5-бис(гидроксиметил)-2-метилпиридин-3-ола гидрохлорид C8H11NO3∙HCl М. м. 205,6 |
Табл. 1. Изучаемые водорастворимые витамины (продолжение).
Фолиевая кислота Folic acid |
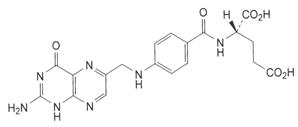
| N-{n-[(2-амид-4-гидроксиокси -6-птеридинил)метил]-амино}-бензоил-L глутаминовая кислота C19H19N7O6 М. м. 441.4 |
Аскорбиновая кислота Ascorbic acid |
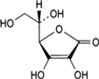
| (5R)-5-[(1S)-1,2-дигидроксиэтил]-2,3-дигидроксифуран-2(5H)-он C6H8O6 М. м. 176,1 |
2. ОБОРУДОВАНИЕ И УСЛОВИЯ ИСПЫТАНИЙ
2.1 иК-СПЕКТРОСКОПИЯ
В работе использовали однолучевой интерференционный (с обратным пре-образованием Фурье) ИК-спектрофотометр Инфралюм ФТ-02 (НПФ «ЛЮМЭКС», Россия). Параметры записи спектров: диапазон cm-1, разрешение 1 cm-1, циклическая запись с количеством сканов 20, аподизация стандартная. Фоновый спектр (воздух) получали непосредственно перед записью каждого спектра.
Управление прибором и обработку спектров осуществляли с использованием программы «Спектралюм» (НПФ «ЛЮМЭКС», Россия) и программы «OPUS», Version 6.0 (Bruker Optics, Германия).
Пробоподготовку субстанций осуществляли в соответствии с требованиями ГФ XII. Навеску субстанции массой 15 мг измельчали в агатовой ступке и растирали с 1-2 каплями вазелинового масла качества «для ИК-спектроскопии». Полученную пасту наносили между двумя пластинками из KBr и получали ИК-спектр образца.
Пробоподготовку таблеток осуществляли путем предварительного извлечения кислоты аскорбиновой из препаратов спиртом 96%, высушивания при 30ºС и расти-рания полученного извлечения с вазелиновым маслом качества «для ИК-спектроско-пии». Полученную пасту наносили между двумя пластинками из KBr и получали ИК-спектр образца.
Интерпретацию спектров проводили с применением ИК-базы данных, доступ-ной в режиме online на сайте Spectral Database for Organic Compounds SDBS (National Institute of Advanced Industrial Science and Technology, Japan) по адресу:
http://riodb01.ibase. aist. go. jp/sdbs/cgi-bin/cre_index. cgi? lang=eng
2.2 БиК-СПЕКТРОСКОПИЯ
Исследования были проведены на приборе ИК-Фурье спектрометр Antaris II фирмы Thermo Electron Corporation (США) с интегрирующей сферой; разрешение – 8 см-1, количество сканирований 16, область измерения от 4000 до 10000 см-1, базовую линию проводили по эталону из тефлона, количество сканирований – 32. Время анализа – 2 минуты, что включает снятие спектра встроенного в прибор эталона (образца сравнения), снятие спектра анализируемого образцах, и обработку полученных данных при помощи внешнего компьютера. Фоновый спектр (воздух) получали непосредственно перед записью каждой группы спектров различных про-изводителей.
Субстанцию слоем 4-6 мм в специальной кювете с закрытой крышкой поме-щали на интегрирующую сферу и снимали спектр не менее трех раз для каждого об-разца, перемешивая его перед каждым измерением. Таблетку помещали на интегри-рующую сферу, фиксировали с помощью специального устройства и снимали спектр. Анализировали 10 таблеток препарата, измеряя каждую таблетку не менее трех раз с двух сторон.
Обработку результатов проводили хемометрическим методом с помощью про-граммы «Thermo Scientific TQ AnalystTM». Обработка БИК-спектров основана на сочетании спектроскопии и статистического метода анализа многофакторных зави-симостей.
2.3 УФ-СПЕКТРОФОТОМЕТРИЯ
В работе использовали двухлучевой спектрофотометр UV1901 (Китай). Полу-чали спектр в диапазоне длин волн от 200 до 400 нм. В качестве раствора сравнения использовали соответствующий растворитель.
Обработку спектров осуществляли с использованием программы «UVWIN 5 Spectrophotometer Software for Windows System» (Китай).
2.4 ТОНКОСЛОЙНАЯ ХРОМАТОГРАФИЯ
Хроматографирование проводилось на пластинах для высокоэффективной ТСХ «Сорбфил» размером 10×10 см (ТУ , , г. Краснодар), покрытых силикагелем, с люминофорным содержаемым. Пластины были представлены двумя видами, отличающимися между собой материалом подложки: алюминиевая фольга (ПТСХ-АФ-В-УФ). Также использовали пластины Silica gel 60 HF254 (0,25 mm) Merck размером 10×20 см (вырезали 10×10 см).
На линию старта пластин с помощью микрошприца наносили 2 мкл раствора сравнения и испытуемого раствора. Пробы наносили таким образом, чтобы расстоя-ние от места нанесения до левого или правого края пластины, а также между пят-нами составляло не менее 2 см. Сушку проб осуществляли с помощью нагреватель-ного устройства для сушки пластины УСП-1 (, г. Краснодар) при температуре около 50ºС. Использовали стеклянную хроматографическую каме-ру размером 150×120×80 мм. Насыщение камеры парами подвижной фазы (ПФ) проводили в течение 20-30 мин.
Пробег фронта растворителя составлял 8,5 см. Проявление пятен водораство-римых витаминов проводили под УФ-лампой при длинах волн 254 и 365 нм (УФС 254/365, , г. Краснодар) после высушивания хроматографи-ческой пластинки в сушильную шкафу при температуре 100ºС в течение 5 мин.
2.5 ВЫСОКОЭФФЕКТИВНАЯ ЖИДКОСТНАЯ ХРОМАТОГРАФИЯ
Исследование проводили в условиях обращенно-фазовой ВЭЖХ. В работе использовали градиентный ВЭЖХ храматограф Vertex Model 500 (США). Колонка SinoChrom ODS-BP (4,6 мм × 200 мм, С18, 5 мкм). Температура колонки 30ºС. Скорость потока 1,0 мл/мин. Объем пробы 20 мкл. Детектирование при длине волны 254 нм.
Управление прибором и расчет хроматографических параметров осуществ-ляли с использованием программы «N2000 Chrom» (Getto Tech., Китай).
3. РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
3.1 иК-СПЕКТРОСКОПИЯ
3.1.1. Анализ ИК-спектров водорастворимых витаминов
Было проведено исследование водорастворимых витаминов с использованием метода ИК-спектроскопии. Пробоподготовку осуществляли путем диспергирования испытуемых лекарственных веществ в вазелиновом масле.
На рис. 1 в качестве примера представлен ИК-спектр кислоты аскорбиновой. В изучаемых спектрах полосы около 2955, 2924, 2855 см−1 соответствуют валентным колебаниям νС-Н, 1462, 1378 и 722 см−1 – деформационным колебаниям δС-Н вазели-нового масла. Полосы с частотами около 2361, 2346, 2334 и 666 см−1 соответствует колебаниям присутствующего в атмосфере углекислого газа.
На основании анализа спектров субстанции кислоты аскорбиновой имею-щихся в нашем распоряжении серий и производителей были выделены следующие характеристических полосы поглощения: νС=О в γ-бутиролактоне (1755 см−1), νС=С (1675 см−1), νas(С-О-С) (1322 см−1) и νs(С-О-С) (1026 см−1).
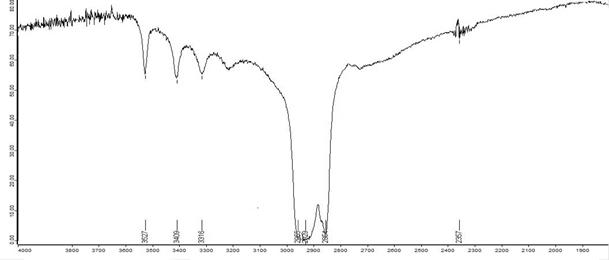

Рис.1. ИК-спектр субстанции кислоты аскорбиновой в вазелиновом масле.
3.1.2. ИК-спектры препаратов водорастворимых витаминов
В данной работе также решалась задача получения ИК-спектров водораство-римых витаминов в готовых лекарственных формах без предварительного извлече-ния действующего вещества. Нами было показано на примере кислоты аскорбино-вой (рис.2), что при достаточно большом содержании действующего вещества в ле-карственной форме «таблетки» (не менее 30-40%) можно получать ИК-спектр, на котором видны практически все полосы поглощения активной субстанции. При от-носительно высоком содержании активной субстанции в препарате ИК-спектр мож-но получать напрямую – вспомогательные вещества не искажают картину и не мас-кируют полосы действующего вещества.

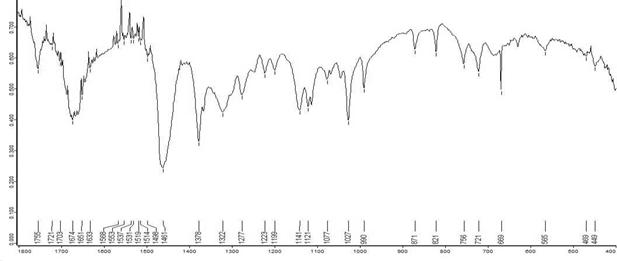
Рис.2. ИК-спектр таблеток Витамин С в вазелиновом масле (Nanjing Baijingyu Pharm, Китай).
Из рис. 1 и 2 видно, что ИК-спектры субстации и таблеток Витамин С (Nanjing Baijingyu Pharm, Китай) различают крайне незначительно – практически совпадают. Аналогичная ситуация наблюдается и для других водорастворимых витаминов. При этом содержание действующего вещества в таблетках кислоты аскорбиновой состав-ляет в среднем около 67%.
Дальнейшие исследования методик непосредственного получения ИК-спектров содержимого порошка измельченных таблеток при низких концентрациях кислоты аскорбиновой в таблетках в виде пасты с маслом вазелиновым показали, что образы нуждаются в предварительной экстракции действующего вещества и его концентриро-вании (рис. 3). Для экстракции кислоты аскорбиновой из таблеток был выбран спирт 96%.
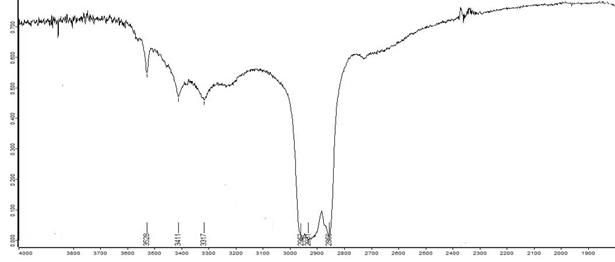

Рис.3. ИК-спектр таблеток Аскорбиновая кислота с глюкозой (Фармстандарт-Уфа-ВИТА, Россия) после проведения экстракции спиртом 96%.
В настоящей работе был составлен атлас ИК-спектров субстанций и препаратов водорастворимых витаминов с целью их последующего использования в качестве стандартных. Таким образом, разработаны методики подтверждения подлинности кислоты аскорбиновой в таблетках методом ИК-спектроскопии, которые могут быть использованы для выявления фальсифицированных препаратов, содержащих указан-ное вещество.
3.2 БиК-СПЕКТРОСКОПИЯ
3.2.1 Идентификация и дискриминация кислоты аскорбиновой
методом БИК-спектроскопии
На рис. 4 представлены БИК-спектры субстанций кислоты аскорбиновой разных производителей с фальсификатом. Видно, что гранулят 97% отличается от порошкообразных субстанций только по интенсивности спектров. Фальсифициро-ванная субстанция кислоты аскорбиновой отличается от других субстанций и грану-лята. БИК-спектры таблеток кислоты аскорбиновой имели заметные отличия, прояв-ляющиеся в основном в интенсивностях основных полос поглощения на отдельных участках спектров (рис. 5). Это может быть связано с разным составом вспомога-тельных веществ и с различным содержанием кислоты аскорбиновой в таблетках. Методика сравнения БИК-спектров может использоваться для установления под-линности препаратов только с концентрацией кислоты аскорбиновой в препарате свыше 25-30%. В этом случае в БИК-спектре можно увидеть полосы действующего вещества.
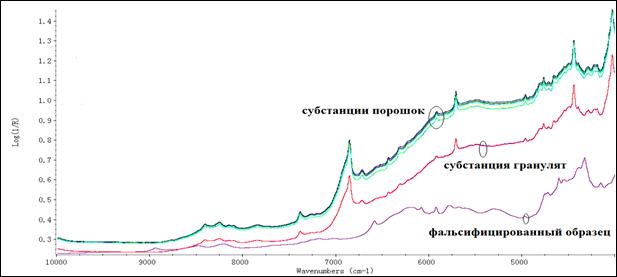
Рис.4. БИК-спектры субстанций кислоты аскорбиновой 13 серий 8 производителей в сравнении с фальсифицированным образцом.
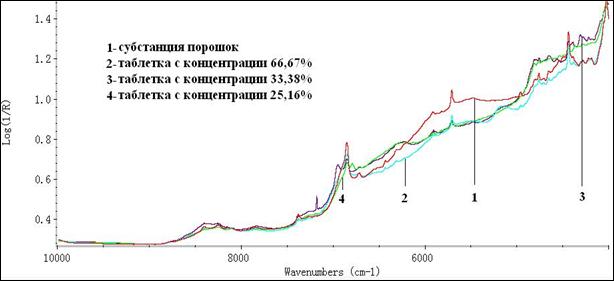
Рис.5. БИК-спектры субстанции и таблеток с концентрацией кислоты аскорбиновой от 25,16% до 66,67%.
В резульлате хемометрической обработки БИК-спектров (дискриминатный анализ, расчет расстояния Махаланобиса) нескольких серий субстанции кислоты аскорбиновой от разных производителей было показано, что все спектры порошко-образных субстанций достоверно различаются: расстояние Махаланобиса во всех случаях превышало 3σ (критическое расстояние Махаланобиса – 3σ при вероят-ности 95%) (табл. 2).
Подходы к классификации таблеток кислоты аскорбиновой были аналогичны методу классификации субстанций (табл. 3). Ясно, что таблетки различных фирм имели достоверные различия. При дискриминатном анализе чем больше расстояние Махаланобиса между центроидами классов образцов, тем больше различаются эти классы.
Табл.2. Статистические расстояния (единицы Махаланобиса) по оси абсцисс при дискриминатном анализе БИК-спектров порошкообразных субстанций кислоты аскорбиновой от 7 разных производителей. (1)фирма «Vitabiotics»; (2)фирма «Hubei Maxpharm»; (3)фирма «Hebei Belcom»; (4)фирма «Shenyang Beisheng»; (5)фирма «Shanghai Sinopharm»; (6)фирма «Dr. Ehrenstorfer GmbH»; (7)фирма «Реактив».
Номер | 2 | 3 | 4 | 5 | 6 | 7 |
1 | 20 | 23 | 19 | 18 | 27 | 19 |
2 | 14 | 5 | 10 | 20 | 15 | |
3 | 14 | 7 | 9 | 8 | ||
4 | 11 | 21 | 14 | |||
5 | 14 | 8 | ||||
6 | 13 |
Табл.3. Статистические расстояния (единицы Махаланобиса) по оси абсцисс при дискриминатном анализе БИК-спектров таблеток кислоты аскорбиновой от 10 разных производителей. (1)фирма «Nanjing Baijingyu»; (2)фирма «Vita come»; (3)фирма «Tsindao Haidewei»; (4)фирма «Hemofarm»; (5)фирма «Zentiva»; (6)фирма «Marbiopharm»; (7)фирма «Hainan Yangshengtang»; (8)фирма «Bristol-Myers Squibb»; (9)фирма «Фармпродукт»; (10)фирма «Фармстандарт-УфаВИТА».
Номер | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
1 | 17 | 8 | 8 | 10 | 11 | 12 | 20 | 6 | 24 |
2 | 15 | 14 | 13 | 13 | 13 | 17 | 15 | 9 | |
3 | 5 | 5 | 9 | 11 | 18 | 7 | 22 | ||
4 | 4 | 10 | 9 | 17 | 6 | 21 | |||
5 | 9 | 8 | 15 | 7 | 21 | ||||
6 | 9 | 18 | 9 | 20 | |||||
7 | 13 | 9 | 21 | ||||||
8 | 16 | 21 | |||||||
9 | 23 |
Полученные результаты свидетельствуют о возможности после расширения банка данных по производителям проводить идентификацию любого БИК-спектра субстанции или препарата кислоты аскорбиновой на принадлежность тому или иному производителю. Соответствующие электронные базы позволят определять «источник происхождения» лекарственного средства и осуществлять контроль рынка обращения, что особенно актуально в настоящее время.
3.2.2 Количественное определение кислоты аскорбиновой
методом БИК-спектроскопии
Из 78 образцов (с концентрацией кислоты аскорбиновой от 0,83% до 66,67%) были случайным образом выбраны 66 образцов и создан обучаюший набор для соз-дания статистической модели количественного анализа. Остальные 12 образцов были отобраны для проверочного набора, который используется для оценки досто-верности модели прогнозирования.
При разработке калибровок спектров использовали метод проекции на латентные структуры (PLS). Точность калибровки принято характеризовать величи-нами среднеквадратичного остатка калибровки (RMSEC) и среднеквадратичного остатка прогноза (RMSEP). Чем меньше RMSEC и RMSEP, тем точнее описываются обучающие данные. Кроме того, качество калибровки характеризуется еще и ко-эффициентом корреляции r2 - чем он ближе к единице, тем достовернее модель.
При предварительной обработке спектров используется метод множественной коррекции сигнала (MSC) для уменьшения влияния случайного шума и сглаживания сигнала. В табл. 4 представлены результаты хемометрических параметров (RMSEC, RMSEР и r2) при обработке спектров в диапазонах выбранных самой программой со вторыми производными спектрами.
Табл.4. Результаты расчета хемометрических параметров.
Метод предварительной обработки спектров | Диапазон спектров (cm-1) | RMSEC | RMSEР | r2 |
Метод множественной коррекции сигнала (MSC) со вторыми производными спектрами | 4065,2,35 4466,3,47 5712,1,12 | 2,14% | 1,70% | 0,99185 |
В табл. 5 представлены результаты анализа проверочных образцов с использо-ванием данной хемометрической модели при определении концентрации кислоты аскорбиновой в таблетках. Из полученных данных следует, что проведение коли-чественного определения кислоты аскорбиновой в таблетках реально возможно при её содержании в лекарственной форме на уровне не менее 25%. При снижении массовой доли кислоты аскорбиновой в общем случае существенно возрастает относительная ошибка определения.
Табл.5. Результаты анализа проверочных образцов.
Номер Образца | Номинальное содержание кислоты аскорбиновой в таблетке (%) | Полученное значение содержания кислоты аскорбиновой (%) | Отклонение от номинального содержания (%) |
1 | 66,67 | 67,22 | 0,85 |
2 | 33,38 | 31,55 | 5,48 |
3 | 27,03 | 26,65 | 1,41 |
4 | 25,32 | 25,49 | 3,98 |
5 | 25,16 | 24,80 | 1,43 |
6 | 25,16 | 29,03 | 15,38 |
7 | 15,38 | 16,19 | 5,27 |
8 | 10,42 | 7,53 | 17,52 |
9 | 10,26 | 11,36 | 10,70 |
10 | 5,88 | 4,85 | 17,52 |
11 | 1,67 | 1,61 | 3,59 |
12 | 0,83 | 1,04 | 25,30 |
3.3 УФ-СПЕКТРОФОТОМЕТРИЯ
3.3.1. Анализ УФ-спектров водорастворимых витаминов
Наличие сложных сопряженных систем в структурах водорастворимых вита-минов дает возможность широкого применения УФ-спектрофотометрии для их фарма-копейного анализа. IP и USP регламентируют при установлении подлинности сравне-ние УФ-спектров испытуемой субстанции со спектрами стандартных образцов. ГФ, CP, EP (BP) и JP при установлении подлинности регламентируют сравнение УФ-спектров испытуемой субстанции со стандартными спектрами.
В табл. 6 представлены спектральные характеристики лекарственных средств водорастворимых витаминов. Жирным шрифтом обозначен главный максимум поглощения.
Полученные УФ-спектры могут быть использованы при анализе водораство-римых витаминов по разделу НД «подлинность» (рис. 6-9).

Рис.6. УФ-спектр тиамина гидрохлорида (8 мкг/мл) в растворе кислоте хлористо-водородной 0,9%.

Рис.7. УФ-спектр рибофлавина (35 мкг/мл) в растворе ацетата натрия 0,01%.

Рис.8. УФ-спектр пиридоксина гидрохлорида (15мкг/мл) в воде (рН≈6,0).

Рис.9. УФ-спектр кислоты аскорбиновой (15 мкг/мл) в растворе кислоты серной 0,005 М.
Табл.6. Характеристика УФ-спектров водорастворимых витаминов.
Лекарственное вещество | Растворитель | Спектральные характеристики | |
Основные максимумы поглощения, нм | Приблизительное значение А (1%, 1 см) | ||
Тиамина гидрохлорид | HCl 0,9% | 246,0 | 421 |
Рибофлавин | CH3COONa 0,01% | 444,5 373,5 266,5 223,0 | 323 290 855 827 |
Пиридоксина гидрохлорид | Вода (рН ≈ 6,0) | 291,0 | 430 |
Аскорбиновая кислота | 0,005 M H2SO4 | 243,0 | 525 |
3.3.2. Количественное определение водорастворимых витаминов
методом УФ-спектрофотометрии
Количественное определение проводится в диапазоне концентраций, в кото-ром не происходит отклонений от линейной зависимости. Из полученных результа-тов следует, что линейная зависимость соблюдается во всем изученном диапазоне (табл. 7). Относительная погрешность количественного определения тиамина гидро-хлорида – 2,19%, рибофлавина – 1,19%, пиридоксина гидрохлорида – 1,27% и кис-лоты аскорбиновой – 2,26%, а полученные средние значения близки к номинальным (табл. 8).
Табл.7. Результаты изучения зависимости оптической плотности от концентрации стандартного раствора (проверка линейности). С – концентрация (мкг/мл).
Лекарственное вещество | Диапазон концентраций | Уравнение | R2 |
Тиамина гидрохлорид | 2 – 20 мкг/мл | А = 0,0471 x C – 0,0243 | 0,9997 |
Рибофлавин | 10 – 60 мкг/мл | А = 0,0082 x С + 0,002 | 0,9999 |
Пиридоксина гидрохлорид | 5 – 40 мкг/мл | А = 0,0382 x C – 0,045 | 0,9999 |
Аскорбиновая кислота | 2 – 20 мкг/мл | А = 0,0509 x C + 0,0037 | 0,9996 |
Табл.8. Метрологическая оценка методик количественного определения водораство-римых витаминов в таблетках методом УФ-спектрофотометрии.
Препарат | F | Хном, мг | Хср, мг | RSD% | S2 | S | Sxcp | α% | t(α, f) | ∆X | ε% |
Витамин В1 | 4 | 10 | 10,04 | 1,68 | 0,028 | 0,17 | 0,08 | 95 | 2,78 | 0,22 | 2,19 |
Витамин В2 | 4 | 40 | 39,46 | 0,97 | 0,146 | 0,38 | 0,17 | 95 | 2,78 | 0,47 | 1,19 |
Витамин В6 | 4 | 15 | 14,97 | 1,10 | 0,027 | 0,16 | 0,07 | 95 | 2,78 | 0,19 | 1,27 |
Витамин С | 4 | 10 | 9,74 | 1,71 | 0,029 | 0,17 | 0,08 | 95 | 2,78 | 0,22 | 2,26 |
Разработанные методики пригодны для анализа таблеток, содержащих указа-ные водорастворимые витамины, по разделу НД «количественное определение». Полученные средние значения содержания действующих веществ близки к номинальным.
3.4 ТОНКОСЛОЙНАЯ ХРОМАТОГРАФИЯ
Нами проведены исследования по разработке методик анализа водораство-римых витаминов методом ТСХ с использованием высокоэффективных пластинок (ПТСХ-АФ-В-УФ) «Сорбфил» размером 10×10 см. Для снижения эффекта размывания пятен водорастворимых витаминов рекомендовано проводить предварительную об-работку пластинок «Сорбфил» ПТСХ-АФ-В-УФ 25% раствором аммиака.
Изучено хроматографическое поведение исследуемых веществ в различных системах растворителей, описанных в научной литературе, и установлено, что они нуждаются в модификации при использовании российских пластин.
В результате проведенных исследований для подтверждения подлинности суб-станций и монопрепаратов были выбраны подвижные фазы, указанные в таблице 9.
В этих условиях значения Rf пятен водорастворимых витаминов находятся в диапазоне 0,39-0,59, что является оптимальным.
Табл.9. Результаты хроматографического анализа тиамина гидрохлорида, рибо-флавина, пиридоксина гидрохлорида, аскорбиновую кислоту с использованием метода ТСХ.
Наименование | Подвижная фаза | Рабочая концентрация, мг/мл | Значение Rf |
Тиамина гидрохлорид | этилацетат-метанол -раствор аммиака 25% (10:2:3) | 1 | 0,49 |
Рибофлавин | бутанол-метанол-бензол-вода (25:10:10:8) | 0,5 | 0,48 |
Пиридоксина гидрохлорид | пропанол-бутанол-вода -раствор аммиака 25% (10:7:1:2) | 1 | 0,59 |
Аскорбиновая кислота | метиленхлорид-этилацетат- этанол-муравьиная кислота (5:2:2:1) | 2 | 0,39 |
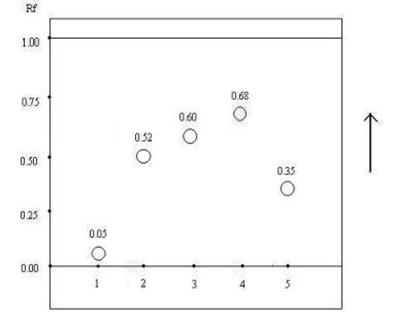
В результате был подобран оптимальный состав ПФ, являющийся универсальным для анализа всех исследованных водорастворимых витаминов группы В: бутанол-ацетон-вода (25:5:9). Диэлектрическая проницаемость данной ПФ, рассчитанная как среднее взвешенное значение, около 32. Значения Rf пятен комплексных водорастворимых витаминов находятся в пределах 0,05-0,68. Для витамина В1 лучше использовать собственную подвижную фазу. На рис. 10 схемати-чно представлена соответствующая хроматограмма.
Детектирование в УФ-свете с использованием разработанной методики позво-ляет различать пятна при нанесении на линию старта тиамина гидрохлорид 2 мкг, рибофлавина 1 мкг, пиридоксина гидрохлорид 2 мкг, никотинамида 2 мкг и фолие-вой кислоты 1 мкг.
При проведении детектирования было отмечено, что тиамин, рибофлавин, пиридоксин и фолиевая кислота различаются по способности флуоресцировать в УФ-свете. Пятна никотинамида и аскорбиновой кислоты проявляются только при облучении светом УФ-лампы при длине волны 254 нм (темные пятна на люминес-цирующем фоне пластины). Для проявления пятен аскорбиновой кислоты требуется обработка парами йода. При облучении УФ-светом с длинной волны 365 нм интен-сивность флуоресценции рибофлавина значительно увеличивается (ярко-желтое свечение) Все другие исследовавшиеся в данной работе (тиамин, пиридоксин и фолиевая кислота) при длине волны 365 нм детектируются в виде пятен темно-синего цвета.
| Рис.10. ТСХ комплексных водораст-воримых витаминов В группы в ПФ бутанол-ацетон-вода (25:5:9). Рядом с пятнами указаны значения Rf.. 1-тиамина гидрохлорид или тиамина мононитрат 2-рибофлавин 3-пиридоксина гидрохлорид 4-никотинамид 5-фолиевая кислота |
Разработанные методики являются воспроизводимыми, экспрессными, доступ-ными и могут использоваться для выявления фальсифицированных препаратов, не содержащих указанные на упаковке лекарственные вещества, и для анализа лекарст-венных витаминных препаратов по разделу НД «подлинность».
3.5 ВЫСОКОЭФФЕКТИВНАЯ ЖИДКОСТНАЯ ХРОМАТОГРАФИЯ
Нами была разработана унифицированная методика установления подлинности и количественного определения рибофлавина, пиридоксина гидрохлорида и никотинамида в поливитаминых препаратах «Центрум».
В качестве растворителя для извлечения витаминов из препарата использовали смесь ацетонитрила, кислоты уксусной ледяной и воды в соотношении 5:1:94.
Экспериментально нами была подобрана подвижная фаза, включаящая кислоту уксусную ледяную, метанол и воду в соотношении 5:270:725 с добавкой гептан-сульфоната натрия 2 ммоль/л.
На рис. 11 представлена хроматограмма раствора таблеток «Центрум» с кон-центрациями рибофлавина (13,6 мкг/мл), пиридоксина гидрохлорида (16 мкг/мл) и никотинамида (160 мкг/мл).
В табл. 10 представлены параметры пригодности хроматографической систе-мы, полученные после 5 последовательных введений стандартных растворов. Из представленных данных видно, что полученные параметры соответствуют не только современным общим фармакопейным требованиям к пригодности хроматографиче-ской системы, но и удовлетворяют более строгим требованиям.
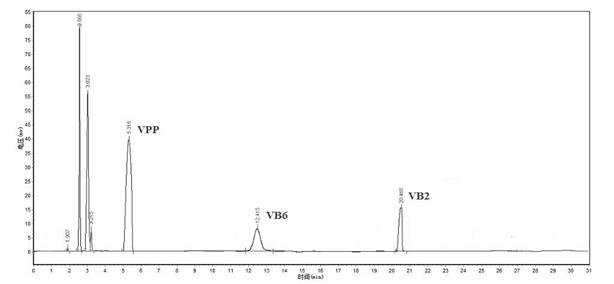
Рис.11. Хроматограмма испытуемого раствора таблеток «Центрум» при использо-вании ПФ вода-метанол-кислота уксусная ледяная (725: 270: 5) + гептансульфонат натрия 2 ммоль/л.
Табл.10. Хроматографические характеристики и параметры пригодности системы при 5 последовательных введениях стандартных растворов в концентрации вита-мина В2 – 13,6 мкг/мл, В6 – 16 мкг/мл, PP – 160 мкг/мл.
Лекарственное вещество | tR, мин | S/N | RSD% | AS | N |
Рибофлавин | 20,998 | 1600 | 0,5 | 1,21 | 7300 |
Пиридоксина гидрохлорид | 12,132 | 1400 | 0,4 | 1,33 | 8200 |
Никотинамид | 5,648 | 1300 | 0,8 | 1,08 | 1100 |
Табл.11. Метрологическая оценка методик количественного определения водораст-воримых витаминов в таблетках «Центрум» методом ВЭЖХ.
Лекарственное вещество в таблетке | f | Хном, Мг | Хср, мг | S2 | S | Sxcp | Α% | t(α, f) | ∆X | ε% |
Рибофлавин | 4 | 1,7 | 1,728 | 0,0041 | 0,064 | 0,011 | 95 | 2,78 | 0,031 | 1,79 |
Пиридоксина гидрохлорид | 4 | 2,0 | 1,944 | 0,0216 | 0,147 | 0,066 | 95 | 2,78 | 0,184 | 9,46 |
Никотинамид | 4 | 20 | 20,082 | 0,555 | 0,745 | 0,333 | 95 | 2,78 | 0,926 | 4,61 |
Метрологическая оценка разработанной методики (табл.11) показывает, что относительная погрешность количественного определения рибофлавина – 1,79%, пиридоксина гидрохлорида – 9,28% и никотинамида – 4,64%. Полученные средние значения близки к номинальным.
Разработанные методики пригодны для анализа таблеток, содержащих ука-заные водорастворимые витамины, по разделам НД «подлинность» и «количест-венное определение».
выводы
1. Разработана унифицированная методика анализа субстанций и лекарственных
препаратов водорастворимых витаминов методом ИК-спектроскопии и составлен атлас соответствующих ИК-спектров в вазелиновом масле, которые предлагаются для использования в качестве стандартных при анализе по разделу нормативной документации «подлинность» и для выявления фальсификатов, не содержащих указанное на упаковке действующее вещество.
2. Показано, что метод ближней ИК-спектроскопии в сочетании с дискрими-натным анализом может быть использован для подтверждения подлинности субстанций кислоты аскорбиновой и идентификации их производителя.
Установлено, что возможна идентификация таблеток кислоты аскорбиновой с определением их производителя при содержании кислоты аскобиновой в препарате от 25% и выше.
Построена калибровочная модель, позволяющая определять процентное содер-жание кислоты аскорбиновой в таблетках. Количественный анализ рекоменду-ется проводить при содержании данного действующего вещества в таблетках на уровне не менее 25%.
3. Разработаны методики анализа субстанций и препаратов водорастворимых витаминов методом УФ-спектрофотометрии, которые можно использовать в разделах нормативной документации «подлинность» и «количественное определение». Относительная погрешность количественного определения тиамина гидрохлорида – 2,19%, рибофлавина – 1,19%, пиридоксина гидро-хлорида – 1,27% и кислоты аскорбиновой – 2,26%.
4. Разработаны условия метода ТСХ и методики пробоподготовки субстанций и препаратов водорастворимых витаминов. Подобраны оптимальные составы подвижных фаз: для тиамина гидрохлорида – этилацетат-метанол-раствор аммиака 25% (10:2:3); для рибофлавина – бутанол-метанол-бензол-вода (25:10:10:8); для пиридоксина гидрохлорида – пропанол-бутанол-вода-раствор аммиака 25% (10:7:1:2) и для кислоты аскорбиновой – метиленхлорид-этилацетат-этанол-муравьиная кислота (5:2:2:1).
Разработан унифицированный состав подвижной фазы для комплексных водо-растворимых витаминов группы В бутанол-ацетон-вода (25:5:9), позволяющий одновременно анализировать тиамин, рибофлавин, пиридоксин, никотинамид и фолиевую кислоту.
Разработанные методики могут использоваться для выявления фальсифициро-ванных препаратов, не содержащие указанные на упаковке лекарственные вещества, и для анализа лекарственных витаминных препаратов по разделу нормативной документации «подлинность».
5. Установлено, что одновременный анализ лекарственных средств водораствори-мых витаминов (рибофлавина, пиридоксина гидрохлорида и никотинамида) методом обращенно-фазовой ВЭЖХ возможен в подвижной фазе – вода: метанол: кислота уксусная ледяная (725: 270: 5) с добавлением гептансульфа-ната натрия 2 ммоль/л.
Разработанная методика ВЭЖХ предлагается для стандартизации и котроля качества субстанций и препаратов водорастворимых витаминов (рибофлавина, пиридоксина гидрохлорида и никотинамида) в лекарственной форме «таблетки» по разделам «подлинность» и «количественное определение». Относительная погрешность количественного определения рибофлавина – 1,79%, пиридоксина гидрохлорида – 9,28% и никотинамида – 4,64%.
Список работ, опубликованных по теме диссертации
1. Ся Юй, Арзамасцев анализ методик ТСХ для стандарти-зации водорастворимых витаминов // Вопросы биологической, медицинской и фармацевтической химии. – 2009. – № 4. – С. 37-40.
2. Ся Юй, Дорофеев аскорбиновой кислоты методом ближней инфракрасной спектроскопии // Фармация. – 2010. – № 3. – С. 9-12.
3. Ся Юй, , Арзамасцев подлинности ком-плексных препаратов водорастворимых витаминов группы В с исполь-зованием метода ТСХ // Человек и лекарство: Тез. Докл. XVII Росс. нац. конгр. – М., 2010. – С. 549.
4. Ся Юй, , Арзамасцев подлинности лекар-ственных препаратов, содержащих действующее вещество аскорбиновой кислоты методом ИК-спектроскопии // Человек и лекарство: Тез. Докл. XVII Росс. нац. конгр. – М., 2010. – С. 549.