Для вспышек обеих этиологий было характерно территориальное распространение эпидемического процесса с вовлечением других ЛПУ, установленное на основании оперативных и ретроспективных эпидемиологических данных, результатов проспективного наблюдения, внутривидового типирования штаммов, включая анализ плазмидограмм и выделение различных плазмидных профилей для генотипической расшифровки эпидемических цепочек. Так, вспышка, вызванная S. typhimurium, в соматическом детском стационаре 1 получила дальнейшее распространение за пределы ЛПУ: 5 случаев (2 заноса, 3 ВБИ) в многопрофильном детском стационаре 8 - в ОРИТ и в отделение новорожденных; занос в детское отделение многопрофильного стационара 7 (1 случай); вынос из ЛПУ с возникновением домашнего очага (2 случая). Первая вспышка нозокомиального сальмонеллеза, вызванного S. virchow, в специализированном хирургическом стационаре получила дальнейшее развитие как в данном ЛПУ - вспышка 2, так и за пределами - вспышка в многопрофильном стационаре 3, возможно, вспышка в многопрофильном взрослом стационаре 4, с вовлечением инфекционного стационара (рис.4). Такое территориальное распространение сальмонеллезов обусловлено особенностями инфекции, способствующими протеканию эпидпроцесса в скрытой форме, свойствами сальмонелл, практикой перевода пациентов из одного ЛПУ в другое для оказания специализированной помощи, сходными нарушениями санитарно-противоэпидемического режима, некачественным эпиднадзором и мероприятиями, работой ЛПУ на оказание скорой помощи, что способствует заносам ГИ.
При анализе эпидемической обстановки на территориальном уровне были выявлены ЛПУ, названные нами проблемными стационарами. Проблемными являются ЛПУ, где повторно возникают групповые случаи и вспышки сальмонеллезов и/или неоднократно выявляются случаи сальмонеллезов с внутрибольничным инфицированием (ВБИ). Например, сальмонеллез, вызванный S. typhimurium, возникал в соматическом детском стационаре 1 12.2случаев), 01.2случая), 05.2случая), 04.2случаев). Неоднократные вспышки были и в многопрофильном стационаре 7, в соматическом детском стационаре 2 и других. Было выявлено несколько механизмов возникновения проблемных ЛПУ: 1) формирование длительных и стойких очагов нозокомиального сальмонеллеза с циркулирующим госпитальным штаммом, что приводит к возникновению вспышек одной этиологии, вызываемых идентичными штаммами; 2) особенности работы стационара и его структура, способствующие многочисленным и регулярным заносам инфекции, а также неудовлетворительное санитарно-техническое состояние ЛПУ, нарушения санитарно-противоэпидемического режима и недостатки в организации эпиднадзора и мероприятий, следствием чего является возникновение вспышек одной этиологии, но вызванных разными штаммами, и вспышек разной этиологии.
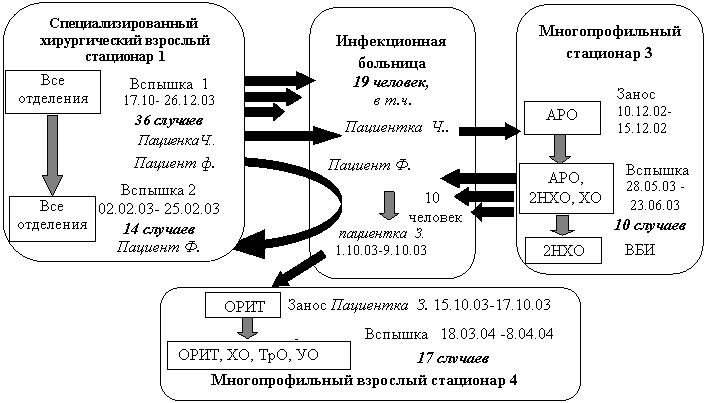
![]() Условные обозначения: - отделение: ОРИТ–отделение реанимации и интенсивной терапии; АРО–отделение анестезиологии и реанимации, ХО–хирургическое отделение, ТрО – травматологическое отделение, УО–урологическое отделение, 2НХО–2-е нейрохирургическое отделение.
Условные обозначения: - отделение: ОРИТ–отделение реанимации и интенсивной терапии; АРО–отделение анестезиологии и реанимации, ХО–хирургическое отделение, ТрО – травматологическое отделение, УО–урологическое отделение, 2НХО–2-е нейрохирургическое отделение.
![]()
![]() Распространение инфекции внутри очага в ЛПУ. Распространение инфекции из очага в ЛПУ в другое ЛПУ или домашний очаг
Распространение инфекции внутри очага в ЛПУ. Распространение инфекции из очага в ЛПУ в другое ЛПУ или домашний очаг
Рис.4. Территориальное распространение нозокомиального сальмонеллеза, обусловленного S.virchow
Была проведена комплексная микробиологическая характеристика в сравнительном аспекте различных вспышечных штаммов S. typhimurium и S. virchow. Штаммы S. typhimurium обладали признаками госпитальных и характеризовались: гомогенностью по биохимической характеристике; полирезистентностью к антибиотикам, продукцией БЛРС; гетерогенностью по профилям антиботикорезистентности (резистенс-типам), наличием 3-х профилей резистентности с ведущим профилем 1 (чувствительность фторхинолонам, амикацину, промежуточная чувствительность к полимиксину и тетрациклину, устойчивость к бета-лактамам, левомицетину, гентамицину); чувствительностью к поливалетному сальмонеллезному бактериофагу; гетерогенностью по чувствительности к дезинфектантам с наличием устойчивых штаммов; специфической плазмидной характеристикой: высокая встречаемость плазмид, особенно тяжелых, с преобладающей тяжелой плазмидой с молекулярным весом 65 МДa, нешироким спектром плазмид и их невысокой представленностью в культуре, мозаичностью плазмидных профилей с ведущим 2ПП (1 тяжелая - 65 МДa, 1 легкая - 17,4 МДa). В отношении редкого возбудителя S. virchow установлены следующие характеристики: способность формировать госпитальные штаммы, длительно циркулирующие в стационарах и получившие территориальное распространение; биохимическая характеристика, идентичная S. typhimurium; преобладание штаммов, полирезистентных к антибиотикам, продуцентов БЛРС; гомогенность по профилям резистентности с преобладающим профилем, отличающимся от ведущего резистенс-типа S. typhimurium чувствительностью к левомицетину; чувствительность к поливалентному сальмонеллезному бактериофагу; гетерогенность по чувствительности к дезинфектантам с наличием устойчивых и с неполной чувствительностью штаммов; специфическая плазмидная характеристика - высокая встречаемость плазмид, особенно легких, с преобладающей легкой плазмидой 13,2 МДa, широким спектром плазмид и их высокой представленностью в культуре, мозаичностью плазмидных профилей (ПП) с ведущими 1ПП (3 тяжелые - 48 МДa, 39 МДa, 32 МДa, 3 легкие - 15 МДa, 13,2 МДa, 5 МДa) и 4 ПП (4 легкие - 15 МДa, 13,5 МДa, 13,2 МДa, 5 МДa).
Полученные результаты послужили научным обоснованием для разработки положений эпиднадзора за нозокомиальными сальмонеллезами на территориальном уровне и на уровне ЛПУ (рис.5). В отличие от других ГИ именно эпиднадзор на территориальном уровне служил основой для эпиднадзора на уровне ЛПУ, где базовые положения адаптировались с учетом особенностей эпидемиологической обстановки и условий конкретного стационара. Благодаря территориальному эпиднадзору было своевременно выявлено эпидемическое неблагополучие по нозокомиальным сальмонеллезам, изменение их этиологии, территориальная ограниченность их распространения, дана комплексная характеристика особенностей нозокомиального сальмонеллеза редкой этиологии, выявлены сходные черты и различия вспышек разной этиологии, проведена дифференцировка связанных между собой вспышек в одном ЛПУ и в различных стационарах, а также вспышек, не связанных с другими, дана микробиологическая характеристика штаммов сальмонелл и изучена их циркуляция на территории. В рамках территориального эпиднадзора были разработаны критерии и выявлены проблемные по нозокомиальному сальмонеллезу ЛПУ. Обосновано выделение неблагополучных по нозокомиальному сальмонеллезу ЛПУ, которыми следует считать ЛПУ при выявлении даже 1 случая сальмонеллеза с внутрибольничным заражением, что обусловлено скрыто протекающим эпидемическим процессом при нозокомиальных сальмонеллезах, существенным преобладанием субклинических форм и бессимптомного носительства. В неблагополучных ЛПУ требуется проведение усиленного эпиднадзора и комплекса противоэпидемических мероприятий, а в проблемных ЛПУ необходима также разработка и внедрение программы по оздоровлению данного стационара.
При эпиднадзоре на уровне ЛПУ нами предложено оценивать обстановку как благополучную, неустойчивую, неблагополучную по таким показателям как наличие случаев сальмонеллеза и их характеристика (занос или ВБИ), выделение из внешней среды сальмонелл, наличие случаев ОКИ неустановленной этиологии и их характеристика (занос или ВБИ), обсемененность внешней среды как дополнительный критерий. Эпиднадзор и мероприятия проводятся дифференцировано исходя из эпидемиологической обстановки.
По данным различных исследователей и нашим собственным результатам микрофлора ЛПУ характеризуется устойчивостью к дезинфектантам. Одним из направлений исследований было изучение данной устойчивости и разработка методических подходов к ее мониторингу. В результате сравнительной оценки чувствительности к ДС в рекомендуемых режимах и при заниженных концентрациях и экспозициях у тест-культур и госпитальных штаммов S. aureus и E. coli установлен факт наличия у госпитальных штаммов устойчивости и неполной чувствительности к различным ДС из разных групп в рекомендуемых бактерицидных режимах.

Рис.5. Эпидемиологический надзор за нозокомиальными сальмонеллезами на уровне территорий и ЛПУ
Выявлен также более высокий порог чувствительности к дезинфектантам у госпитальных штаммов по сравнению с тест-штаммами, причем устойчивость и/или неполная чувствительность есть ко всем изученным группам ДС.
Для определения распространенности устойчивости к ДС среди микроорганизмов в стационарах города были организованы скрининговые исследования в 4 ЛПУ различного профиля. Установлена высокая доля устойчивых к ДС штаммов в микрофлоре различных стационаров по обобщенным данным - 39,42±12,1%. Устойчивость присутствовала как среди клинических изолятов, так и культур из внешней среды - 37,5±12,1% и 42,5±15,6% соответственно (p>0,05). Выявлена широкая вариабельность доли устойчивых к ДС микроорганизмов в различных ЛПУ в пределах от 7,14% до 86,7% (рис.6). Отмечена также неоднородость культур по степени чувствительности к ДС. Доля штаммов, на которые ДС оказывали суббактерицидное действие, колебалась от 2,38 до 10%, а неполное бактерицидное действие – от 3,33 до 35%. Устойчивость микрофлоры присутствовала по отношению ко всем изученным группам ДС, но в различной степени. Наибольшая устойчивость отмечена к средствам на основе четвертично-аммониевых соединений (ЧАС в сочетании с другими действующими веществами) – доля устойчивых штаммов 25,0 ± 4,2% (p<0,05), далее в порядке убывания кислородсодержащие, альдегидсодержащие, хлорсодержащие ДС, третичные амины, фенолсодержащие и наименьшая устойчивость была к группе гуанидинов – 9,4±2,8%.
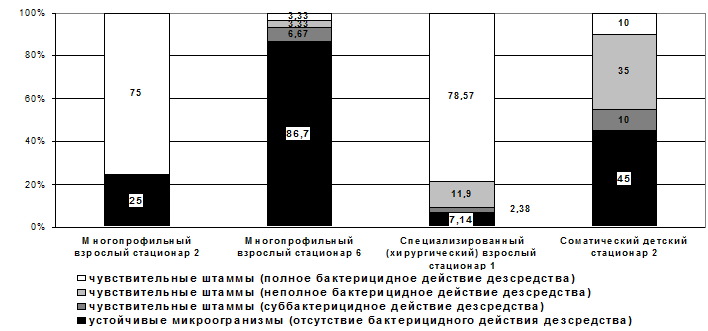
Рис.6. Структура чувствительности штаммов микроорганизмов к ДС,
применяемым в ЛПУ различного профиля.
Установлены выраженные различия по ЛПУ как по общей доле устойчивых штаммов, так и спектру устойчивости. Так, в многопрофильном взрослом стационаре 2 наибольшая доля устойчивых штаммов была к фенолсодержащим, далее равные показатели к хлорсодержащим и на основе ЧАС, к гуанидинам и третичным аминам устойчивости не было. В многопрофильном взрослом стационаре 6 наибольшая устойчивость была к средствам на основе ЧАС, далее в порядке убывания – кислородсодержащие, третичные амины, фенолсодержащие, хлорсодержащие и альдегидсодержащие ДС. Это указывает на определяющее значение при формировании устойчивости факторов, связанных с ЛПУ, предположительно, экологических особенностей, характеристик дезинфекционного режима, эпидемиологической ситуации, что требует дальнейшего исследования.
В то же время отмечен ряд общих для всех ЛПУ особенностей: дозозависимый эффект действия дезсредств; устойчивость к различным средствам одной группы (с одним действующим веществом) – перекрестная резистентность; устойчивость к средствам из различных групп – ассоциированная резистентность; гетерогенность культур по степени чувствительности; устойчивость у клинических штаммов и выделенных из внешней среды, при этом уровень устойчивости был как сопоставимым, так и было преобладание одной из категорий (выше среди клинических изолятов или наоборот). Термины «перекрестная резистентность» и «ассоциированная резистентность» введены нами по аналогии с антибиотикорезистентностью.
Был проведен сравнительный анализ чувствительности к дезинфектантам различных видов микроорганизмов (P. aeruginosa, Citrobacter spp., включая C. freundii и C. diversus, E. coli) на примере многопрофильного взрослого стационара 6. Установлена высокая устойчивость всех тестируемых видов и родов микроорганизмов. Так, все штаммы P. aeruginosa и E. coli, 75% культур Citrobacter spp. были устойчивы хотя бы к одному из ДС. Для указанных видов микроорганизмов была характерна полирезистентность, т. е. устойчивость к 2-м и более средствам. Выявлена также перекрестная резистентность, например, у культур P. aeruginosa к кислородсодержащим средствам, на основе ЧАС. Выявлена также ассоциированная резистентность у 100% штаммов P. aeruginosa, 50,0% Citrodacter spp. и 16,7% E. coli.
При наличии общей высокой доли устойчивых штаммов тестируемых видов, установлены выраженные видовые различия в спектре и уровне устойчивости как по группам ДС, так и по отдельным средствам. Для P. aeruginosa характерен высокий уровень устойчивости, наибольшая устойчивость к кислородсодержащим и на основе ЧАС, низкая устойчивость к хлорсодержащим средствам, более широкий спектр устойчивости по сравнению с другими видами; большая доля культур с полирезистентностью, перекрестной и ассоциированной резистентностью; достоверно более высокий уровень устойчивости к альдегидсодержащим ДС и на основе ЧАС как к группам в целом, так и к различным средствам. Культуры Citrobacter spp. проявили устойчивость к большинству групп дезинфектантов, кроме кислородсодержащих средств, что достоверно отличает данный род от других. Для E. coli был характерен менее широкий спектр устойчивости по группам и средствам.
Особое внимание было уделено оценке чувствительности к ДС микрофлоры хирургического поликлинического отделения, учитывая выявленные эколого-эпидемиологические особенности АПУ и ГСИ в условиях поликлиники. Установлено, что по отношению к ДС микрофлора АПУ характеризовалась:
- наличием устойчивости, но на более низком уровне по сравнению со среднестационарным показателем - 14,7±7,2% vs 39,42±12,1% (p<0,05), однако сравнимо с показателями отдельных ЛПУ;
- наличием устойчивости как у культур, выделенных от пациентов, так и из внешней среды с преобладанием первых - 20,0% vs 5,7% (p<0,05);
- присутствие гетерогенности по степени чувствительности к ДС: на 13,7% всех штаммов средства оказывали неполное бактерицидное действие, на 1,1% – суббактерицидное действие;
- различной представленностью устойчивых штаммов среди возбудителей в зависимости от условий возникновения ГСИ: выше доля устойчивых среди штаммов, занесенных из стационаров (2-я группа) - 42,9%, наличие устойчивости среди возбудителей внутриполиклинических ГСИ (3-я группа) - 25,0%, у возбудителей внебольничных инфекций (I группа) устойчивости не было (p<0,05);
- отмечено наличие зависимости время-эффект действия дезинфектантов.
Важным аспектом в мониторинге устойчивости к ДС является тестирование штаммов, обусловивших вспышки ВБИ, что необходимо для проведения эффективных дезинфекционных мероприятий в возникшем очаге, а также для выяснения причин вспышки, одной из которых может быть устойчивость возбудителей к ДС. Были исследованы культуры сальмонелл, вызвавшие вспышки нозокомиального сальмонеллеза в ЛПУ города и имевшие территориальное распространение. Установлено что устойчивость к ДС присутствовала в 3 вспышках из 7, включая 2 вспышки из 4, обусловленных S. virchow (14,8% и 25%) и 1 вспышку из 3, вызванных S. typhimurium (45,0%). Общим для указанных сероваров сальмонелл являлось высокая представленость культур, устойчивых к дезинфектантам – 15,1% в целом, 10,6% среди культур S. virchow и 22,5% среди S. typhimurium (p>0,05), а также штаммов с неполной чувствительностью – 20,8%, 9,1% и 40,0% соответственно (p<0,05). Отмечено наличие перекрестной, ассоциированной и полирезистентности, гетерогенности штаммов по профилям резистентности, но присутствием и штаммов с одинаковым профилем. У обоих сероваров выявлена устойчивость к большинству протестированных групп ДС: к хлорсодержащим, на основе ЧАС, к фенолсодержащим. Различия также присутствовали: у S. virchow устойчивость была при разных вспышках, тогда как у S. typhimurium – только в одной, были различия и в профилях резистентности.
При оценке штаммов, которые отличались устойчивостью, установлено, что они имели идентичные профили антибиотикорезистентности и биохимические свойства, а по плазмидным профилям имелись как отличия, так и совпадения. В то же время штаммы, чувствительные к ДС, имели различия по плазмидным профилям и антибиотиограмме. Таким образом, вопрос о применении профиля устойчивости к дезинфектантам при выявлении эпидемических цепочек как маркера штамма остается открытым, его можно рассматривать как характеристику культуры только в комплексе с другими маркерами. Был проведен сравнительный анализ профилей резистентности вспышечных культур S. virchow из 2-х разных стационаров по тем 5 дезинфектантам из 5 групп, которые применялись в обоих ЛПУ. Получены результаты о выраженных различиях в чувствительности к одним и тем же ДС микроорганизмов одного серовара, следовательно, при формировании устойчивости определяющее значение имеют экологические условия в каждом конкретном ЛПУ, формирующие фенотипические характеристики штаммов.
С целью изучения устойчивости к ДС в естественных условиях был организован на протяжении 6 месяцев мониторинг в различных отделениях взрослого многопрофильного стационара 6. Полученные данные позволили предположить существование следующих состояний (стадий) чувствительности к ДС микрофлоры ЛПУ: 1) состояние чувствительности; 2) состояние формирования устойчивости; 3) состояние сформированной устойчивости, ограниченной по территории; 4) состояние распространенной устойчивости. В качестве критериев применялись следующие показатели: наличие устойчивых к ДС штаммов; характеристика культур по степени чувствительности; источник выделения устойчивых культур (пациенты, внешняя среда или оба источника); территориальная характеристика выделения устойчивых штаммов (распространенность по отделениям); длительность и постоянство выделения устойчивых и с неполной чувствительностью штаммов в отделении и стационаре. Было разработаны рекомендации по организации мониторинга устойчивости и тактике дезинфекции в ЛПУ в зависимости от состояния. Например, состояние распространенной устойчивости микрофлоры стационара к дезинфектанту характеризуется наличием устойчивых штаммов среди культур, выделенных от пациентов и из внешней среды; широкой распространенностью устойчивости и неполной чувствительности в различных отделениях; стабильностью выделения устойчивых штаммов и/или с неполной устойчивостью в одном отделении в динамике; выделением устойчивых штаммов от пациентов и из внешней среды в одном отделении; при применении средства в нескольких режимах устойчивость и/или неполная чувствительность проявляется в более чем одном режиме. При таком состоянии рекомендован отказ от применения данного средства во всех режимах и данной группы дезинфектантов (временно), подбор новых ДС из других групп после предварительного тестирования чувствительности к ним госпитальных штаммов, усиление мониторинга устойчивости (ежемесячно).
Таким образом, полученные результаты о широкой распространенности устойчивости и ее характеристиках послужили научным обоснованием необходимости внедрения мониторинга устойчивости к дезинфектантам как компонента эпиднадзора за ГИ. Наряду с общими принципами нами научно обоснованы и разработаны дифференцированные организационно-методические положения мониторинга при разных видах медицинской помощи и на территориальном уровне. Полученные результаты определяют необходимость характеристики устойчивости в каждом ЛПУ в комплексе с оценкой эпидемиологической обстановки, микробного пейзажа и дезинфекционного режима. Тактика проведения мониторинга в многопрофильных ЛПУ определяется состоянием чувствительности микрофлоры к разным ДС, учитываются типы отделений по роли в поддержании эпидемического процесса, параметры адаптируются к особенностям конкретного стационара. При организации мониторинга в АПУ учитываются различия устойчивости к ДС возбудителей ГСИ в зависимости от условий возникновения и другие эколого-эпидемиологические особенности АПУ.
Обобщая полученные результаты исследований, многолетний собственный опыт изучения ГИ, данные других авторов, накопленные теоретические и практические разработки, нами была сформулирована концепция многоуровневой системы эпиднадзора за госпитальными инфекциями.
Основные положения концепции многоуровневой системы эпиднадзора за госпитальными инфекциями следующие.
Ø Эпиднадзор за ГИ, осуществляемый на уровне ЛПУ (основной уровень) и на территориальном уровне (Управление Роспотребнадзора, ФГУЗ «Центр гигиены и эпидемиологии», департамент здравоохранения), различен. Эпиднадзор имеет разные задачи, компоненты, характер управленческих решений и другие параметры.
Ø Эпиднадзор за ГИ отличается при различных видах медицинской помощи: 1) в амбулаторно-поликлинических учреждениях; 2) в многопрофильных ЛПУ; 3) в специализированных стационарах и отделениях. Это обусловлено существенными различиями в плане эколого-эпидемиологических особенностей, закономерностей и проявлений эпидемического процесса ГИ, что требует дифференцированного подхода к эпиднадзору и мероприятиям.
Ø Существуют положения и компоненты эпиднадзора, общие для всех ЛПУ, и параметры эпиднадзора, адаптированные к особенностям разных видов медицинской помощи и профилей специализации ЛПУ.
Ø Эпиднадзор за ГИ осуществляется дифференцированно за традиционными инфекциями, паразитозами и ГСИ вследствие значительных эпидемиологических различий этих групп болезней.
Ø Эпиднадзор за ГИ должен проводиться с учетом этиологии, он имеет свои особенности при разных моноэтиологичных ГИ и инфекциях смешанной этиологии.
Ø Требуется включение нового компонента эпиднадзора за ГИ – мониторинга устойчивости к дезинфектантам микрофлоры ЛПУ, который также имеет различные параметры на территориальном уровне, в многопрофильных и специализированных ЛПУ (отделениях) и в АПУ.
Многоуровневая система эпиднадзора за ГИ, как и за другими инфекциями, состоит из трех основных подсистем, каждая из которых включает ряд компонентов, имеющих те или иные адаптированные параметры в зависимости от уровня надзора и профиля ЛПУ (рис.7).
Основанием для данной концепции послужили результаты собственных исследований о выраженных эколого-эпидемиологических особенностях ГИ при разных видах медицинской помощи; положение о хирургическом стационаре как о своеобразной экосистеме (, 1996); социально-экологическая концепция эпидемического процесса (,1984), позволяющая рассматривать территориальное распространение ГИ как соцэкосистемный уровень эпидемического процесса; концепция профилактики ВБИ ( с соавт., 1999); общая система эпиднадзора за инфекционными болезнями и разработанные ранее компоненты эпиднадзора за ВБИ, принятые за основу. В предлагаемой нами системе эпиднадзора за ГИ существующая система расширена и рассмотрена с точки зрения различных уровней (ЛПУ и территориальный), подуровней (различных виды оказания медицинской помощи), усовершенствованы общие положения, добавлены новые компоненты, разработаны адаптированные параметры уже имевшихся ранее компонентов. Было проведено теоретическое обоснование всех изменений, отработано их организационно-методическое обеспечение, осуществлено внедрение в практическое здравоохранение с оценкой эффективности.
Разработанная многоуровневая система эпиднадзора за ГИ позволила:
· осуществлять дифференцированный подход к эпиднадзору при различных видах медицинской помощи с учетом эколого-эпидемиологических особенностей ГИ;
· оптимизировать эпиднадзор на уровне ЛПУ и на территориальном уровне;
· учитывать этиологические особенности инфекции;
· вводить новые компоненты (мониторинг устойчивости к дезинфектантам);
· дать объективную оценку эпидемиологической ситуации в многопрофильных ЛПУ и определить особенности ГСИ как в целом, так и определенной этиологии;
· охарактеризовать микробный пейзаж многопрофильных ЛПУ и циркуляцию госпитальных штаммов и госпитальных ассоциаций;
· определить эколого-эпидемиологические особенности АПУ, истинный уровень заболеваемости и структуру ГСИ;
· выявить особенности территориального распространения ГИ на модели нозокомиального сальмонеллеза, расшифровать вспышки этой инфекции в ЛПУ.
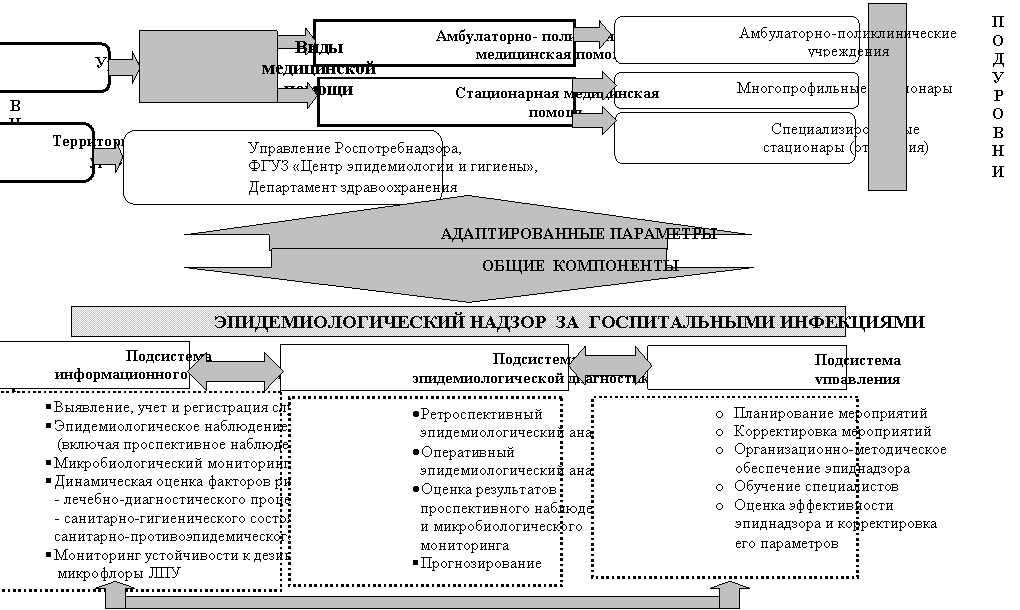
Рис.7. Многоуровневая система эпидемиологического надзора за госпитальными инфекциями
На основании результатов эпиднадзора научно обоснован, разработан и внедрен комплекс мероприятий с оценкой его эпидемиологической эффективности:
- полный комплекс противоэпидемических мероприятий, проведенный своевременно благодаря раннему и полному выявлению случаев инфекции;
- устранение нарушений санитарно-противоэпидемического режима;
- изменение дезинфекционного режима в соответствии с устойчивостью микрофлоры к дезинфектантам и выявленным ведущим факторам передачи;
- совершенствование диагностических мероприятий: определение показаний к микробиологическому и другому обследованию, методов и сроков;
- оптимизация лечебных мероприятий, в т. ч. антибиотикотерапии, фаготерапии;
- совершенствование методических подходов к применению бактериофагов;
- изменение лечебно-диагностического процесса: внедрение безопасных алгоритмов манипуляций, проведение мероприятий по снижению риска инфицирования.
В результате совершенствования эпиднадзора и внедрения комплекса мероприятий удалось существенно снизить заболеваемость ГИ (ВБИ). Так, достигнуто снижение заболеваемости ВБИ синегнойной этиологии в детском многопрофильном стационаре в целом в 2,9 раза (0,58±0,14 vs 0,2±0,01 в начале и конце анализируемого периода, p<0,05) и в проблемных отделениях в 2,7 – 11 раз (p<0,05): урологии - 3,2±0,68 vs 0,65±0,3, в гематологии - 3,6±0,9 vs 0,98±0,5, в ОРИТ - 2,0±0,58 vs 0,72±0,35, в ОРН - 21,4±2,8 vs 1,9±0,93. Изменились также другие проявления эпидемического процесса: тенденция к снижению заболеваемости ВБИ в многолетней динамике по ЛПУ в целом и в отделениях риска, изменения в структуре заболеваемости - преобладание заносов над ВБИ (доля 69,7% vs 30,3% соответственно, частота 0,47±0,11 vs 0,2±0,007 на 100 пациентов, p<0,05), снижение обсемененности внешней среды стационара P. aeruginosa (0,52±0,05 vs 0,37±0,03%, p<0,05), прекращение циркуляции двух основных госпитальных штаммов.
В хирургическом отделении поликлиники итогом внедрения оптимизированного эпиднадзора и комплекса мероприятий было снижение обсемененности внешней среды в 2,4 раза (с 17,2% до 7,05%, p<0,05), снижение эпидемиологической значимости пациентов с первичными ГСИ и ГСИ, занесенными из стационаров, за счет уменьшения контаминации раны и сокращения длительности выделения возбудителя при применении бактериофага, снижение заболеваемости внутриполиклиническими ГСИ в 4 раза - с 3,8±0, 97 до 0, 96±0, 68 на 100 операций (p<0,05).
В результате усиленного эпиднадзора и комплекса мероприятий по борьбе с нозокомиальными сальмонеллезами в различных ЛПУ и на территории удалось
добиться улучшения эпидемиологической ситуации: снизить заболеваемость с 3,7-8,30/0000 до 1,10/0000 в 2005 г., 0,40/0000 в 2006 г. (в 9-20 раз, p<0,01), снизить
число вспышек, вызванных S. typhimurium,
· предотвратить вспышки, обусловленные S. virchow, в неблагополучных ЛПУ ликвидировать длительно существующие очаги с циркуляцией госпитальных штаммов.
Таким образом, оптимизированный эпиднадзор на основе предложенной концепции многоуровневой системы эпиднадзора за ГИ и разработанные мероприятия продемонстрировали высокую фактическую эпидемиологическую эффективность. Были сделаны следующие выводы и даны практические рекомендации.
ВЫВОДЫ
1. Многопрофильные стационары и ГИ в данных ЛПУ характеризуются эколого-эпидемиологическими особенностями: напряженной общей эпидемиологической обстановкой (общая заболеваемость - 31,53±1,620/00 – 204,12±1,130/00), широкой представленностью всех групп традиционных инфекций с достоверным лидированием инфекций наружных покровов (53,89-92,26%, 9,61±0,76 – 14,53 ± 2,250/00) и преобладанием заносов (77,8 – 95,7%, 12,52±1,030/00 – 18,05±2,50/00), более узким спектром паразитозов, являвшихся заносами, преобладанием в структуре ГСИ (51,7%-83,3%) преимущественно ВБИ, особенностями микробного пейзажа, отличительными характеристиками ГСИ в целом и различной этиологии в пределах всего ЛПУ и в отделениях.
2. ГСИ в условиях многопрофильных ЛПУ отличались относительно невысоким уровнем в целом по стационару и выраженными колебаниями показателей по отделениям (1,63±0,2 на 100 пациентов, от 0,27±0,08 до 38,28±4,03 на 100 пациентов, p<0,01). Установлено этиологическое и клиническое разнообразие ГСИ с общими лидирующими возбудителями и нозологическими группами в стационаре и меньшее разнообразие ГСИ в отделениях. Имелись выраженные эпидемиологические, клинические и микробиологические особенности инфекций по отделениям, которые нивелировались при оценке по стационару в целом.
3. Микробный пейзаж многопрофильных ЛПУ характеризовался большим разнообразием (13 родов, 21 вид микроорганизма) с преобладанием стафилококков. Хирургические и терапевтические отделения имели выраженные различиями по частоте высеваемости, разнообразию и представленности грамположительных и грамотрицательных микроорганизмов. Определены отделения, «показательные» по разным микроорганизмам с высокой частотой и постоянством их выделения. В годовой динамике высеваемости условно-патогенных микроорганизмов выявлены выраженные и регулярные подъемы в определенные сезоны года как в ЛПУ в целом, так и в «показательных» отделениях, с большей или меньшей синхронностью, различиями кривых высеваемости микроорганизмов разных видов и родов. Отмечалось 2-3 подъема высеваемости в осенне-зимний и/или зимне-весенний и в летний сезоны. Для грамположительных микроорганизмов было характерно 2-3 подъема с наибольшим в осенне-зимний и/или зимне-весенний сезоны, грамотрицательные микроорганизмы имели 2 подъема - наибольший в летний и в зимне-весенний сезоны.
4. Для ГСИ определенной этиологии, изученной на модели синегнойной инфекции, были характерны как общестационарные черты, так и особенности в разных отделениях. К общестационарным характеристикам относились: преимущественно внутрибольничное возникновение, экзогенное происхождение, лидирующая нозологическая группа (инфекции органов дыхания - 32,5%), возрастная группа риска (дети до 1 года), основные механизмы (контактный и артифициальный) и категории факторов передачи инфекции (растворы, аппаратура, предметы ухода), преобладание в структуре двух госпитальных штаммов, получивших общестационарное распространение. Отделения различались по уровню заболеваемости, частоте заносов, манифестности форм, клиническим формам инфекций, штаммовому пейзажу, путям передачи, конкретным факторам передачи инфекции и территориям риска.
5. В условиях многопрофильных ЛПУ при выраженном штаммовом разнообразии создаются условия для широкой и длительной циркуляции госпитальных штаммов микроорганизмов. Отделения отличаются по их роли в поддержании эпидемического процесса ГИ определенной этиологии и циркуляции возбудителей. I тип - отделения, обеспечивающие присутствие возбудителя в стационаре и поддержание эпидемического процесса вызываемой им инфекции. II тип - отделения, обеспечивающие распространение возбудителя и его циркуляцию в переделах ЛПУ. III тип - отделения с высоким риском возникновения заболеваний. IV тип - отделения, вовлеченные в эпидемический процесс инфекции. Критериями для их выделения явились уровень заболеваемости, частота заносов и ВБИ, соотношение носительства и манифестных форм инфекции, штаммовое разнообразие, обсемененность внешней среды, особенности лечебно-диагностического процесса и контингента пациентов. Компоненты эпидемиологического надзора имеют параметры, адаптированные к особенностям указанных типов отделений.
6. Установлена высокая частота и существенная доля полиэтиологичных инфекций в многопрофильных ЛПУ (15,1%-34,7%), у хирургических пациентов (1,6±0,35 на 100 пациентов, удельный вес среди всех ГСИ – 41±7,1%), эпидемиологические, клинические и микробиологические различия полиэтиологчных и моноэтиологичных инфекций. Выявлено существование госпитальных ассоциаций микроорганизмов, обладающих особыми характеристиками и циркуляцией в пределах отделения, способных вызвать внутрибольничное инфицирование пациентов с возникновением полиэтиологичных инфекций.
7. Хирургические отделения амбулаторно-поликлинических учреждений обладают эколого-эпидемиологическими особенностями, отличающимися от различных хирургических отделений стационаров характеристикой пациентов по основной патологии, лечебно-диагностическим процессом и организацией работы, микробным пейзажем, частотой ГСИ, структурой ГСИ по условиям возникновения с выраженными эпидемиологическими, микробиологическими и клиническими различиями первичных ГСИ, инфекций, занесенных из стационаров и внутриполиклинических ГСИ, что определяет необходимость дифференцированного подхода к эпидемиологическому надзора и контролю в условиях АПУ.
8. Эпидемический процесс нозокомиальных сальмонеллезов характеризуется способностью к территориальному распространению с вовлечением различных стационаров (неблагополучные ЛПУ), повторным поражением одних и тех же стационаров (проблемные ЛПУ), наличием выраженных особенностей при разной этиологии. Выявлена способность Salmonella virchow к образованию госпитальных штаммов, циркулирующих в пределах стационара и на территории, формирующих стойкие очаги нозокомиального сальмонеллеза и вспышки в различных ЛПУ. Вспышки, обусловленные S. virchow, отличались от сальмонеллеза, вызванного S. typhimurium, большей продолжительностью (в среднем, на 9 дней, 33 vs 24, p<0,05); большим числом случаев (в среднем, на 6 человек, 19 случаев vs 13 человек); поражением исключительно взрослых пациентов; меньшим вовлечением персонала и ухаживающих; большей долей случаев средней тяжести (83,3% vs 65,2%, p<0<0,5) и меньшей долей тяжелых клинических форм (10% vs 21,7%, p<0,05), меньшей летальностью (1,3% vs 3,8%, p<0,05); более широким распространением в пределах ЛПУ; поражением хирургических отделений и ОРИТ; автономностью эпидемического процесса.
9. Госпитальные штаммы S. virchow и S. typhimurium характеризовались полирезистентностью к антибиотикам, продукцией БЛРС, чувствительностью к бактериофагу, наличием устойчивых к дезинфектантам штаммов, частой встречаемостью плазмид и их широким спектром, наличием общих тяжелых плазмид (39 МДa и 32 МДa). Штаммы данных сероваров отличались по профилям антибиотикорезистентности и разнообразию резистенс-типов, а также по таким плазмидными характеристиками как спектр и представленность тяжелых и легких плазмид, частота встречаемости плазмид с разными молекулярными весами и плазмидные профили.
10. Установлена высокая распространенность устойчивости дезинфектантам микрофлоры различных многопрофильных стационаров (в среднем, 39,42±12,1%) и АПУ (14,7±7,2%, p<0,05), наличие устойчивости среди культур, выделенных из клинического материала (37,5±12,1%) и из внешней среды (42,5±15,6%, p>0,05), а также вспышечных штаммов, гетерогенность культур по чувствительности к ДС, более высокий порог чувствительности к дезинфектантам госпитальных штаммов по сравнению с тест-штаммами, широкий спектр устойчивости к разным группам и ДС, наличие полирезистентности, перекрестной и ассоциированной резистентности, выраженные видовые различия устойчивости микроорганизмов, что определяет необходимость внедрения мониторинга устойчивости к ДС как обязательного компонента эпиднадзора за ГИ при разных видах медицинской помощи и на территориальном уровне.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |




