Как видно, из данных приведенных в таблице 2, анализируемые составы обладают хорошими реологическими свойствами, высокими показателями насыпной массы. Несмотря на широкий интервал значений, все образцы разработанных составов обладали высокой сыпучестью, минимум в два раза превышающей требуемые значения (не менее 4-5 г/с). Угол естественного откоса также охарактеризовал исследуемые составы как хорошо сыпучие, так как его значения для всех образцов находились в интервале 25-34º.
Распадаемость для составов 1-1, 2-1, 29-2 и 46-2 составила менее 5 минут, что считается удовлетворительным для быстрорастворимых («шипучих») гранулятов и таблеток (European pharmacopoeia, 5 edition). Распадаемость состава 59 составила менее 15 минут (ГФ XI, вып.2).
Измерение рН растворов, образуемых при растворении образцов составов 1-1, 2-1, 29-2 и 46-2 показало, что данный показатель близок к рН кожного покрова человека и, следовательно, растворы не должны обладать местно раздражающим действием.
Разработанные составы гранул соответствовали требованиям ГФ XI по статье «Испытание на микробиологическую чистоту» и Изменению №3 «Методы микробиологического контроля ЛС» от 01.01.2001 г (Изм. №3). Растворы гранул с концентрацией ДВ 0,4% (ПГМГф) и 0,5% (ПГМГх) полностью подавляли рост следующих микроорганизмов: Escherichia coli АТСС 25922, Staphylococcus aureus АТСС 6538-Р, Trichophyton mentagrophytes interdigitale, Trichophyton verrucosum и Microsporum canis.
Таким образом, на основании проведенных исследований можно сделать вывод о том, что основные качественные, количественные и технологические характеристики гранулятов составов 1-1, 2-1, 29-2 и 46-2 и 59 удовлетворяют предъявляемым к ЛФ «Гранулы» требованиям.
С целью установления стабильности образцы составов гранул были заложены на хранение. С этой целью образцы составов гранул хранили в полимерных банках с навинчивающимися крышками: одну часть наработанных составов гранул хранили в сухом, защищенном от света месте при температуре 15-25°С, а другую в термостате при температуре 40±1°С. В день изготовления и в процессе хранения (через каждые 6 месяцев при хранении в естественных условиях, через каждые 46 суток при хранении по методу ускоренного старения) образцы гранул анализировали по следующим показателям: внешний вид, подлинность, количественное содержание ДВ, определение фракционного состава, насыпной массы, сыпучести, угла естественного откоса, остаточной влажности, распадаемости и значения рН. Анализ полученных данных свидетельствуют о стабильности изучаемых образцов как в процессе естественного хранения (в течение 2 лет), так и методом ускоренного старения (в течение срока эквивалентного 2 годам хранения в естественных условиях). Основные технологические характеристики гранул, а также распадаемость и значение рН образуемых растворов практически не изменяются. Гранулы характеризуются постоянством качественного и количественного содержания действующего вещества в течение всего срока хранения. Образцы гранул, хранившиеся по методу ускоренного старения и в естественных условиях в течение 2 лет, соответствуют требованиям статьи ГФ XI «Испытание на микробиологическую чистоту» и Изм. №3, сохраняют антимикробную и противогрибковую активность.
Полученные данные позволяют рекомендовать срок хранения составов 1-1, 2-1, 29-2, 46-2 и 59, расфасованных в полимерные банки, в сухом, защищенном от света месте при температуре 15-25°С в течение 2 лет (срок наблюдения).
Разработка состава и технологии изготовления быстрорастворимых таблеток, содержащих ПГМГф
На основе разработанных составов и технологии получения быстрорастворимых гранул, содержащих в качестве ДВ ПГМГф, была проведена оценка возможности прессования гранулятов, с целью получения ЛФ таблетки. В состав образцов вводили смазывающие ВВ, обладающие гидрофобными и гидрофильными свойствами: аэросил, кислоту стеариновую, натрия бензоат и глицин в количестве 1-4% от общей массы гранулята.
На основании полученных экспериментальных данных нами для таблетирования была отобрана рецептура состава 29-2, представленная в таблице 3.
Таблица 3
Рецептура состава, отобранного для таблетирования, содержащего ПГМГф в качестве ДВ
Ингредиент | 29-2 | ||
На 1 таблетку | На 100,0 г | ||
мг | % | ||
ПГМГф (лиофилизированный) | 477 | 31,8 | 31,8 |
Винная кислота | 546 | 36,4 | 36,4 |
Натрия карбонат | 405 | 27,0 | 27,0 |
Коллидон | 42 | 2,8 | 2,8 |
Натрия бензоат | 30 | 2,0 | 2,0 |
С целью выявления оптимальной для таблетирования величины влагосодержания гранулята, было проведено изучение зависимости механической прочности на сжатие и времени распадаемости таблеток от остаточной влажности разработанных составов. На рис. 1 и 2 приведены зависимости механической прочности и распадаемости таблеток от остаточной влажности гранулята.
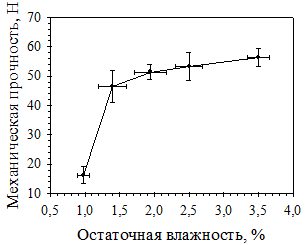
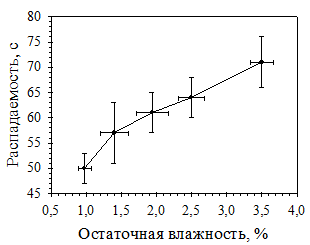
Рис. 1. Зависимость механической прочности на сжатие таблеток состава 29-2 от остаточной влажности гранулята
Рис. 2. Зависимость распадаемости таблеток состава 29-2 от остаточной влажности гранулята
Проведенные исследования показали, что распадаемость разработанных составов таблеток напрямую зависит от остаточной влажности гранулята, но на протяжении всего интервала исследуемых давлений прессования не превышает 5 минут. Механическая прочность таблеток возрастает при увеличении остаточной влажности, при значении влажности гранулята менее 1% таблетки обладают очень низкой (менее 20Н) механической прочностью. Оптимальная для таблетирования гранулята состава 29-2 влажность
составила 1,2-1,6%.
С целью выявления оптимального режима таблетирования было проведено изучение зависимости основных характеристик таблеток от величины прилагаемого давления прессования (рис. 3 и 4). При увеличении давления прессования увеличивается механическая прочность на сжатие и распадаемость. При любом значении давления прессования время распадаемости не превышало 5 минут, прочные таблетки получаются при давлении прессования выше 150 МПа. Таким образом, оптимальный диапазон давления прессования для разработанного состава таблеток составляет 150-240 МПа.
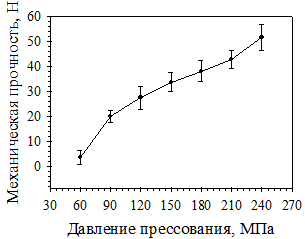
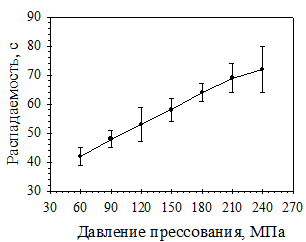
Рис. 3. Зависимость механической прочности на сжатие таблеток состава 29-2 от давления прессования
Рис. 4. Зависимость распадаемости таблеток состава 29-2 от давления прессования
Технология выбранного нами метода влажного гранулирования (рис. 5) позволила получить однородный гранулят с хорошей сыпучестью, прессуемостью и высокой насыпной массой.
Доброкачественность таблеток оценивали на основании качественных и количественных характеристик. Оценка качества полученных таблеток проводилась по следующим показателям: внешний вид, качественное и количественное содержание ДВ, отклонение от средней массы, механическая прочность, истираемость, распадаемость, значение рН водного раствора, микробиологическая чистота, контроль антимикробной и противогрибковой активности (данные представлены в таблицах 4, 5).
Рис. 5. Технологическая схема изготовления гранул и таблеток состава 29-2 с использованием метода влажного гранулирования

Таблица 4
Результаты анализа таблеток состава 29-2, полученных методом влажного гранулирования, при выпуске
Показатели | № серии | ||
01 | 02 | 03 | |
Описание | Таблетки белого цвета | ||
Подлинность٭ | Соответствует | ||
Средняя масса (от 1,425 до 1,575 г) | 1,498 | 1,504 | 1,502 |
Отклонение от средней массы (1,5±5%) | Соответствует | ||
Содержание ДВ с±∆с, % | 100,53±4,84 | 100,21±3,98 | 99,76±4,23 |
Содержание ДВ с±∆с, г/л | 4,0212±0,1960 | 4,0084±0,1595 | 3,9904±0,1688 |
Механическая прочность на сжатие, Н (Хср±ΔХ, n=6) | 46,5±3,2 | 44,3±2,1 | 47,1±3,9 |
Коэфф. пресс., г/см (Кпр. ср. ±Δ Кпр, n=6) | 2,01±0,04 | 1,98±0,05 | 2,02±0,06 |
Истираемость, % (Хср±ΔХ, n=6) | 99,5±0,1 | 99,4±0,2 | 99,5±0,2 |
Остаточная влажность, % (Хср±ΔХ, n=6) | 1,40±0,09 | 1,40±0,10 | 1,38±0,13 |
Распадаемость, с (tср±Δt, n=6) | 116±6 | 121±7 | 112±5 |
рН Хср±ΔХ, n=6 | 5,5±0,1 | 5,6±0,2 | 5,5±0,1 |
Примечание: * – взаимодействие с реактивом на гуанидиновую группу с образованием соединения, окрашенного в розовый цвет; ТСХ – соответствие свидетелю
Таблица 5
Показатели качества таблеток состава 29-2, полученных методом влажного гранулирования, при хранении в естественных условиях в течение 1 года и при хранении по методу ускоренного старения (при температуре 40±1°С)
№ серии | Срок хранения, год | Описание | Подлинность* | Средняя масса от 1,425 до 1,575 г | Отклонение от средней массы 1,5±5% | Содержание ДВ с±∆с, % | Содержание ДВ с±∆с, г/л | Механическая прочность на сжатие, Н (Хср±ΔХ, n=6) | Истираемость, % (Хср±ΔХ, n=6) | Остаточная влажность, % (Хср±ΔХ, n=6) | Распадаемость, с (tср±Δt, n=6) | рН Хср±ΔХ, n=6 |
Хранение в течение 1 года в естественны условиях | ||||||||||||
01 | 0 | Таблетки белого цвета | Соотв. | 1,498 | Соотв. | 100,53±4,87 | 4,0212±0,1960 | 46,5±3,2 | 99,5±0,1 | 1,40±0,09 | 116±6 | 5,5±0,1 |
0,5 | −//− | 1,497 | −//− | 99,73±4,26 | 3,9892±0,1699 | 51,2±4,1 | 99,7±0,1 | 1,38±0,10 | 125±8 | 5,5±0,2 | ||
1,0 | −//− | 1,496 | −//− | 100,37±4,63 | 4,0148±0,1859 | 44,2±2,9 | 99,5±0,2 | 1,44±0,12 | 122±6 | 5,5±0,1 | ||
02 | 0 | Таблетки белого цвета | Соотв. | 1,504 | Соотв. | 100,21±3,98 | 4,0084±0,1595 | 44,3±2,1 | 99,4±0,2 | 1,40±0,10 | 121±7 | 5,6±0,2 |
0,5 | −//− | 1,501 | −//− | 100,49±4,53 | 4,0196±0,1821 | 46,3±2,9 | 99,6±0,3 | 1,37±0,05 | 118±5 | 5,5±0,1 | ||
1,0 | −//− | 1,500 | −//− | 100,34±4,71 | 4,0136±0,1890 | 45,7±3,4 | 99,8±0,1 | 1,36±0,06 | 120±4 | 5,5±0,1 | ||
03 | 0 | Таблетки белого цвета | Соотв. | 1,502 | Соотв. | 99,76±4,23 | 3,9904±0,1688 | 47,1±3,9 | 99,7±0,2 | 1,38±0,13 | 112±5 | 5,5±0,1 |
0,5 | −//− | 1,500 | −//− | 100,22±4,60 | 4,0088±0,1844 | 50,2±3,0 | 99,6±0,2 | 1,38±0,10 | 119±7 | 5,5±0,1 | ||
1,0 | −//− | 1,506 | −//− | 99,84±3,88 | 3,9936±0,1550 | 47,3±3,5 | 99,8±0,3 | 1,42±0,11 | 118±7 | 5,6±0,2 | ||
Хранение по методу ускоренного старения (при температуре 40±1°С) | ||||||||||||
01 | 0 | Таблетки белого цвета | Соотв. | 1,498 | Соотв. | 100,53±4,84 | 4,0212±0,1960 | 46,5±3,2 | 99,5±0,1 | 1,40±0,09 | 116±6 | 5,5±0,1 |
0,5 | −//− | 1,497 | −//− | 99,87±4,37 | 3,9948±0,1746 | 45,2±2,9 | 99,6±0,1 | 1,42±0,10 | 118±5 | 5,5±0,1 | ||
1,0 | −//− | 1,498 | −//− | 100,24±3,82 | 4,0096±0,1532 | 47,4±3,4 | 99,5±0,2 | 1,40±0,09 | 113±6 | 5,5±0,2 | ||
1,5 | −//− | 1,498 | −//− | 100,12±4,78 | 4,0048±0,1914 | 46,5±4,1 | 99,5±0,1 | 1,40±0,12 | 121±6 | 5,4±0,1 | ||
2,0 | −//− | 1,497 | −//− | 99,27±3,95 | 3,9708±0.1568 | 45,8±3,6 | 99,6±0,2 | 1,41±0,07 | 119±5 | 5,5±0,1 | ||
02 | 0 | Таблетки белого цвета | Соотв. | 1,504 | Соотв. | 100,21±3,98 | 4,0084±0,1595 | 44,3±2,1 | 99,4±0,2 | 1,40±0,10 | 121±7 | 5,6±0,2 |
0,5 | −//− | 1,502 | −//− | 100,06±4,03 | 4,0024±0,1613 | 44,6±3,2 | 99,4±0,1 | 1,40±0,13 | 127±5 | 5,5±0,1 | ||
1,0 | −//− | 1,502 | −//− | 100,44±4,37 | 4,0176±0,1756 | 43,4±3,0 | 99,3±0,3 | 1,40±0,10 | 122±6 | 5,6±0,2 | ||
1,5 | −//− | 1,503 | −//− | 100,32±4,56 | 4,0128±0,1830 | 45,1±2,4 | 99,5±0,2 | 1,42±0,09 | 125±5 | 5,4±0,2 | ||
2,0 | −//− | 1,502 | −//− | 100,41±4,62 | 4,0164±0,1856 | 44,0±3,5 | 99,2±0,3 | 1,43±0,12 | 125±7 | 5,5±0,1 | ||
03 | 0 | Таблетки белого цвета | Соотв. | 1,502 | Соотв. | 99,76±4,23 | 3,9904±0,1688 | 47,1±3,9 | 99,5±0,2 | 1,38±0,13 | 112±5 | 5,5±0,1 |
0,5 | −//− | 1,502 | −//− | 99,47±4,58 | 3,9788±0,1822 | 46,7±3,1 | 99,7±0,2 | 1,37±0,07 | 131±6 | 5,4±0,2 | ||
1,0 | −//− | 1,501 | −//− | 99,72±3,71 | 3,9888±0,1480 | 47,1±2,5 | 99,4±0,2 | 1,38±0,12 | 123±4 | 5,4±0,1 | ||
1,5 | −//− | 1,502 | −//− | 99,89±4,82 | 3,9956±0,1926 | 47,3±1,8 | 99,4±0,1 | 1,40±0,13 | 120±7 | 5,5±0,3 | ||
2,0 | −//− | 1,502 | −//− | 99,58±4,39 | 3,9832±0,1748 | 47,7±2,4 | 99,6±0,3 | 1,38±0,10 | 118±4 | 5,5±0,2 | ||
Анализ технологических характеристик, полученных при хранении быстрорастворимых таблеток по методу ускоренного старения (при температуре 40±1°С в течение 182 суток), показал, что таблетки состава 29-2 выдерживают хранение в течение двух лет. Срок наблюдения за таблетками, хранившимися в естественных условиях, составил 1 год. Таблетки характеризуются постоянством: основных технологических характеристик, качественного и количественного содержания действующего вещества в течение всего срока хранения (таблица 5), а также соответствуют требованиям ГФ XI «Испытание на микробиологическую чистоту» и Изм. №3, сохраняют фунгицидное и бактерицидное действие. Полученные данные позволяют рекомендовать срок хранения таблеток состава 29-2, расфасованных в полимерные банки, в сухом, защищенном от света месте при температуре 15-25°С в течение 1 года (срок наблюдения).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



