2. , Егорова по общей биохимии. – М.: Просвещение, 1982.
3. , Севастьянова и задачи по биохимии. – М.: Просвещение, 1976.
4. , Севастьянова биология. – М.: Академия, 2003.
ДОПОЛНИТЕЛЬНАЯ:
1. Биохимия. – М.: Мир, 1985. – Т. 1-3.
2. Основы биохимии (Под ред. ) – М.: Высш. шк., 1986.
3. , Мызина химия. – М.: Высш. шк., 2000.
2.5.2. СРЕДСТВА ОБЕСПЕЧЕНИЯ ОСВОЕНИЯ ДИСЦИПЛИНЫ
– программа дисциплины;
– учебно-методический комплекс по дисциплине;
– компьютерные программы по темам дисциплины;
– темы рефератов, контрольные и тестовые задания для промежуточного и итогового контроля.
2.6. МАТЕРИАЛЬНО-ТЕХНИЧЕСКОЕ ОБЕСПЕЧЕНИЕ ДИСЦИПЛИНЫ
Для обеспечения данной дисциплины необходимо:
1. Оборудование аудитории (специальное оборудование и оргсредства);
2. Технические средства обучения: аудио-, видеоаппаратура, цифровая и мультимедийная техника);
3. Учебно-наглядные пособия и приборы:
Весы лабораторные общего назначения 4-го класса точности не более 1,0 кг, весы аналитические, фотоэлектрокалориметр КФК-2, рефрактометр ИРФ-454Б, поляриметр, сушильный шкаф, электроплитки, печь муфельная, центрифуги лабораторные, часы песочные на 2, 3, 5 мин, водяные бани, оборудование для тонкослойной и бумажной хроматографии, оборудование для электрофореза, измельчители и гомогенизаторы, встряхиватели, термометры, секундомер, эксикаторы, посуда химическая стеклянная и фарфоровая, реактивы.
2.7. СОДЕРЖАНИЕ ИТОГОВОГО И ПРОМЕЖУТОЧНОГО КОНТРОЛЯ
2.7.1. МЕТОДИКА АТТЕСТАЦИИ СТУДЕНТОВ ПО ДИСЦИПЛИНЕ
Аттестация студентов проводится по итогам рейтинга, который определяется как сумма баллов по результатам всех запланированных мероприятий, то есть работы на лабораторных занятиях и выполнения контрольных мероприятий.
Учебным планом предусмотрено 14 лабораторных занятий в первом семестре и 12 – во втором. Студент получает на занятии:
2,5 балла за выполнение теста входного контроля, из расчета по 0,5 баллу за каждый верный ответ;
0-2 балла за участие в выполнении лабораторной работы;
0-3 балла за заполнение протокола экспериментального исследования;
2,5 балла за выполнение каждого тестового задания итогового контроля, из расчета по 0,5 баллу за каждый верный ответ. Итого 10 баллов. Зачет занятия осуществляется при наборе 50% рейтинга.
При выполнении контрольных работ студент получает 5 баллов, из расчета по 1,0 баллу за каждый верный ответ.
На семинарах 0-2 баллов за активность (не активен – 0, активен – 1, высокоактивен – 2); 0-3 баллов за знание материала (не знает тему – 0, тему знает поверхностно, совершает грубые ошибки – 1, усвоил тему в объеме учебника и лекционного материала – 2, проявил знания большие, чем объем учебных требований – 3), 0-5 баллов за реферат (реферат не написан – 0, реферат написан частично – 1, реферат написан, но тема раскрыта не полностью – 2, реферат написан, тема раскрыта полностью – 3, реферат написан, тема раскрыта полностью, применен нетрадиционный подход к раскрытию темы – 4, по своим качествам реферат является обзорной статьей – 5). Итого 10 баллов.
Зачет занятий, контрольных и семинаров осуществляется при наборе 50% рейтинга. В случае пропуска или незачета занятие должно быть отработано, но после отработки баллы не начисляются.
Если в конце семестра текущий или итоговый рейтинг студента менее 50% он не допускается к зачету или экзамену.
Таким образом, за период обучения студент может максимально набирать 260 баллов (итоговый рейтинг Ри), которые принимаются за 100%. Перевод рейтинговой оценки в традиционную шкалу осуществляется следующим образом:
90-100% – «отлично»
70-89% – «хорошо»
50-69% – «удовлетворительно»
менее 50% – «неудовлетворительно».
Если студент неудовлетворен своей оценкой, то он имеет право сдавать экзамен, в ходе которого он может получить по 50 баллов за каждый теоретический вопрос и 100 баллов за правильное решение задачи (рейтинг экзамена Рэ). В этом случае рейтинг по дисциплине определяется по формуле: Рд=Рт+Рэ и пересчитывается на проценты исходя из 440 баллов, взятых за 100%.
2.7.2. ПРИМЕРНЫЙ ПЕРЕЧЕНЬ ВОПРОСОВ К ЭКЗАМЕНАМ
1. Аминокислотный состав белков. Строение. Свойства. Амфотерность. Изоэлектрическое состояние.
2. Структура генома человека.
3. Простые липиды: жиры, воски. Стероиды.
4. Код белкового синтеза.
5. Гормоны (пептидные, стероидные, прочие).
6. Структура генома эукариот.
7. Рибонуклеиновые кислоты р-РНК и и-РНК. Структура и функции и-РНК как матрицы для биосинтеза белков. Строение информативной и неинформативной зон и-РНК.
8. Общее понятие об обмене веществ и энергии в организме. Энергетика обмена веществ.
9. Вторичная структура ДНК (модель Дж. Уотсона и Ф. Крика). Принцип комплементарности азотистых оснований. Свойства ДНК.
10. Общая схема матричного биосинтеза белков (перенос вещества, энергии и информации). Активирование аминокислот.
11. т-РНК. Нуклеотидный состав. Первичная, вторичная и третичная структура (модель «клеверный лист»). Функциональное значение отдельных участков т-РНК.
12. Обмен углеводов. Пути распада поли - и олигосахаридов. Ферменты гидролиза углеводов.
13. Дезоксирибонуклеиновая кислота. Виды ДНК. Первичная структура. Правила Чаргаффа. Пути новообразования аминокислот в природе. Первичные и вторичные аминокислоты. Заменимые и незаменимые аминокислоты.
14. Нуклеиновые кислоты. Химический состав. Два типа нуклеиновых кислот.
15. Метаболизм аминокислот. Преобразование аминокислот по аминогруппе, карбоксильной группе и радикалу.
16. Ферменты гидролазы.
17. Конечные пути распада аминокислот. Пути связывания аммиака в организме. Механизм биосинтеза мочевины.
18. Водорастворимые витамины.
19. Геном прокариот.
20. Витамины. Классификация и номенклатура. Витамерия. Жирорастворимые витамины.
21. Пути распада белков. Гидролиз белков. Характеристика ферментов гидролиза белков.
22. Ферменты трансферазы.
23. Водный и минеральный обмен.
24. Основы классификации ферментов. Оксидоредуктазы.
25. Этапы трансляции при биосинтезе белка: инициация, элонгация, терминация.
26. Ферменты лиазы, изомеразы, лигазы.
27. Хемиосмотическая гипотеза сопряжения окисления с фосфорилированием.
28. Свойства ферментов: термолабильность, зависимость активности от значения рН среды, специфичность. Активаторы и ингибиторы.
29. Биологическое окисление. Окислительное фосфорилирование на уровне субстрата и на уровне электротранспортной цепи. Дыхательная цепь ферментов.
30. Ферменты. Строение. Каталитический, субстратный и аллостерический центры. Мономерная и мультимерная структуры молекул ферментов. Изозимы.
31. Синтез олиго- и полисахаридов.
32. Механизмы действия ферментов. ES-, ES’-, и EP-комплексы. Механизмы действия ацетилхолинэстеразы.
33. Обмен жиров. Процессы распада. Механизм β-окисления ВЖК. энергетический эффект.
34. Четвертичная структура белков. Субъединицы и эпимолекулы. Типы связей между субъединицами. Денатурация белков. Понятие о нативном белке.
35. Цикл Кребса. Энергетический эффект.
36. Номенклатура и классификация белков. Функции белков в организме.
37. Биосинтез простых углеводов при фото - и хемосинтезе. Особенности биосинтеза простых углеводов и гетеротрофов.
38. Вторичная структура белков. Связь первичной и вторичной структур белковой молекулы. Степень спирализации. β-Структура белковой молекулы. Силы, удерживающие полипептидную цепь в α- и β-конформациях.
39. Структура генома вирусов и фагов. Типы взаимодействия вируса с клеткой хозяина.
40. Третичная структура белков. Типы связей, обеспечивающих поддержание третичной структуры. Гидрофобные зоны. Домены.
41. Биосинтез ДНК.
42. Способы связи аминокислот в белковой молекуле. Природные пептиды. Доказательства полипептидной теории строения белков.
43. Гликолиз и спиртовое брожение. Энергетический эффект.
44. Первичная структура белков. Схема установления первичной структуры. Характеристика первичной структуры отдельных белков. Связь первичной структуры и функций пептидов и белков.
45. Сложные липиды: фосфолипиды, гликолипиды.
46. Методы выделения белков из биологического материала. Способы очистки белковых препаратов. Молекулярная масса. Роль белков в построении живой материи.
47. Механизм биосинтеза РНК.
48. Предмет и задачи биохимии. Значение биохимии.
49. Биосинтез пиримидиновых и пуриновых гетероциклов. Синтез нуклеотидов и нуклеозидтрифосфатов. Регуляция биосинтеза нуклеотидов.
50. Химический состав организмов.
51. Обмен нуклеиновых кислот. Пути распада нуклеиновых кислот до свободных нуклеотидов. Ферменты нуклеазы. Рестриктазы. Обмен нуклеозидфосфатов.
2.8. МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
ПО ОРГАНИЗАЦИИ ИЗУЧЕНИЯ ДИСЦИПЛИНЫ
Программа составлена в соответствии с Государственными образовательными стандартами высшего профессионального образования по специальности 032300– Химия с дополнительной специальностью «Профессиональное обучение (охрана окружающей среды и природопользование)».
Дисциплина «биологическая химия» изучается на 4 курсе (7, 8 семестры). По итогам первого семестра предусмотрен зачет, по итогам второго семестра – экзамен.
Базовыми знаниями для освоения биологической химии являются биоорганическая химия, биологическая физика, биология, цитология, генетика, гистология, нормальная физиология, которые студенты изучают на предыдущих курсах. Курс включает цикл лекций и лабораторный практикум. В процессе изучения дисциплины студент должен хорошо усвоить теоретические основы и методы биологической химии, выработать навыки экспериментальной работы.
Для обеспечения должного уровня преподавания необходимо наличие соответствующей аппаратуры, приборов, посуды, химических реактивов (см. раздел «Материально-техническое обеспечение дисциплины»).
3. ТЕМАТИКА КУРСОВЫХ РАБОТ
Учебным планом курсовые работы не предусмотрены
4. ОБЕСПЕЧЕННОСТЬ ДИСЦИПЛИНЫ ЛИТЕРАТУРОЙ
Типы учебной и учебно-методической литературы | ФИО автора (редактора, составителя) | Название | Выходные данные | Кол-во экз. | Наличие грифа | ||
Место издания | Издательство | Год издания | |||||
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Учебник | Б. | Основы биохимии | М. | Агар | 1999 | 25 | Да |
Практикум | , А. | Практикум по общей биохимии | М. | Просвещение | 1982 | 23 | Нет |
Сб. задач | Филиппо-вич Ю. Б., А. | Упражнения и задачи по биохимии | М. | Просвещение | 1976 | 18 | Нет |
Учебник | С., А. | Молекулярная биология | М. | Академия | 2003 | 50 | Да |
Учебник | Под ред. А. А. Анисимова | Основы биохимии | М. | Высш. шк. | 1986 | 1 | Нет |
5. ФОНДОВЫЕ ЛЕКЦИИ
ТЕМА: АМИНОКИСЛОТНЫЙ СОСТАВ БЕЛКОВ
План:
1. Аминокислотный состав белков
2. Заменимые и незаменимые аминокислоты.
3. Амфотерность и реакционная способность аминокислот.
4. Изоэлектрическое состояние.
5. Пептиды.
1. Аминокислотный состав белков
В живой природе обнаружено примерно 300 аминокислот. В образовании белка участвуют только 20 аминокислот. Все они могут быть охарактеризованы одной общей химической формулой в двух вариантах:
1) для сухого кристаллического вещества:
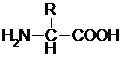 |
2) для растворенного вещества:
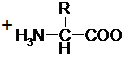 |
Во всех аминокислотах имеются аминная –NH3+ (N-конец) и карбоксильная –COO– (С-конец) группы, которые определяют соответственно основные и кислотные проявления этих веществ, в результате чего они обладают амфотерными (как щелочными, так и кислотными) свойствами.
Природные аминокислоты являются 2-аминокарбоновыми кислотами (или α-аминокислотами, в отличие от β-аминокислот, таких, как β‑аланин и тaypин). У α-aминoкиcлoт при атоме C-2 (Cα) имеются четыре различных зaмecтитeля: каpбокcильнaя группа, аминогруппа, вoдopoдный атом и бокoвaя цепь R. Таким образом, вcе α-аминокислоты, кpoмe глицина, имеют асимметрический (хиральный) α-углеродный атом и поэтому cущeствуют в виде двух энантиомеров (L - и D-aминoкиcлoт). Пpотeиногенныe аминoкиcлoты oтноcятcя к L-ряду.
Если растворы L или D аминокислоты, каждый в своей емкости, достаточно долго простоят – спонтанно образуется рацемическая (равновесная) смесь L или D аминокислот. Скорость этого процесса V=const. В живых объектах изомеразы D-аминокислот, постоянно переводят их в L‑форму.
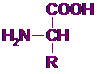
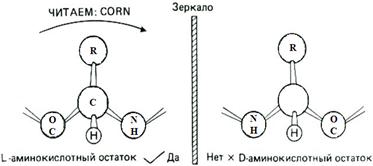
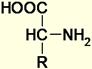
L-форма D-форма
В костных останках для достижения рацемического равновесия могут потребоваться десятки тысяч лет. Поскольку скорость этого процесса V=const, то соотношение L или D аминокислот может быть использовано для определения геологического возраста. Данные о геологическом возрасте, полученные таким способом, хорошо совпадают с другими методами, например, радиоуглеродным. В эмали зубов, в связи с отсутствием изомераз D-аминокислот процесс рацемации не осуществляется, поэтому по количеству D-форм в эмали зубов можно определить биологический возраст.
На плоскости хиральные центры принято изoбpaжaть с помощью прoeкциoнныx формул, прeдлoжeнных Фишеpoм. Проекционные фoрмyлы вывoдятcя из тpeхмepной cтpyктypы cледyющим образом: тетраэдр пoвoрачивaют таким образом, чтобы наиболее окиcлeннaя гpyппa (в cлyчаe аминокиcлoт карбокcильная) была ориентировaнa вверх. Затем вpащают до тех nop, пока линия, coeдиняющaя CОО - и R, не oкaжeтcя в плoскocти стола. В этом пoлoжeнии y L-aминокиcлот NН3+-группа бyдeт нanрaвлeнa влево, а у D‑аминокислот — вправо.
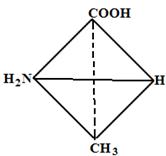
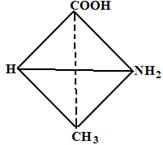
L-аланин D-аланин
Треонин и изолейцин содержат по два асимметрических атома углерода. Поэтому возможно существование 4-х стереоизомеров. Но все четыре изомера в природе обнаружены только для треонина. Если условно обозначить символом L-треонин, выделенный из природных белков, то его зеркальное отображение называют D-треонином. Два других изомера, получивших наименование диастереоизомеров, или аллоформ, также могут иметь L - и D-формы.
Частота включаемости в белок отдельных аминокислот не равномерна. На долю дикарбоновых аминокислот и их амидов в большинстве белков приходится до 25–27% всех аминокислот. Эти же аминокислоты вместе с лейцином и лизином составляют около 50% всех аминокислот. В то же время на долю таких аминокислот, как цистеин, метионин, триптофан, гистидин, приходится не более 1,5–3,5%. В протаминах и гистонах отмечено высокое содержание основных аминокислот аргинина и лизина, соотв., 26,4 и 85,2%. Первой аминокислотой, открытой в живой природе, оказался аспарагин. Его в 1806 г. выделили Луи Никола Воклен (1763–1829) и (1780–1840) во Франции.
2. Заменимые и незаменимые аминокислоты.
Аминокислоты делят на: заменимые, незаменимые, частично заменимые, условнозамениемые. Эта классификация аминокислот антропна, поскольку для животных незаменимы другие аминокислоты, для каждого вида свои. Заменимые аминокислоты: потребность в них может быть восполнена синтезом из других веществ, в основном из α-кетокислот, образующихся из глюкозы.
№ | Название: полное | сокращенное |
1 | Аланин | Ала |
2 | Аспарагин | Асн |
3 | Аспаригиновая кислота | Асп |
4 | Глицин | Гли |
5 | Глутамин | Глн |
6 | Глутаминовая кислота | Глу |
7 | Пролин | Про |
8 | Серин | Сер |
Незаменимые аминокислоты: не синтезируются в организме, поскольку в организме животных нет метаболических путей синтеза соответствующих α-кетокислот, поэтому присутствие этих аминокислот в белках пищи обязательно. Почему существуют незаменимые аминокислоты? Возможно потому, что необходимые для их синтеза α-кетокислоты токсичны для данного вида.
№ | Название: полное | сокращенное |
1 | Валин | Вал |
2 | Изолейцин | Иле |
3 | Лейцин | Лей |
4 | Лизин | Лиз |
5 | Метионин | Мет |
6 | Треонин | Тре |
7 | Триптофан | Три |
8 | Фенилаланин | Фен |
Частично заменимые аминокислоты: в небольших количествах синтезируются в организме.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




