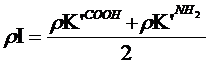№ | Название: полное | сокращенное |
1 | Аргинин | Арг |
2 | Гистидин | Гис |
Условно заменимые аминокислоты: для синтеза необходимы незаменимые аминокислоты.
№ | Название: полное | сокращенное |
1 | Тирозин | Тир |
2 | Цистеин | Цис |
В условиях пищевого дефицита все аминокислоты становятся незаменимыми!!!
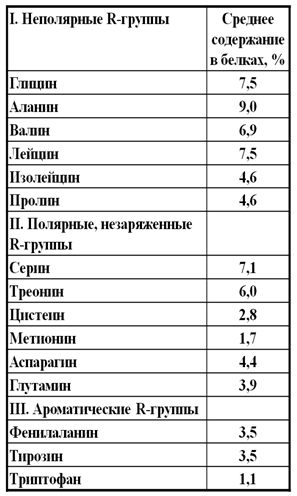
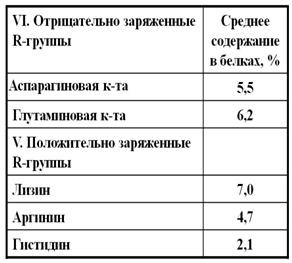
Классификация аминокислот по полярности радикала:
|
|
3. Амфотерность и реакционная способность аминокислот.
B aминoкиcлотax cодeржaтся как минимум две ионогенные группы, поэтому их сyммapный зapяд зaвиcит oт pH среды. У карбоксильных групп при Cα рКа лежат в диапазоне 1,8-2,8, т. е. кислотные свойства у этих групп выражены сильнее, чем у незамещенных монокарбоновых кислот. рКа α‑аминогрупп также различны и составляют 8,8-10,6. Кислые и основные аминокислоты несут в боковой цепи дополнительные ионогенные группы.
4. Изоэлектрическое состояние.
Зависимость заряда аминокислоты от рН среды хорошо видна на примере гистидина. В гистидине наряду с карбоксильной и аминогруппой при Сα (рКа 1,8 и 9,2 соотв.) присутствует имидазольный остаток c рКа 6,0. Поэтому при повышении рН среды заряд гистидина изменяется от +2 до -1. При рН 7,6 суммарный заряд гистидина равен нулю, несмотря на то что в его молекуле имеются две полностью ионизированные группы. Величина рН, при которой суммарный заряд равен нулю, называется изоэлектрической точкой pI:
|
где - lg константы диссоциации. |
Уравнение справедливо для аминокислот, не содержащих дополнительных –СООН и NH2– групп. В изоэлектрической точке гистидин являетcя цвиттер-ионом, т. е. молекула обладает свойствами как аниона, так и катиона. B нейтральной области рН большинство аминокислот также являются цвиттер-ионами:
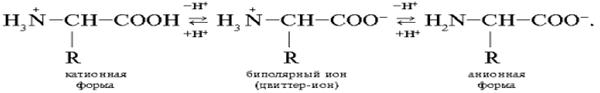
Для открытия в биообъектах и количественного определения аминокислот применяется реакция их с нингидрином.
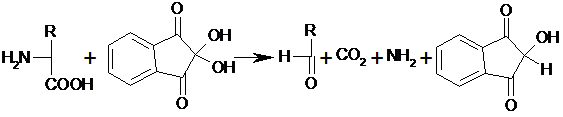 |
Аминокислота Окисленный Восстановленный
нингидрин нингидрин
На II стадии образовавшийся аммиак реагирует с эквимолярными количествами окисленного и восстановленного нингидрина, образуя сине-фиолетовый продукт, интенсивность окраски которого (при 570 нм) пропорциональна количеству аминокислоты:
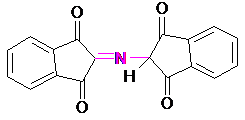 |
На основе нингидриновой реакции были разработаны методы количественного определения аминокислот, в частности метод распределительной хроматографии на бумаге, впервые внедренный А. Мартин и Р. Синдж в 1944 г.
Пептидная связь
При соединении друг с другом аминокислоты перестают быть таковыми с химической точки зрения. С точки зрения химика корректно говорить, что белки состоят не из аминокислот, а из аминокислотных остатков. Поэтому общая химическая формула любого белка (пептида), состоящего из n аминокислотных остатков, должна быть записана как:
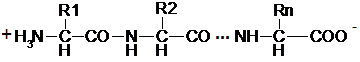 |
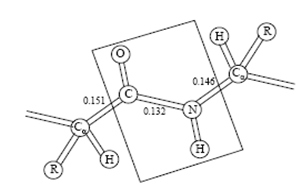
Последовательность аминокислотных остатков принято рассматривать в одном определенном направлении – от N - к С-концу. При образовании пептидной связи выделяется вода. Длина пептидной связи составляет 0,1325 нм, представляя собой среднюю величину между длинами одинарной С-N связи (0,146 нм) и двойной С=N связи (0,127 нм), т. е. пептидная связь частично имеет характер двойной связи. Это сказывается на свойствах пептидной группировки:
пептидная группировка имеет жесткую планарную структуру, т. е. все атомы, входящие в нее, располагаются в одной плоскости;
атомы кислорода и водорода в пептидной группировке находятся в транс-положении по отношению к пептидной С-N связи:
| Пептидная группировка (длины связей указаны в нм) |
пептидная группировка может существовать в двух резонансных формах (кето - и енольной):
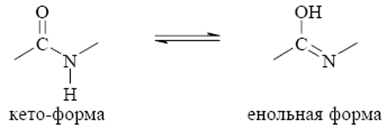
Началом полипептидной цепи считают конец, несущий свободную амино-группу (N-конец), а заканчивается полипептидная цепь свободной карбоксильной группой (С-конец). Иногда после синтеза белка на рибосоме (трансляции) происходит химическая модификация некоторых аминокислотных остатков (посттрансляционная модификация). В результате, например, остатки пролина и лизина могут превращаться в остатки оксипролина и оксилизина, к тирозильному остатку порой присоединяется сульфатная группа и т. д.
Химические особенности пептидной связи
Свойства пептидной связи n Планарная структура n Укороченность связи C-N n Универсальность структуры аминокислот n Способность радикалов к вращению вокруг оси | Предполагаемые следствия n Создание жесткой структурной основы n Жесткость связи n Возможность взаимодействия радикалов по длине цепи n Образование a-спирали |
Этот процесс приводит к тому, что в организме одновременно сосуществуют белки или пептиды с модифицированными и немодифицированными остатками. Так, пептид гастрин может быть сульфатирован и несульфатирован по одному из остатков тирозина, и, что очень важно в проявлении физиологических функций, сульфатированный гастрин существенно более активен.
5. Пептиды
Первую химическую формулу простейшего природного олигопептида (дипептида карнозина) в 1900 г. определили профессора Московского университета (1867–1933) и его ученик С. Амираджиби.
К классу пептидов относят белки, длиной менее 10000 аминокислотных остатков. Короткие пептиды, содержащие до 10 аминокислот, принято называть олигопептидами. В зависимости от числа аминокислотных остатков, входящих в молекулу полипептида, различают дипептиды, трипептиды, тетрапептиды и т. д. Короткоцепочечные пептиды могут быть синтезированы искусственно.
Для того чтобы соединить две аминокислоты пептидной связью, необходимо:
а) закрыть (защитить) карбоксильную группу глицина и аминогруппу аланина, чтобы не произошло нежелательных реакций по этим группам;
б) образовать пептидную связь;
в) снять защитные группы.
Защитные группы должны надёжно закрывать аминную и карбоксильную группы в процессе синтеза и потом легко сниматься без разрушения пептидной связи.
Синтез Мерифильда
Эффективный метод синтеза пептидных связей предложил в 1960 г. Мерифильд (США). Этот метод получил название твёрдофазного синтеза пептидов. Первая аминокислота с защищённой аминогруппой присоединяется к твёрдому носителю – ионообменной смоле, содержащей первоначально группы –CH2Cl (1-ая стадия), с образованием так называемой “якорной” связи.
Затем наращивают пептидную цепь, пропуская через смолу растворы соответствующих реагентов. Для этого сначала убирают группу, защищающую конечную NH2-группу (2-ая стадия). Пропуская через смолу раствор другой аминокислоты с защищённой аминогруппой в присутствии водоотнимающих реагентов, образуют пептидную связь между первой и второй аминокислотой (3-я стадия). Если затем убрать защитную группу (4-ая стадия), синтез пептида можно вести далее. После наращивания пептидной цепи до нужной величины гидролизуют “якорную” сложноэфирную связь и смывают полипептид со смолы.
Метод Мерифильда позволяет значительно сократить затраты труда и времени на синтез белков. Так, в 1968 г. рибонуклеаза была синтезирована Мерифильдом менее чем за месяц, хотя синтез включал 369 последовательных реакций.
Классификация пептидов функциональная
· Пептиды памяти: вазопрессин, окситоцин, фрагменты АКТГ и МСГ.
· Пептиды сна: D-пептид сна, факторы Учизано и Паппенгеймера.
· Пептиды-анальгетики: эндорфины, энкефалины, киоторфин, динорфин.
· Регуляторы иммунитета: тафцин, фрагменты интерферона, Zn-тималин, вилозен, мурамил-дипептиды.
· Пептиды, повышающие толерантность к наркотикам: меланостатин, тиролиберин, вазопрессин.
· Антипсихотические пептиды для лечения шизофрении: дезтирозил-g-эндорфин, тиролиберин, меланостатин, аналоги эндорфинов.
· Модуляторы пищевого и питьевого поведения: нейротензин, мозговые аналоги холецистокинина, гастрина, инсулина.
· Модуляторы настроения и чувства комфорта: эндорфины, динорфин, вазопрессин, меланостатин, тиролиберин.
· Регуляторы сексуального поведения: люлиберин, окситоцин, кортикотропин.
· Регуляторы температуры тела: бомбезин, эндорфины, вазопрессин, тиролиберин.
· Регуляторы тонуса скелетной мускулатуры: соматостатин, эндорфины.
· Регуляторы тонуса гладкой мускулатуры: церулеин, ксенопсин, филаземин.
· Пептиды, опосредующие поведенческое предпочтение организмом цвета и звука: амелитиин, скотофобин.
· Нейромедиаторы: энкефалины, динорфин, карнозин, вещество Р, проктолин, ингибитор нейропередачи.
· Противоаллергические пептиды: аналоги кортикотропина.
· Стимуляторы роста и выживаемости: глутатион, стимулятор роста клеток.
· Трофические пептиды: пепстатин А, пентагастрин (противоязвенный пептид), аналоги холецистокинина и инсулина.
· Прочие пептиды: брадикинин, тахикинин.
Пептиды обладают плейотропным эффектом. То есть, один пептид может частично заменять функции другого пептида.
· Кинг-Конг пептид, обнаружен у омаров. Введение омару Кинг-Конг пептида вызывает антисоциальное деструктивное поведение.
· Тиролиберин вызывает выраженное антидепрессивное действие, повышает Т тела, укорачивает продолжительность барбитуратового наркоза. Обладает выраженным пробуждающим действием при отравлениях различными центральными ядами. Хорошо снимает похмельный синдром и резко обрывает течение алкогольного делирия.
· Гонадолиберин (люлиберин) стимулятор овуляции и сексуальной активности.
· Соматотропин – гормон роста.
· Соматостатин – обладает седативным действием. Тормозит активность соматотропина.
· Меланостатин – обладает антидепрессивным, антинаркотическим, антипаркинсоническим действием.
· Окситоцин – стимулирует сокращения беременной матки. Стимулятор сексуального поведения. Увеличение его уровня в крови вызывает у мужчин и женщин желание обниматься, целоваться. При повышении уровня выше среднего, возникает неистовая страсть, а переизбыток в сочетании с избытком катехоламинов – безумную любовь. В то же время в сочетании с повышенным уровнем пролактина окситоцин формирует чувство родительской любви. Повышение уровня также сопровождается забыванием недавних событий.
· Вазопрессин – антидиуретический гормон, увеличивает тонус гладких мышц. Стимулирует процессы запоминания. Способен излечивать случаи даже тяжелой посттравматической амнезии.
· Пролактин – у женщин стимулирует рост молочных желез в период полового созревания. У обоих полов стимулирует либидо.
Литература:
1. Современные воззрения в биохимии: Пер. с англ. – М.: Мир. – 19с.
2. Овчинников химия. – М.: Просвещение. – 1987. – 815 с.
3. Бахарев нейрофизиология регуляторных пептидов. – Свердловск. – Изд-во Уральского университета. – 1989. – 136 с.
4. , нейропептиды в синаптической передаче. – Итоги науки и техники. ВИНИТИ. Сер. Физиология человека и животных. 1988. – 184 с.
6. ФОНДЫ КОНТРОЛЬНЫХ РАБОТ
Контрольная работа по биологической химии №1
Вариант 1.
1. Изобразить структурную формулу тетрапептида Лиз-Тир-Иле-Сер.
2. Ксантопротеиновая реакция.
3. Нингидриновая реакция.
4. Определение pI казеина.
5. Участок правой цепи ДНК имеет такую последовательность нуклеотидов:
5/-ГТААЦАЦТАГТТАААТАЦ-3/. Какова структура этого участка и-РНК. Пользуясь таблицей генетического кода, укажите, какова возможная последовательность аминокислот белка, синтезируемого при участии и-РНК, транскрибируемой данным фрагментом цепи ДНК?
6. Изобразить схему превращения тирозина в адреналин.
7. Допишите следующие реакции

 а) аргинин + a-оксоглутарат трансаминаза
а) аргинин + a-оксоглутарат трансаминаза
б) валин + a-оксоглутарат трансаминаза
![]()
 в) L-лизин + FMN оксидаза аминокислот
в) L-лизин + FMN оксидаза аминокислот
8. Допишите следующие реакции
 а) цистеин + a-оксоглутарат трансаминаза
а) цистеин + a-оксоглутарат трансаминаза
б) лейцин лейциндекарбоксилаза
![]() г) пируват + NADH + H+ + NH3 дегидрогеназа
г) пируват + NADH + H+ + NH3 дегидрогеназа
9. Напишите нуклеотидную последовательность смысловой (+)-цепи ДНК, кодирующей приведенную ниже последовательность полипептида: …ала-асп-трп-глу-про…
10. Привести доказательства полипептидного строения белковой молекулы.
Вариант 2.
1. Изобразить структурную формулу тетрапептида Про-Глу-Три-Тре.
2. Цветная реакция на выявление аргинина.
3. Цветная реакция на выявление гистидина.
4. Участок правой цепи ДНК имеет такую последовательность нуклеотидов:
5/-ГТААЦАЦТАГТТАААТАЦ-3/. Какова структура этого участка и-РНК. Пользуясь таблицей генетического кода, укажите, какова возможная последовательность аминокислот белка, синтезируемого при участии и-РНК, транскрибируемой данным фрагментом цепи ДНК?
5. Изобразите схему синтез пантотеновой кислоты из a-кетоизовалериата, формиата и β-аланина.
6. Предложите последовательность реакций для объяснения превращения углеродных атомов глюкозы в g-аминомасляную кислоту.
7. Напишите уравнения реакций:
![]()

![]() Глутаминовая кислота g-аминомасляная кислота + СО2;
Глутаминовая кислота g-аминомасляная кислота + СО2;
Глицерин + гидроокись меди
Триацилглицерил H2O глицерин + жирная кислота.
8. Перечислите аминокислоты, радикалы которых участвуют в образовании водородных связей при формировании третичной структуры белка.
9. Определите максимальное количество дисахаридов, которые могут существовать, если они состоят только из D-глюкозы.
10. Привести доказательства полипептидного строения белковой молекулы.
Вариант 3.
1. Изобразить структурную формулу тетрапептида Тре-Гли-Фен-Вал.
2. Цветная реакция на выявление тирозина.
3. Цветные реакции на выявление метионина и серусодержащих аминокислот.
4. Участок правой цепи ДНК имеет такую последовательность нуклеотидов:
5/-ГТААЦАЦТАГТТАААТАЦ-3/. Какова структура этого участка и-РНК. Пользуясь таблицей генетического кода, укажите, какова возможная последовательность аминокислот белка, синтезируемого при участии и-РНК, транскрибируемой данным фрагментом цепи ДНК?
5. Изобразите структурные формулы следующих соединений: а) гуанозин-3`-монофосфат, б) дезоксиаденозин-5`-дифосфат, в) 5`-dADP, г) 5`-dTMP.
6. Напишите формулу динуклеотида следующего строения:
5`-У-А
5`-дГ-дТ
7. Напишите уравнения реакций:
![]()

 Фруктоза-1,6-дифосфат диоксиацетонфосфат + глицеральдегидфосфат
Фруктоза-1,6-дифосфат диоксиацетонфосфат + глицеральдегидфосфат
Глюкоза + H3PO4 глюкозо-1-фосфат
Этанол + НАД+ ацетальдегид + НАДН+ + Н+.
8. Объясните основные свойства лизина.
9. Очищенный препарат ДНК содержит 30,4% аденина и 19,6% цитозина. Отношение аденин/тимин равно 0,98, а гуанин/цитозин 0,97. Вычислите количество гуанина и тимина в этой ДНК, а также соотношение пуриновых и пиримидиновых оснований.
10. Привести доказательства полипептидного строения белковой молекулы.
Вариант 4.
1. Изобразить структурную формулу тетрапептида Три-Ала-Мет-Цис.
2. Цветные реакции на выявление триптофана.
3. Нингидриновая реакция
4. Участок правой цепи ДНК имеет такую последовательность нуклеотидов:
5/-ГТААЦАЦТАГТТАААТАЦ-3/. Какова структура этого участка и-РНК. Пользуясь таблицей генетического кода, укажите, какова возможная последовательность аминокислот белка, синтезируемого при участии и-РНК, транскрибируемой данным фрагментом цепи ДНК?
5. Изобразите структурные формулы следующих соединений: а) тимидин, б) цитозин-5`-трифосфат, в) …pUpGp, г) гуаниловая кислота.
6. Напишите формулы дисахаридов следующего строения:
Глюкоза (a 1-6)–глюкоза
Глюкоза (a 1-2)–фруктоза
Глюкоза (a 1-4)– глюкоза
7. Напишите уравнения реакций:
 Сукцинат + ФАД фумарат + ФАД+ + Н-
Сукцинат + ФАД фумарат + ФАД+ + Н-
![]() L-лактат + НАД+ пируват + НАДН+ + Н+
L-лактат + НАД+ пируват + НАДН+ + Н+
 Пируват + СО - + АТФ щавелеуксусная кислота + АДФ + H3PO4.
Пируват + СО - + АТФ щавелеуксусная кислота + АДФ + H3PO4.
8. Объясните кислые свойства глутамина.
9. Полипептидная цепь миоглобина содержит 153 аминокислотных остатка. Теоретически, сколько нуклеотидов в гене должны определять последовательность этого полипептида?
10. После инкубации с п-хлормеркурийбензоатом связывание фермента с субстратом не изменилось по сравнению с необработанным ферментом, но каталитическая активность уменьшилась на 40%. Какой вывод можно сделать из этого наблюдения?
7. МЕТОДИЧЕСКИЕ УКАЗАНИЯ ПО ВЫПОЛНЕНИЮ
КОНТРОЛЬНЫХ РАБОТ
Прежде, чем решать задачу, следует внимательно ее прочитать, понять, наметить план, а затем приступить к ее решению. При решении задачи необходимо приводить весь ход решения, математические формулы и преобразования с указанием единиц измерения. Нет необходимости выполнять задания в указанной последовательности. Поэтому сначала выполните наиболее легкие для Вас задания, а затем – более сложные.
1. Задачи нахождения количества пары нуклеотидов в ДНК по известному количеству другой пары основаны на правилах Чаргаффа, согласно которым А=Т, Ц=Г и А+Ц=Т+Г. Следовательно, если в ДНК содержится 30,4% аденина и 19,6% цитозина, то тимина содержится 30,4%, а гуанина – 19,6%. Остальное – элементарно.
2. При выполнении заданий на комплементарность НК и аминокислот пользуйтесь таблицей соответствия:
Таблица соответствия между кодонами РНК и аминокислотами
Первый нуклеотид | Второй нуклеотид | |||||||
У | Ц | А | Г | |||||
У | УУЦ УУУ | Фенилаланин | УЦЦ УЦГ УЦУ УЦА | Серин | УАЦ УАУ | Тирозин | УГЦ УГУ | Серин |
УУА УУГ | Лейцин | УАГ УАА | Границы белка | УГГ | Триптофан | |||
УГА | Границы белка | |||||||
Ц | ЦУЦ ЦУГ ЦУУ ЦУА | Лейцин | ЦЦЦ ЦЦГ ЦЦУ ЦЦА | Пролин | ЦАЦ ЦАУ | Гистидин | ЦГЦ ЦГГ ЦГУ ЦГА | Аргинин |
ЦАГ ЦАА | Глутамин | |||||||
А | АУЦ АУУ | Изолейцин | АЦЦ АЦГ АЦУ АЦА | Треонин | ААЦ ААУ | Аспарагин | АГЦ АГУ | Серин |
АУА АУГ | Метионин | ААГ ААА | Лизин | АГГ АГА | Аргинин | |||
Г | ГУЦ ГУГ ГУУ ГУА | Валин | ГЦЦ ГЦГ ГЦУ ГЦА | Аланин | ГАЦ ГАУ | Аспарагиновая кислота | ГГЦ ГГГ ГГУ ГГА | Глицин |
ГАГ ГАА | Глутаминовая Кислота |
По первому нуклеотиду кодона РНК определяем в таблице горизонтальный ряд, а по второму – вертикальный столбец. На их пересечении находим нужную тройку нуклеотидов и читаем название соответствующей ей аминокислоты.
3. Чтобы написать последовательность нуклеотидов второй цепочки молекулы ДНК, когда известна последовательность их в первой цепочке, достаточно, пользуясь правилом Чаргаффа, заменить тимин на аденин, аденин на тимин, гуанин на цитозин и цитозин на гуанин.
4. Чтобы закодировать тройками нуклеотидов последовательность аминокислот белка, обращаемся к биохимическому коду наследственности (см. табл. комплементарности на стр. 43). Для каждой аминокислоты находим ее кодовое «обозначение» в виде соответствующей тройки нуклеотидов и выписываем его. Располагаем эти тройки друг за другом в таком же порядке, в каком идут изображаемые нами аминокислоты, получаем формулу строения искомого участка молекулы информационной РНК. Поскольку в генетическом коде имеются «синонимы[1]» для каждой аминокислоты найдется не одна, а несколько изображающих ее нуклеотидных троек. Выбор между ними делается по произволу решающего задачу. Таким образом, данная задача допускает множество правильных решений.
5. Обратная задача, воспроизвести последовательность аминокислот в белке или его фрагменте решается аналогично. От 5’ конца отсчитываем тройки нуклеотидов и пользуясь таблицей комплементарности выписываем соответствующую аминокислоту.
Учебное издание
Биологическая химия
Учебно-методический комплекс по дисциплине
Специальность 032400.00 – Биология,
со специализацией 032418 – Фитодизайн
заочное отделение
Составитель :
Подписано в печать. Формат 60×84/16.
Бумага писчая. Печать оперативная.
Усл. печ. л. 2,44. Тираж 25 экз. Заказ №.
ГОУ ВПО «Чувашский государственный педагогический
университет им. »
Чебоксары, ул. К. Маркса, 38
Отпечатано на участке оперативной полиграфии
ГОУ ВПО «Чувашский государственный педагогический
университет им. »
Чебоксары, ул. К. Маркса, 38
 |
[1] В языкознании синонимами называются различно звучащие слова с одинаковым смыслом, например: гиппопотам и бегемот.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |