На правах рукописи
СОБОЛЕВА
Елена Леонидовна
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА И
ПАТОГЕНЕТИЧЕСКАЯ ТЕРАПИЯ
ВРОЖДЕННОЙ ГИПЕРПЛАЗИИ КОРЫ НАДПОЧЕЧНИКОВ
И СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
14.01.01 – акушерство и гинекология
14.01.02 – эндокринология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора медицинских наук
Санкт-Петербург – 2011
Работа выполнена в Учреждении Российской академии медицинских наук
Научно-исследовательском институте акушерства и гинекологии им. Северо-Западного отделения РАМН
Научные консультанты:
академик РАМН, заслуженный деятель науки РФ,
доктор медицинских наук, профессор
заслуженный деятель науки РФ,
доктор медицинских наук, профессор
Официальные оппоненты:
заслуженный деятель науки РФ,
доктор медицинских наук, профессор
доктор медицинских наук, профессор
доктор медицинских наук, профессор
Ведущая организация: Московский областной научно-исследовательский институт акушерства и гинекологии
Защита состоится « ____» _______________ 2011 г. в ______часов на заседании диссертационного совета Д 001.021.01 при Научно-исследовательском институте акушерства и гинекологии им. СЗО РАМН ( Санкт-Петербург, Менделеевская линия, д. 3).
С диссертацией можно ознакомиться в библиотеке Научно-исследовательского
института акушерства и гинекологии им. СЗО РАМН.
Автореферат разослан «_____» _______________2011 г.
Ученый секретарь
диссертационного совета
доктор медицинских наук
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Проблема диагностики и лечения заболеваний, сопровождающихся гиперандрогенемией, в настоящее время является одной из самых актуальных в гинекологической эндокринологии. Это связано с тем, что гиперандрогенемия может оказывать влияние на все стороны жизни женщины – начиная от внешности и заканчивая состоянием репродуктивной функции. Наиболее частыми причинами гиперандрогенемии у женщин являются синдром поликистозных яичников (СПЯ) и неклассическая форма врожденной гиперплазии коры надпочечников (НФ ВГКН), а также нарушение синтеза фермента 5α-редуктазы и повышение чувствительности к андрогенам в тканях-мишенях, приводящее к развитию "идиопатического" гирсутизма (Blume-Peytavi U., Hahn S., 2008, Brodell L. A., Mercurio M. G., 2010, Castelo-Branco C., Cancelo M. J., 2010). Распространенность СПЯ среди женщин репродуктивного возраста составляет 5-10% ( и соавт., 2010, Azziz R. et al., 2004, Ehrmann D. A., 2005), при этом частота встречаемости в структуре бесплодия – 8,5 – 12%, а среди женщин с эндокринным бесплодием частота возрастает до 30 – 40% (, 1991, Franks S., 1989). Частота НФ ВГКН широко варьирует в различных этнических группах и составляет среди европейцев 1:1000, а в гетерогенной популяции Нью-Йорка – 1:100 человек (Speiser P.W. et al., 1985, New M. I., 2006). У женщин с НФ ВГКН может быть нарушение функции яичников в виде ановуляции, приводящей к бесплодию (, 1995, London D., 1987, New M. I., 2006). Частота невынашивания беременности при НФ ВГКН может достигать 25% (Bidet M. et al., 2010, Feldman S. et al., 1992, Moran С. et al., 2006).
До настоящего времени вопросы диагностики и лечения андрогензависимых состояний у женщин остаются до конца не изученными. Ввиду общности клиничес-кой симптоматики СПЯ и НФ ВГКН затруднена дифференциальная диагностика. При гормональном обследовании повышенный уровень дегидроэпиандростерона-сульфата (ДЭА-С), андрогена, преимущественно синтезируемого в надпочечниках, наблюдается у 20-30% больных СПЯ (Young M. et al., 1989). "Золотым стандартом" для диагностики НФ ВГКН считается проба с адренокортикотропным гормоном (АКТГ) (New M. I., 2006). При уровне стимулированного 17-гидроксипрогестерона (17-ОНП) более 30 нмоль/л диагностируется НФ ВГКН ( и соавт., 2010, Azziz R. et al., 1999, Huerta R. et al., 2000, Kelestimur F., 2006). В нашей стране применяется препарат АКТГ пролонгированного действия – синактен-депо. Однако в настоящее время нет единой точки зрения о методике проведения и критериях оценки данной пробы. Кроме того, продолжается обсуждение вопроса о показаниях к проведению пробы с АКТГ. Часть авторов считает, что проведение пробы с АКТГ целесообразно только в том случае, если базальный уровень 17-ОНП в крови превышает 6 нмоль/л (, , 2007, Azziz R. et al., 1994, Dewailly D., 2002). Другие авторы полагают, что пробу с АКТГ следует проводить независимо от базального уровня 17-ОНП (Rumsby G. et al., 1988). В настоящее время все большее распространение получает молекулярно-генетический метод обследования больных с подозрением на НФ ВГКН. Хорошо известно, что наличие носительства мутаций в гене 21-гидроксилазы (21-Г) в гомозиготном или компаундном гетерозиготном носительстве трактуется как наличие у больной ВГКН (New M. I., 2006). При этом остается открытым вопрос о том, вызывает ли гетерозиготное носительство мутаций в гене 21-Г развитие НФ ВГКН (, 1995, Azziz R., Owerbach D., 1995, Moran C., 2006 , New M. I., 2006). Кроме того, изучение спектра мутаций в гене 21-Г может помочь не только в плане диагностики НФ ВГКН, но и в профилактике рождения детей с классической формой ВГКН (Azziz R. et al., 1994, Moran C., 2006, New M. I., 1998). Риск рождения ребенка с классической формой ВГКН от матерей с НФ ВГКН составляет 2,5%, а ребенка с НФ ВГКН – 15% (Moran C. et al. 2006). В настоящее время применение глюкокортикостероидов рекомендовано больным НФ ВГКН на этапе планирования беременности (Castelo-Branco C., Cancelo M. J., 2009, Feldman S. et al., 1992, New M. I., 2006). Однако в России достаточно часто назначение глюкокортикостероидов происходит уже после наступления беременности, на основании определения уровня 17-ОНП и ДЭА-С в крови. При этом в работе в 2007 году было убедительно доказано, что при беременности верификация диагноза НФ ВГКН возможна только путем молекулярно-генетического исследования, а определение уровня адреналовых андрогенов в крови не является информативным. Для лечения симптомов андрогензависимой дермопатии широко применяются комбинированные оральные контрацептивы (КОК), в состав которых входят гестагены с антиандрогенной активностью, но остается не ясным вопрос о продолжительности и безопасности применения антиандрогенов (Castelo-Branco C., Cancelo M. J., 2009, Dewailly D., 2000). Данные о применении агонистов гонадотропин-рилизинг гормона (аГн-РГ) для лечения СПЯ и гирсутизма носят противоречивый характер. На фоне применения аГн-РГ у больных отмечалось подавление гонадотропной функции гипофиза, уменьшение объема яичников, уменьшение гирсутизма (, 2002, De Leo V. et al., 2000]. В то же время Szilagyi A. et al., 2000, не обнаружили уменьшения гирсутизма на фоне применения аГн-РГ. Некоторые авторы [Castelo-Branco C., Cancelo M. J., 2009) указывают на более низкую эффективность терапии гирсутизма при применении аГн-РГ в сочетании с КОК по сравнению с сочетанием КОК и ципротерона ацетата. Дискутируется вопрос о целесообразности предварительной подготовки больных СПЯ антиандрогенами и/или аГн-РГ перед индукцией овуляции ( и соавт., 2010, Carmina E., Lobo R. A., 1997). Кроме того, до настоящего времени не решен вопрос о целесообразности и продолжительности применения глюкокортикостероидов у больных НФ ВГКН, предъявляющих жалобы на гирсутизм. По данным Spritzer P. et al., 1998, глюкокортикостероиды не уменьшают выраженность гирсутизма, в то время как на фоне ципротерона ацетата наблюдается редукция гирсутизма. В представленных в последние годы обзорах литературы (Brodell L. A., Mercurio M. G., 2010, Castelo-Branco C., Cancelo M. J., 2009, Lumachi F., Basso S. M.M., 2010), обобщающих данные мировых исследований по лечению гирсутизма, глюкокортикостероиды даже не рассматриваются как метод лечения гирсутизма. В то же время отечественные авторы (, , 2005, , 2009) рекомендуют применение глюкокортикостероидов для лечения гирсутизма, причем и во время беременности. Все вышеизложенное определяет актуальность проблемы, связанной с диагностикой и лечением гиперандрогенемии у женщин.
Цель исследования заключалась в разработке критериев диагностики и оптимизации патогенетических методов терапии врожденной гиперплазии коры надпочечников и синдрома поликистозных яичников.
Задачи исследования
1. Выяснить диагностическую ценность клинических, гормональных и
эхографических показателей для СПЯ и НФ ВГКН.
2. Установить диагностические критерии функциональной пробы с
синтетическим аналогом АКТГ пролонгированного действия для
диагностики НФ ВГКН.
3. Оценить частоту и характер метаболических нарушений у больных СПЯ.
4. Выяснить диагностическую ценность выявления мутаций в гене 21-гидроксилазы для верификации НФ ВГКН.
5. Изучить эффективность применения глюкокортикостероидных препаратов у больных НФ ВГКН для лечения андрогензависимой дермопатии и нарушения репродуктивной функции.
6. Определить показания к применению метформина у больных СПЯ.
7. Оценить эффективность применения комбинированных оральных
контрацептивов, а также их сочетания с антиандрогенами и агонистами
гонадотропин-рилизинг гормона для лечения больных СПЯ.
8. Выяснить клиническую эффективность медикаментозной терапии андрогензависимой дермопатии.
Научная новизна и теоретическая значимость работы
Показано, что подъем уровня 17-ОНП в крови выше 26 нмоль/л в ответ на стимуляцию пролонгированным препаратом АКТГ указывает на наличие НФ ВГКН с высокой точностью предсказания (91,2%). Впервые проведен анализ гетерозиготного носительства мутаций в гене 21-гидроксилазы у больных с андрогензависимой дермопатией независимо от генеза заболевания. Выявлена высокая частота нарушения репродуктивной функции у гетерозиготных носителей мутаций в гене 21-гидроксилазы независимо от результатов пробы с АКТГ. Обнаружено, что при нормальной пробе с АКТГ могут быть выявлены мутации в гене 21-Г в виде компаундного гетерозиготного носительства, указывающие на наличие НФ ВГКН.
Показано, что при СПЯ нормогонадотропная недостаточность яичников в виде хронической ановуляции встречается у подавляющего числа больных. При этом установлено, что при СПЯ значительно чаще наблюдается повышение секреции гонадотропинов гипофизом, сопровождающееся нарушением функции яичников в виде хронической ановуляции, чем у больных НФ ВГКН. В то же время содержание базального и стимулированного 17-ОНП в крови больных СПЯ не отличается от показателей у здоровых женщин и значительно ниже, чем у больных НФ ВГКН, что свидетельствует об отсутствии дефекта синтеза надпочечниковых андрогенов. Установлено, что нарушение толерантности к глюкозе выявляется у трети больных СПЯ и встречается с одинаковой частотой при нормальной и избыточной массе тела. При этом более выраженная гиперинсулинемия наблюдается при наличии избытка массы тела. Показано, что развитие гирсутизма связано не только с гиперандрогенемией, но и с рецепцией андрогенов в тканях, на что указывает отсутствие корреляции между уровнем андрогенов в крови и гирсутным числом, независимо от этиологии гиперандрогенемии.
Продемонстрировано, что применение патогенетической терапии глюкокортикостероидами у больных НФ ВГКН на этапе восстановления репродуктивной функции приводит к снижению частоты невынашивания беременности. Установлено, что применение антиандрогенов в составе комбинированных оральных контрацептивов у больных СПЯ является патогенетическим методом лечения, приводящим к нормализации секреции гонадотропинов гипофизом, андрогенов яичниками и к нормализации объема яичников. Разработаны медикаментозные принципы лечения андрогензависимой дермопатии.
Практическая значимость работы
Разработан алгоритм дифференциальной диагностики гиперандрогенемии различного происхождения, включающий в себя данные гормонального, ультразвукового, молекулярно-генетического исследования и функциональной пробы с препаратом АКТГ пролонгированного действия. Доказана необходимость проведения пробы на толерантность к глюкозе всем больным СПЯ с определением уровня инсулина натощак для своевременного выявления гиперинсулинемии и/или нарушения углеводного обмена и назначения патогенетической терапии. Показана целесообразность проведения предварительной медикаментозной подготовки больных СПЯ перед индукцией овуляции. Обнаружена высокая эффективность применения терапии глюкокортикостероидами у больных НФ ВГКН для восстановления репродуктивной функции. Установлено, что применение глюкокортикостероидов не приводит к уменьшению степени выраженности гирсутизма у больных НФ ВГКН. Продемонстрирована высокая эффективность применения комбинированных оральных контрацептивов, содержащих гестаген с антиандрогенным действием (ципротерона ацетат, дроспиренон) при лечении симптомов андрогензависимой дермопатии (вульгарных угрей, гирсутизма). Установлено, что ципротерона ацетат имеет дозозависимый эффект, в связи с чем при гирсутизме средней и тяжелой степени целесообразно применение комбинированных оральных контрацептивов в сочетании с ципротерона ацетатом.
Основные положения, выносимые на защиту
1. Повышенное содержание общего и свободного тестостерона, андростендиона и низкий уровень глобулина, связывающего половые стероиды, в крови больных СПЯ обусловлено гиперсекрецией лютеинизирующего гормона гипофизом и гиперинсулинемией. При этом реакция 17-гидроксипрогестерона на экзогенный АКТГ не нарушена.
2. Диагностическими признаками НФ ВГКН являются мутации в гене 21-гидроксилазы (мутация сплайсинга во 2 интроне, делеция гена в 3 экзоне; точковые мутации: I172N в 4 экзоне, V237E в 6 экзоне, V281L в 7 экзоне, Q318X в 8 экзоне; "химерные" гены 1-го и 2-го типа в гомозиготном, гетерозиготном и компаундном носительстве) и/или повышение базального и стимулированного АКТГ уровня 17-гидроксипрогестерона в крови. Повышение уровня 17-гидроксипрогестерона в крови в ответ на экзогенный АКТГ более 26 нмоль/л указывает на наличие НФ ВГКН с точностью предсказания 91,2%.
3. Терапия глюкокортикостероидами является высокоэффективным методом лечения нарушения репродуктивной функции у больных НФ ВГКН, приводящим к восстановлению фертильности у большинства больных и значительному снижению частоты невынашивания беременности.
4. Комбинированные оральные контрацептивы, в состав которых входят рецепторные антагонисты андрогенов (ципротерона ацетат, дроспиренон), вызывают у больных СПЯ через 3 месяца лечения нормализацию секреции ЛГ гипофизом, размеров яичников и продукцию ими андрогенов.
5. Ципротерона ацетат оказывает дозозависимый эффект на снижение
гирсутного числа у больных как с овариальной, так и с надпочечниковой
гиперандрогенемией.
Апробация работы и внедрение результатов в практику. Материалы диссертации представлены на III Всероссийском съезде эндокринологов (Москва, 1996), на научно-практической конференции молодых ученых и врачей (Москва, 1996), на II съезде Российской ассоциации врачей акушеров-гинекологов (Москва, 1997), на Балтийской конференции акушеров-гинекологов (Санкт-Петербург, 1999), на юбилейной Российской конференции, посвященной 100-летию со дня рождения академика АМН СССР (Санкт-Петербург, 2000), на IV Всероссийском конгрессе эндокринологов “Актуальные проблемы современной эндокринологии” (Санкт-Петербург, 2001), на конференции “Контрацепция и гиперандрогенемия” (Архангельск, 2002), на отчетной конференции акушеров-гинекологов в г. Мурманске и Новгороде в 2002 году, на конференции “Новые горизонты гинекологической эндокринологии” (Москва, 2002), на Всероссийской научно-практической конференции «Клиническая эндокринология – достижения и перспективы», посвященной 80-летию со дня рождения Заслуженного деятеля науки РСФСР, профессора (Санкт-Петербург, 2003), на отчетной конференции акушеров-гинекологов Петрозаводска в 2003 году, на Европейской конференции “European human genetic conference” (Прага, 2005), на конференции “Гиперандрогенемия у женщин” для акушеров-гинекологов и эндокринологов (Псков, 2006), на V Всероссийском конгрессе эндокринологов “Высокие медицинские технологии в эндокринологии” (Москва, 2006), на Международном конгрессе ”Практическая гинекология: от новых возможностей к новой стратегии” (Москва 2006), на конференции “Метаболический синдром у женщин” (Санкт-Петербург, 2006), на конференции “Современная контрацепция” (Сыктывкар, 2007) и на отчетной конференции эндокринологов (Сыктывкар, 2009), на конференции “Эндокринное бесплодие у женщин” (Тюмень, 2010), на конференции “Гиперандрогенемия у женщин” (Калининград, 2010), на V Международном конгрессе по репродуктивной медицине (Москва, 2011); на ежегодных семинарах в НИИ АГ им. СЗО РАМН "Актуальные вопросы гинекологической эндокринологии", проводимых для врачей России, стран СНГ и ближнего зарубежья. Результаты работы также были доложены на научно-практических семинарах для акушеров-гинекологов и эндокринологов Санкт-Петербурга и Ленинградской области (), на заседании акушеров-гинекологов Ленинградской области (2006), на обществе эндокринологов Санкт-Петербурга (2009), на обществе акушеров-гинекологов Санкт-Петербурга (1998, 2007, 2011).
Основные результаты исследования используются в работе отделения гинекологической эндокринологии, научно-поликлинического отделения и лаборатории пренатальной диагностики врожденных и наследственных болезней НИИ АГ им. СЗО РАМН. Результаты исследования внедрены в работу женских консультаций № 9 и № 20, используются в учебно-педагогической работе кафедры акушерства, гинекологии и репродуктологии СПб Государственного Университета и кафедры акушерства и гинекологии СПб Государственного медицинского университета им. акад. .
По теме диссертации опубликовано 35 печатных работ, в том числе 15 – в ведущих рецензируемых научных журналах и изданиях, определенных ВАК РФ, одно учебное пособие для врачей.
Структура и объем диссертации. Диссертация состоит из введения, обзора литературы, главы о материалах и методах, 4 глав собственных исследований, обсуждения, выводов, практических рекомендаций, списка использованной литературы, включающего 82 отечественных и 225 зарубежных источников. Материалы диссертации изложены на 282 страницах машинописного текста, иллюстрированы 87 таблицами и 41 рисунком.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования
Исследование выполнено в отделении гинекологической эндокринологии, в научно-поликлиническом отделении и в лабораториях эндокринологии и пренатальной диагностики врожденных и наследственных болезней НИИ АГ им. СЗО РАМН. Для решения поставленных задач в период с 1995 по 2010 гг. было обследовано 595 женщин: 35 женщин вошли в контрольную группу и 560 больных составили основную группу. Для проведения исследования и решения поставленных задач были сформированы несколько групп больных. Первую группу составили 145 больных НФ ВГКН. Возраст больных колебался от 18 до 37 лет и в среднем составил 24,3±0,4 года. Нарушение менструального цикла было у,8%) больной. Симптомы андрогензависимой дермопатии были у ,7%) больных. Во вторую группу вошли 197 больных СПЯ. Возраст больных колебался от 18 до 37 лет и в среднем составил 23,9±0,4 года. Нарушение менструального цикла было у %) больной. Симптомы андрогензависимой дермопатии выявлены у ,7%) женщин. В третью группу были включены 218 больных с симптомами андрогензависимой дермопатии неясного генеза. Возраст женщин колебался от 18 до 40 лет и в среднем составил 24,2±0,4 года. Ввиду выраженной неоднородности данной группы было проведено разделение больных на 2 подгруппы в зависимости от уровня прогестерона в крови на 21–23-й день менструального цикла. В первую подгруппу (подгруппа 3а) вошли 105 женщин с уровнем прогестерона в крови ниже 28 нмоль/л – больные с нормогонадотропной недостаточностью яичников. Вторую подгруппу (подгруппа 3б) составили 74 женщины с регулярным овуляторным менструальным циклом (уровень прогестерона в крови выше или равен 28 нмоль/л, при ультразвуковом исследовании яичников (УЗИ) – наличие желтого тела в яичнике) – больные с «идиопатической» андрогенизацией. Контрольную группу составили 35 здоровых женщин репродуктивного возраста (средний возраст 25,5±0,3 года) с регулярным овуляторным менструальным циклом без симптомов андрогензависимой дермопатии. Популяционную выборку составили 47 здоровых доноров из Северо-Западного региона России.
Всем больным проводилось клиническое и лабораторное обследование, включающее в себя оценку менструального цикла и репродуктивной функции, весо-ростовых показателей, степени тяжести гирсутизма и вульгарных угрей, а также биохимическое, гормональное, ультразвуковое и молекулярно-генетическое исследования. Всем больным проводилось лабораторное обследование, которое включало в себя биохимические исследования (липидный профиль, коагулограмма, определение уровней печеночных трансаминаз в крови), проведение пробы на толерантность к глюкозе (ПТГ) и определение содержания гормонов в крови. Определение уровня гормонов в крови проводилось в лаборатории эндокринологии НИИ АГ им. СЗО РАМН (руководитель отдела эндокринологии – з. д.н. РФ, д. м.н., профессор ). Уровень фолликулостимулирующего гормона (ФСГ), лютеинизирующего гормона (ЛГ), пролактина, прогестерона, тестостерона, глобулина, связывающего половые стероиды (ГСПС), ДЭА-С в крови определяли иммуноферментным методом с использованием наборов фирмы ²Алкор-Био² (Россия). Уровень андростендиона, свободного тестостерона, дигидротестостерона, 17-ОНП, инсулина определяли иммуноферментным методом с использованием наборов фирмы "DRG-Diagnostics" (Германия). Пробу с синтетическим аналогом АКТГ продленного действия – тетракозактидом (синактен-депо) проводили на 5–8-й день менструального цикла в модификации, разработанной в Научном центре акушерства, гинекологии и перинатологии РАМН [, 1995]. Ультразвуковое исследование органов малого таза проводили на аппарате Medison SA-8000. Генетическое исследование проводилось в лаборатории пренатальной диагностики врожденных и наследственных болезней НИИ АГ им. СЗО РАМН (руководитель лаборатории – член.-корр. РАМН, з. д.н. РФ, д. м.н., профессор ). Методом полимеразной цепной реакции с использованием анализа полиморфизма длины рестрикционных фрагментов исследованы спектр и частоты мутаций в гене 21-Г у 107 больных, а также у 47 здоровых доноров Северо-Западного региона России.
Статистическую обработку полученных результатов проводили с использованием методов параметрической и непараметрической статистики. Для оценки межгрупповых различий значений признаков, имеющих непрерывное распределение, применяли t-критерий Стьюдента, ранговый U-критерий Манна-Уитни, а при сравнении частотных величин - c2-критерий Пирсона и точный метод Фишера (ТМФ). При сравнении парных (сопряженных) выборок использовали парный td-кpитеpий (Стьюдента), парный Ud-критерий (Вилкоксона) и парный критерий МакНемара. Для решения дифференциально-диагностических задач применяли линейный дискриминантный анализ. Статистическая обработка материала выполнялась на персональном компьютере с использованием стандартного пакета программ прикладного статистического анализа (Statistica for Windows v. 6.0). Критический уровень достоверности нулевой статистической гипотезы (об отсутствии значимых различий или факторных влияний) принимали равным 0,05.
Результаты исследования
Характеристика больных НФ ВГКН
В исследуемую группу вошли 145 больных. Средний возраст наступления менархе составил 13,2±0,1 года и не отличался от показателя в контрольной группе (13,0±0,1; р>0,1). По нашим данным, недостаточность функции яичников встречалась у 77,2% больных, в виде хронической ановуляции – у 89,3% из них. Нарушение менструального цикла (НМЦ), чаще всего по типу опсоменореи, отмечено у 63% больных. Частота бесплодия при НФ ВГКН составила 24% (у 35 из 145 больных). Невынашиванием закончились 50,9% беременностей, у 17% больных было привычное невынашивание. Симптомы андрогензависимой дермопатии наблюдались у ,7%) больных и у большинства появлялись одновременно с нарушением менструального цикла, что подтверждает роль гиперандрогенемии в нарушении функции яичников. Однако у%) женщин возраст появления гирсутизма опережал возраст менархе, что может указывать на наличие гиперандрогенемии в допубертатный период вследствие врожденного ферментного дефекта синтеза андрогенов надпочечниками. Гирсутизм обнаружен у,9%) больных, вульгарные угри – у,7%). Избыток массы тела встречался относительно редко – у%) больной. У,7%) больных были указания на быстрый рост до пубертатного возраста, после чего произошло резкое его прекращение; преждевременное прекращение роста (в 12-14 лет) наблюдалось у%) больных и низкий рост по сравнению с родителями имели,9%) больных. Нарушение нормальных темпов роста может быть связано с гиперпродукцией адреналовых андрогенов в пре - и пубертатном возрасте, которая приводит к преждевременному закрытию "зон роста". При оценке гормональных показателей было обнаружено (табл. 1), что у больных НФ ВГКН имеется значительное повышение в крови уровней ДЭА-С, 17-ОНП, свободного тестостерона, андростендиона и дигидротестостерона, снижение ГСПС, приводящее к повышению расчетного индекса свободного андрогена (ИСА) по сравнению с аналогичными показателями в контрольной группе.
Таблица 1
Содержание андрогенов в крови больных НФ ВГКН и у здоровых женщин
Гормоны | НФ ВГКН M±m | Контроль M±m | р |
Тестостерон (нмоль/л) | 2,9±0,2 n=81 | 1,4±0,1 n=30 | <0,001 |
ГСПС (нмоль/л) | 49,9±4,7 n=35 | 68,8±3,9 n=30 | =0,001 |
ИСА (%) | 8,6±1,2 n=35 | 2,3±0,3 n=30 | <0,001 |
Свободный тестостерон (пмоль/л) | 77,5±24,3 n=71 | 4,02±0,63 n=23 | <0,001 |
Андростендион (нмоль/л) | 10,8±1,0 n=59 | 7,0±0,8 n=30 | =0,006 |
ДЭА-С (мкмоль/л) | 10,6±0,6 n=96 | 4,4±0,4 n=23 | <0,001 |
Дигидротестостерон (нмоль/л) | 2,6±0,3 n=61 | 0,77±0,05 n=21 | <0,001 |
17-ОНП (нмоль/л) | 8,2±0,9 n=137 | 3,4±0,3 n=13 | <0,001 |
Примечание: при сравнении групп использовался критерий Манна-Уитни (U)
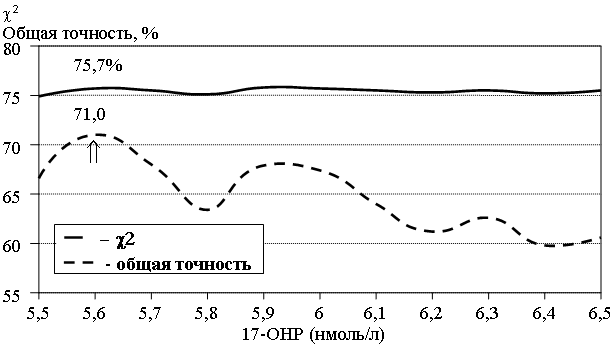
Известно, что содержание ДЭА-С в крови линейно снижается с возрастом, начиная с 20 лет. Однако в группе больных НФ ВГКН отсутствовала отрицательная корреляция между возрастом и уровнем ДЭА-С в крови, что указывает на постоянную монотонную гиперсекрецию ДЭА-С надпочечниками, не изменящуюся с возрастом. Не было обнаружено достоверной корреляции между гирсутным числом и уровнем андрогенов в крови. Полученные данные указывают на то, что степень выраженности гирсутизма зависит не только от уровня андрогенов в крови, но и от многих других факторов (активность фермента 5α-редуктазы, чувствительность тканевых рецепторов андрогенов, наследственная предрасположенность и др.). Базальный уровень 17-ОНП в крови выше 15 нмоль/л был выявлен у 14 (9,7%) больных, что является диагностическим критерием наличия НФ ВГКН. В настоящее время нет единой точки зрения о критериях оценки пробы с АКТГ пролонгированного действия (синактен-депо), в связи с чем мы сочли необходимым попытаться установить диагностический уровень базального и стимулированного 17-ОНП в крови. Для этого был применен метод последовательного приближения к точкам максимума двух целевых функций – c2-критерия и общей точности прогноза. Сравнение проводилось между больными НФ ВГКН и суммарной группой, в которую были включены больные СПЯ и женщины с симптомами андрогензависимой дермопатии неясного происхождения. В результате проведенного анализа (рис. 1) был установлен абсолютный максимум базального уровня 17-ОНП в крови – 5,6 нмоль/л (c2=71,0; р<0,001).


|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



