ТСО: Мм – мультимедийные средства, ПК – персональный компьютер, Пл – плакаты, Тб – таблицы, Лу – лабораторная установка, Сл – слайды, Вф – видеофильмы, ТК – входной тестовый контроль, РК – рубежный контроль или контрольная работа, ИК – итоговый тестовый контроль (Интернет – экзамен) или экзамен в традиционной форме.
Приложение 1
Структура, состав и варианты расчетно-графической работы для специальности 080102.65 – мировая экономика,
080105.65 – финансы и кредит.
ВАРИАНТ 1
Раскройте тему (оформите в виде реферата)
Хаос и современность. Хаос и социальные катаклизмы.
Решите задачи:
1. Вычислите, при какой температуре реакция закончится за 45 минут, если при 293 К на это требуется 3 часа. Температурный коэффициент равен 3,2.
2. Дайте термодинамическую характеристику процесса
Fe2O3(т) + H2(г) → Fe(т) + H2O(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте алюминий по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Результаты измерения (мг) 398, 396, 398, 392, 393, 401 при эталонном значении 400 мг. Рассчитайте абсолютное и относительное отклонение и погрешности измерения. Все ли значения входят в доверительный интервал с вероятностью 0,95 ?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – время (τ), единица измерения – секунда (с); формула для расчета 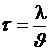 ; исходные данные: расстояние 3050 футов (1 фут=0,3048 м), скорость движения 50 км/час.
; исходные данные: расстояние 3050 футов (1 фут=0,3048 м), скорость движения 50 км/час.
ВАРИАНТ 2
Раскройте тему (оформите в виде реферата)
Будущее человека и процесс генетики.
Решите задачи:
1. Для практической остановки реакции применяют быстрое охлаждение реакционной смеси. Определите, во сколько раз изменится скорость реакции при охлаждении реакционной смеси с 40 0С до -10 0С, если температурный коэффициент реакции равен 2,7.
2. Дайте термодинамическую характеристику процесса
С2Н2(г) + О2(г) → СО2(г) + Н2О(ж)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте железо по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Результаты измерения 25, 29, 23, 29, 26. Рассчитайте стандартное отклонение. Определите доверительный интервал для вероятности 0,95.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – масса (m), единица измерения – килограмм (кг); формула для расчета 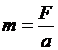 ; исходные данные: сила 60 Н (Н=кг·м·с-2), ускорение 80 см/с2.
; исходные данные: сила 60 Н (Н=кг·м·с-2), ускорение 80 см/с2.
ВАРИАНТ 3
Раскройте тему (оформите в виде реферата)
НТР и проблемы экологии.
Решите задачи:
1. Две реакции при 283 К протекают с одинаковой скоростью. Температурный коэффициент скорости первой и второй реакции равны соответственно 2,5 и 3,0. Как будут относиться скорости реакций, если первую из них провести при 350 К, а вторую при 330 К?
2. Дайте термодинамическую характеристику процесса
TiO2(т) + C(графит) → Ti(т) + CO(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте хлор по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Найдите случайную ошибку анализа при Р = 0,95 и доверительные границы для определяемой величины, если результаты её измерения: 3,25; 3,15; 3,08; 3,20; 3,20.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – давление (Р), единица измерения – Паскаль (Па); формула для расчета 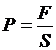 ; исходные данные: сила 100 Н (1 Н=1 кг·м·с-2), площадь 15,5.
; исходные данные: сила 100 Н (1 Н=1 кг·м·с-2), площадь 15,5.
1 Па = 1 Н· м-2
ВАРИАНТ 4
Раскройте тему (оформите в виде реферата)
Гипотезы профессора о новых свойствах времени.
Решите задачи:
1. На сколько нужно повысить температуру, чтобы скорость реакции возросла в 90 раз? Температурный коэффициент равен 2,7.
2. Дайте термодинамическую характеристику процесса
PCl5(г) → PCl3(г) + Cl2(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте хром по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Сколько параллельных измерений необходимо выполнить, если границы доверительного интервала ± 0,10; стандартное отклонение S = 2,5, а доверительная вероятность —95%?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – масса (m), единица измерения – килограмм (кг); формула для расчета 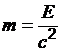 ; исходные данные: энергия 1,8· 1014 Дж, с = 2,998 · 1010 см/с.
; исходные данные: энергия 1,8· 1014 Дж, с = 2,998 · 1010 см/с.
1 Дж = 1 кг· м2 · с-2
ВАРИАНТ 5
Раскройте тему (оформите в виде реферата)
Циклы и длинные волны в экономике и социологии.
Решите задачи:
1. Реакция протекает по уравнению 2А = В. Исходная концентрация вещества А равна 0,2 моль/м3. Константа равновесия реакции 0,5. Вычислите равновесные концентрации веществ.
2. Дайте термодинамическую характеристику процесса
HCl(г) + O2(г) → H2O(г) + Cl2(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте свинец по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Покажите, является ли «промахом» измеренная величина 50,5 среди результатов 48,0; 49,1; 48,7; 49,95; 50,1; 50,3.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – длина волны (λ), единица измерения – нанометр (нм); формула для расчета 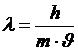 ; исходные данные: масса частицы 1,67· 10-24 г, скорость = 2,998 · 1010 см/с постоянная Планка h = 6,62 · 10-34 Дж · с.
; исходные данные: масса частицы 1,67· 10-24 г, скорость = 2,998 · 1010 см/с постоянная Планка h = 6,62 · 10-34 Дж · с.
1 Дж = 1 кг· м2 · с-2
ВАРИАНТ 6
Раскройте тему (оформите в виде реферата)
Строение клетки живого организма. Роль ее элементов.
Решите задачи:
1. Скорость химической реакции при 20 0С равна 1 моль/(л·с). Вычислите скорость этой реакции при 60 0С, если температурный коэффициент равен 3.
2. Дайте термодинамическую характеристику процесса
CaO(т) + H2O(ж) → Ca(OH)2(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте висмут по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Установите, имеется ли систематическая ошибка в результатах измерений: 121,5; 102,5; 120,0; 122,0 при заданном значении 124,0.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – энергия (Е), единица измерения – джоуль (Дж); формула для расчета 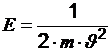 ; исходные данные: масса 360 тонн, скорость 40 км/час.
; исходные данные: масса 360 тонн, скорость 40 км/час.
1 Дж = 1 кг· м2 · с-2
ВАРИАНТ 7
Раскройте тему (оформите в виде реферата)
Устройство памяти. Воспроизводство и передача информации в организме.
Решите задачи:
1. На сколько градусов надо повысить температуру газообразной реакционной смеси, чтобы скорость реакции увеличилась в 125 раз, если температурный коэффициент равен 5?
2. Дайте термодинамическую характеристику процесса
C2H5OH(ж) + O2(г) → CO2(г) + H2O(ж)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте кадмий по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Рассчитайте абсолютное и относительное значение стандартного отклонения результатов измерений: 11,11; 11,12; 11,15; 11,10; 11,11; 11,13. Определите, есть ли «промахи» в результатах измерений?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – ускорение (а), единица измерения – м/с2; формула для расчета 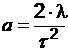 ; исходные данные: длина 3 · 102 см, время движения 0,04 с.
; исходные данные: длина 3 · 102 см, время движения 0,04 с.
ВАРИАНТ 8
Раскройте тему (оформите в виде реферата)
Экологические проблемы Дальнего Востока.
Решите задачи:
1. При охлаждении реакционной смеси с 50 до 20 0С скорость химической реакции уменьшилась в 27 раз. Вычислите температурный коэффициент этой реакции.
2. Дайте термодинамическую характеристику процесса
NH3(г) + O2(г) → N2(г) + H2O(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте магний по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Сколько параллельных измерений необходимо выполнить для сужения доверительного интервала до ± 0,15, если эмпирическое стандартное отклонение равно 2,50, а вероятность — 95%?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – теплоемкость (С), единица измерения – Дж/К; формула для расчета  ; исходные данные: количество теплоты 1,5 кДж, изменение температуры на 50.
; исходные данные: количество теплоты 1,5 кДж, изменение температуры на 50.
ВАРИАНТ 9
Раскройте тему (оформите в виде реферата)
Человек, биосфера и космические циклы.
Решите задачи:
1. Скорость химической реакции при 50 0С равна 5 моль/(л·с). Вычислите скорость этой реакции при 100 0С, если температурный коэффициент равен 2.
2. Дайте термодинамическую характеристику процесса
NH3(г) + O2(г) → NO(г) + H2O(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте фосфор по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Результаты измерения 8,25; 8,15; 8,08; 8,20; 8,02. Найти случайную ошибку анализа при Р = 0,95 и границы доверительного интервала.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – молярная теплоемкость (См), единица измерения – Дж/моль·К; формула для расчета 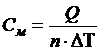 ; исходные данные: количество теплоты 2,09 кДж, количество вещества 5 моль, нагрев на 100 градусов.
; исходные данные: количество теплоты 2,09 кДж, количество вещества 5 моль, нагрев на 100 градусов.
ВАРИАНТ 10
Раскройте тему (оформите в виде реферата)
Роль и действие ДНК и РНК в организме. Передача наследственной информации.
Решите задачи:
1. Реакция при температуре 50 0С протекает за 200 с. Температурный коэффициент данной реакции равен 2. За сколько времени закончится эта реакция при 70 0С?
2. Дайте термодинамическую характеристику процесса
N2(г) + H2(г) → NH3(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте кремний по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Получены результаты измерения: 0,525; 0,611; 0,584; 0,550; 0,577; 0,568. Рассчитайте доверительные границы для среднего результата с доверительной вероятностью 95 %.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – сопротивление электрическое (R), единица измерения – Ом; формула для расчета 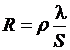 ; исходные данные: удельное электрическое сопротивление
; исходные данные: удельное электрическое сопротивление
ρ = 1,49 · 10-6 Ом· см, длина 10 м, площадь поперечного сечения 0,1256 см2.
ВАРИАНТ 11
Раскройте тему (оформите в виде реферата)
Экология и культура. Биоэтика.
Решите задачи:
1. Исходные концентрации азота и водорода в реакционной смеси для получения аммиака составили 4 и 10 моль/л соответственно. При наступлении равновесия прореагировало 50 % азота. Вычислите равновесные концентрации азота, водорода и аммиака.
2. Дайте термодинамическую характеристику процесса
Al(т) + Fe2O3(т) → Fe(т) + Al2O3(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте фтор по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Получены результаты измерения: 024; 0,23; 0,23; 0,25; 0,25; при за данном значении 0,23. Установите, есть ли систематическая ошибка в результатах измерения?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – скорость (υ), единица измерения – м/с; формула для расчета 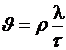 ; исходные данные: время 20 мин, расстояние 3050 фут (1 фут = 0,3048 м).
; исходные данные: время 20 мин, расстояние 3050 фут (1 фут = 0,3048 м).
ВАРИАНТ 12
Раскройте тему (оформите в виде реферата)
Идеи Чижевского о цикличности процессов в Космосе и на Земле.
Решите задачи:
1. Реакция при температуре 40 0С протекает за 180 с. Температурный коэффициент реакции равен 3. За сколько секунд завершиться эта реакция при 60 0С?
2. Дайте термодинамическую характеристику процесса
FeО(т) + O2(г) → Fe2O3(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте йод по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Рассчитайте абсолютное и относительное значения стандартного отклонения следующих величин; 35,12; 35,17; 35,15; 35,11; 35,13. Все ли они входят в доверительный интервал с вероятностью 95 %?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – высота (h), единица измерения – метр (м); формула для расчета 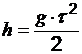 ; исходные данные: время 4 с, скорость падения g = 10 м/с2.
; исходные данные: время 4 с, скорость падения g = 10 м/с2.
ВАРИАНТ 13
Раскройте тему (оформите в виде реферата)
Социальные функции естествознания.
Решите задачи:
1. При наступлении равновесия реакции ![]() концентрации веществ имели следующие значения: азота 0,5 моль/л, водорода 1,5 моль/л, аммиака 1 моль/л. Рассчитайте исходные концентрации азота и водорода.
концентрации веществ имели следующие значения: азота 0,5 моль/л, водорода 1,5 моль/л, аммиака 1 моль/л. Рассчитайте исходные концентрации азота и водорода.
2. Дайте термодинамическую характеристику процесса
Ca(т) + H2O(ж) → Ca(OH)2(т) + H2(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте серу по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Сколько параллельных измерений необходимо выполнить для сужения доверительных границ до ± 0,1 если S = 2,5 с доверительной вероятностью 95 % и 99 %?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – диаметр (d), единица измерения – метр (м); формула для расчета 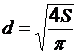 ; исходные данные: площадь круга 15,3 · 102 см2 .
; исходные данные: площадь круга 15,3 · 102 см2 .
ВАРИАНТ 14
Раскройте тему (оформите в виде реферата)
Рождение и эволюция звезд.
Решите задачи:
1. Как измениться скорость химической реакции ![]() ,если давление системы увеличить в 5 раз?
,если давление системы увеличить в 5 раз?
2. Дайте термодинамическую характеристику процесса
СН4(г) + О2(г) → СО2(г) + Н2О(ж)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте кислород по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



