ж) Перечислите все возможные валентности и степени окисления.
4. Найти случайную ошибку измерения и доверительные границы для среднего значения измеряемой величины 21,0; 20,9; 22,0; 21,0; 20,5. Есть ли промах среди результатов измерений? Р = 0,95.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – удельное количество теплоты (q), единица измерения – Дж/кг; формула для расчета 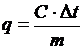 ; исходные данные: масса 120 г, теплоемкость системы С = 300 Дж/град, повышение температуры на 15 градусов.
; исходные данные: масса 120 г, теплоемкость системы С = 300 Дж/град, повышение температуры на 15 градусов.
ВАРИАНТ 15
Раскройте тему (оформите в виде реферата)
Золотое сечение – появление гармонии природы.
Решите задачи:
1. Во сколько раз увеличиться скорость реакции ![]() , если концентрацию водорода увеличить в 2 раза, а азота – в 4 раза?
, если концентрацию водорода увеличить в 2 раза, а азота – в 4 раза?
2. Дайте термодинамическую характеристику процесса
CaO(т) + CO2(г) → CaCO3(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте кальций по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. При измерении массы были получены следующие результаты (мг): 238, 236, 238, 231, 233, 235 при истинном значении 235 мг. Рассчитайте среднее значение, размах варьирования, величину среднего абсолютного и относительного отклонения от среднего значения, абсолютную и относительную погрешности измерения, абсолютную и относительную погрешности среднего значения.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – площадь (S), единица измерения – м2; формула для расчета ![]() ; исходные данные: радиус круга 125 см.
; исходные данные: радиус круга 125 см.
ВАРИАНТ 16
Раскройте тему (оформите в виде реферата)
Экологические заболевания. Пути решения проблемы.
Решите задачи:
1. Обратимая реакция протекает по уравнению: ![]() . Константа равновесия при определенной температуре равна 1. Определить концентрации всех реагирующих веществ при равновесии, зная, что исходные концентрации окиси углерода и водяного пара были 0,02 моль/л.
. Константа равновесия при определенной температуре равна 1. Определить концентрации всех реагирующих веществ при равновесии, зная, что исходные концентрации окиси углерода и водяного пара были 0,02 моль/л.
2. Дайте термодинамическую характеристику процесса
CaO(т) + P2O5(т) → Ca3(PO4)2(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте бром по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Результаты измерения (мг) 398, 396, 398, 392, 393, 401 при эталонном значении 400 мг. Рассчитайте абсолютное и относительное отклонение и погрешности измерения. Все ли значения входят в доверительный интервал с вероятностью 0,95 ?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – работа (А), единица измерения – Джоуль (Дж); формула для расчета ![]() ; исходные данные: сила F = 30 Н (кг · м / с2), длина 0,8 км.
; исходные данные: сила F = 30 Н (кг · м / с2), длина 0,8 км.
1Дж = 1 кг · м2 / с2
ВАРИАНТ 17
Раскройте тему (оформите в виде реферата)
Мутации – неопределенность со стороны биологии.
Решите задачи:
1. Реакция протекает по уравнению: ![]() . Равновесие установилось при следующих концентрациях участвующих в ней веществ: [NO]= 0,02 моль/л, [NО2]= 0,06 моль/л, [О2]= 0,3 моль/л. Определите константу равновесия и исходную концентрацию кислорода.
. Равновесие установилось при следующих концентрациях участвующих в ней веществ: [NO]= 0,02 моль/л, [NО2]= 0,06 моль/л, [О2]= 0,3 моль/л. Определите константу равновесия и исходную концентрацию кислорода.
2. Дайте термодинамическую характеристику процесса
TiO2(т) + H2(г) → Ti(т) + H2O(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте серебро по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Результаты измерения 25, 29, 23, 29, 26. Рассчитайте стандартное отклонение. Определите доверительный интервал для вероятности 0,95.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – количество электричества (Q), единица измерения – кулон (Кл); формула для расчета ![]() ; исходные данные: константа Фарадея F = 96468 А·с/моль, количество вещества 40 ммоль. 1Кл = 1 А· с
; исходные данные: константа Фарадея F = 96468 А·с/моль, количество вещества 40 ммоль. 1Кл = 1 А· с
ВАРИАНТ 18
Раскройте тему (оформите в виде реферата)
Необратимость процессов в природе и стрела времени.
Решите задачи:
1. Равновесие реакции, протекающей по уравнению 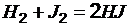 , установилось при следующих концентрациях: [Н2]= 0,004 моль/л, [J2]= 0,025 моль/л, [HJ]= 0,08 моль/л. Определите константу равновесия этой реакции и исходные концентрации йода и водорода.
, установилось при следующих концентрациях: [Н2]= 0,004 моль/л, [J2]= 0,025 моль/л, [HJ]= 0,08 моль/л. Определите константу равновесия этой реакции и исходные концентрации йода и водорода.
2. Дайте термодинамическую характеристику процесса
(СН3)2СО(г) + О2(г) → СО2(г) + Н2О(ж)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте марганец по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Найдите случайную ошибку анализа при Р = 0,95 и доверительные границы для определяемой величины, если результаты её измерения: 3,25; 3,15; 3,08; 3,20; 3,20.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – осмотическое давление (p), единица измерения – Паскаль (Па); формула для расчета 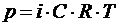 ; исходные данные: концентрация 50 ммоль/л, температура 200С, i = 1, универсальная газовая постоянная R = 8,31 Дж/моль·К.
; исходные данные: концентрация 50 ммоль/л, температура 200С, i = 1, универсальная газовая постоянная R = 8,31 Дж/моль·К.
1 Па = 1 кг · м-1 · с-2, 1 Дж = 1 кг · м2 · с-2
ВАРИАНТ 19
Раскройте тему (оформите в виде реферата)
Причуды генетики. Генная инженерия.
Решите задачи:
1. Константа равновесия для реакции ![]() при 850 0С равна 1. Исходные концентрации воды – 0,03 моль/л, угарного газа – 0,01 моль/л. Определите концентрации всех четырех веществ при равновесии.
при 850 0С равна 1. Исходные концентрации воды – 0,03 моль/л, угарного газа – 0,01 моль/л. Определите концентрации всех четырех веществ при равновесии.
2. Дайте термодинамическую характеристику процесса
С2Н2(г) → С6Н6(ж)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте никель по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Сколько параллельных измерений необходимо выполнить, если границы доверительного интервала ± 0,10; стандартное отклонение S = 2,5, а доверительная вероятность —95%?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – объем (V), единица измерения – м3; формула для расчета 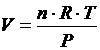 ; исходные данные: n = 1,7 моль, температура 100С, R = 8,31 Дж/моль·К, давление Р = 101,3 кПа.
; исходные данные: n = 1,7 моль, температура 100С, R = 8,31 Дж/моль·К, давление Р = 101,3 кПа.
1 Па = 1 кг · м-1 · с-2, 1 Дж = 1 кг · м2 · с-2
ВАРИАНТ 20
Раскройте тему (оформите в виде реферата)
Эволюция и становление интеллекта. Искусственный интеллект и эволюционное моделирование.
Решите задачи:
1. Как измениться скорость реакции ![]() , если увеличить объем газовой смеси в 3 раза и предположить, что реакция протекает в соответствии с законом действующих масс?
, если увеличить объем газовой смеси в 3 раза и предположить, что реакция протекает в соответствии с законом действующих масс?
2. Дайте термодинамическую характеристику процесса
Hg(CNO)2(т) → Hg(ж) + CO(г) + N2(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте азот по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Покажите, является ли «промахом» измеренная величина 50,5 среди результатов 48,0; 49,1; 48,7; 49,95; 50,1; 50,3.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – сила тяготения (F), единица измерения – ньютон (Н); формула для расчета 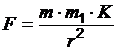 ; исходные данные: m1 = 200 г, m = 500 мг, r = 2 см,
; исходные данные: m1 = 200 г, m = 500 мг, r = 2 см,
К = 6,67 · 10-11 Н · м2/ кг2.
ВАРИАНТ 21
Раскройте тему (оформите в виде реферата)
Физические поля в организме человека и возможности медицинской диагностики.
Решите задачи:
1. При некоторой температуре константа равновесия реакции 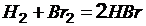 равна 1. Определите состав равновесной смеси, если для реакции были взяты 1 моль водорода и 2 моль брома.
равна 1. Определите состав равновесной смеси, если для реакции были взяты 1 моль водорода и 2 моль брома.
2. Дайте термодинамическую характеристику процесса
H2(г) + O2(г) → H2O(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте углерод по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Установите, имеется ли систематическая ошибка в результатах измерений: 121,5; 102,5; 120,0; 122,0 при заданном значении 124,0.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – количество вещества (n), единица измерения – моль; формула для расчета 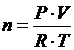 ; исходные данные: температура 200С, R = 8,31 Дж/моль · К, V = 22,4 л, Р = 7,5 · 10-3 мм Hg = 1 Па = 1 кг · м-1 · с-2; 1 Дж = 1 кг · м2 · с-2
; исходные данные: температура 200С, R = 8,31 Дж/моль · К, V = 22,4 л, Р = 7,5 · 10-3 мм Hg = 1 Па = 1 кг · м-1 · с-2; 1 Дж = 1 кг · м2 · с-2
ВАРИАНТ 22
Раскройте тему (оформите в виде реферата)
Мир живого на молекулярном уровне.
Решите задачи:
1. Определите равновесные количества веществ в реакции 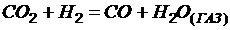 ,если константа равновесия при некоторой температуре равна 1 и для реакции было взято 1 моль углекислого газа и 3 моль водорода.
,если константа равновесия при некоторой температуре равна 1 и для реакции было взято 1 моль углекислого газа и 3 моль водорода.
2. Дайте термодинамическую характеристику процесса
CaO(т) + H2(г) → H2O(г) + Ca(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте барий по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Рассчитайте абсолютное и относительное значение стандартного отклонения результатов измерений: 11,11; 11,12; 11,15; 11,10; 11,11; 11,13. Определите, есть ли «промахи» в результатах измерений?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – константа скорости реакции (к), единица измерения – с-1; формула для расчета 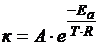 ; исходные данные: температура 6800С, А = 4,2 · 1029 с-1, Еа = 0,45 кДж/моль, е = 2,71, R = 8,31 Дж / моль · К.
; исходные данные: температура 6800С, А = 4,2 · 1029 с-1, Еа = 0,45 кДж/моль, е = 2,71, R = 8,31 Дж / моль · К.
ВАРИАНТ 23
Раскройте тему (оформите в виде реферата)
Биосфера и предельные возможности Земли.
Решите задачи:
1. Равновесие в системе ![]() при некоторой температуре установилось при концентрациях в моль/м3: [NO2]=0,06; [NO]=0,24; [O2]=0,12. Определите константу равновесия и рассчитайте исходную концентрацию NO2.
при некоторой температуре установилось при концентрациях в моль/м3: [NO2]=0,06; [NO]=0,24; [O2]=0,12. Определите константу равновесия и рассчитайте исходную концентрацию NO2.
2. Дайте термодинамическую характеристику процесса
Fe(т) + O2(г) → Fe2O3(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте цинк по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Сколько параллельных измерений необходимо выполнить для сужения доверительного интервала до ± 0,15, если эмпирическое стандартное отклонение равно 2,50, а вероятность — 95%?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – температура (Т), единица измерения – Кельвин (К); формула для расчета 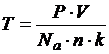 ; исходные данные: Na = 6,02 · 1023 моль-1, V = 800 л, n = 3 кмоль, k = 1,38 · 10-23 Дж/К, Р = 760 мм Hg. 1 Дж = 1 кг · м2 · с-2. 1 мм Hg = 133,3 Па, 1 Па = 1 кг · м-1 · с-2.
; исходные данные: Na = 6,02 · 1023 моль-1, V = 800 л, n = 3 кмоль, k = 1,38 · 10-23 Дж/К, Р = 760 мм Hg. 1 Дж = 1 кг · м2 · с-2. 1 мм Hg = 133,3 Па, 1 Па = 1 кг · м-1 · с-2.
ВАРИАНТ 24
Раскройте тему (оформите в виде реферата)
Экологические основы феномена здоровья.
Решите задачи:
1. В начальный момент протекания реакции ![]() концентрации были равны (моль/л): азота - 1,5; водорода - 2,5; аммиака - 0. Каковы концентрации азота и водорода при концентрации аммиака равной 0,5 моль/л?
концентрации были равны (моль/л): азота - 1,5; водорода - 2,5; аммиака - 0. Каковы концентрации азота и водорода при концентрации аммиака равной 0,5 моль/л?
2. Дайте термодинамическую характеристику процесса
CaC2(т) + H2O(г) → Ca(OH)2(т) + C2H2(г)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте таллий по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Результаты измерения 8,25; 8,15; 8,08; 8,20; 8,02. Найти случайную ошибку анализа при Р = 0,95 и границы доверительного интервала.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – молярная концентрация вещества (С), единица измерения – моль/дм3; формула для расчета 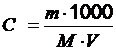 ; исходные данные: масса 1,250 кг, объем 5 · 106 мл, молярная масса М = 60,7 г/моль.
; исходные данные: масса 1,250 кг, объем 5 · 106 мл, молярная масса М = 60,7 г/моль.
ВАРИАНТ 25
Раскройте тему (оформите в виде реферата)
Концепция Пригожина «от существующего к возникающему».
Решите задачи:
1. Начальные концентрации веществ в реакции ![]() были равны (моль/м3): оксида углерода (II) - 0,05; паров воды - 0,06; оксида углерода (IV) - 0,4; водорода - 0,2. Вычислите концентрации всех реагирующих веществ, после того как прореагировало 60 % Н2О.
были равны (моль/м3): оксида углерода (II) - 0,05; паров воды - 0,06; оксида углерода (IV) - 0,4; водорода - 0,2. Вычислите концентрации всех реагирующих веществ, после того как прореагировало 60 % Н2О.
2. Дайте термодинамическую характеристику процесса
N2(г) + H2O(ж) → NH4NO2(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо- или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте медь по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Получены результаты измерения: 0,525; 0,611; 0,584; 0,550; 0,577; 0,568. Рассчитайте доверительные границы для среднего результата с доверительной вероятностью 95 %.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – молярная масса вещества (М), единица измерения – г/моль; формула для расчета 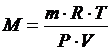 ; исходные данные: масса 0,015 кг, объем 22,4 л, температура 250С, Р = 109 Н/мм2, R = 8,31 Дж/моль·К. 1 Дж = 1 кг · м2 · с-2, 1Па = 106 Н/мм2, 1 Па = 1 кг · м-1 · с-2.
; исходные данные: масса 0,015 кг, объем 22,4 л, температура 250С, Р = 109 Н/мм2, R = 8,31 Дж/моль·К. 1 Дж = 1 кг · м2 · с-2, 1Па = 106 Н/мм2, 1 Па = 1 кг · м-1 · с-2.
ВАРИАНТ 26
Раскройте тему (оформите в виде реферата)
Модель Большого взрыва.
Решите задачи:
1. При синтезе фосгена имеет место равновесие реакции 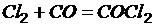 Определите исходные концентрации хлора и оксида углерода, если равновесные концентрации в моль/м3 равны: [Cl2] = 2,5; [CO] = 1,8; [COCl2] = 3,2
Определите исходные концентрации хлора и оксида углерода, если равновесные концентрации в моль/м3 равны: [Cl2] = 2,5; [CO] = 1,8; [COCl2] = 3,2
2. Дайте термодинамическую характеристику процесса
Ca(OH)2(т) + CO2(г) → CaCO3(т) + H2O(ж)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте мышьяк по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Получены результаты измерения: 024; 0,23; 0,23; 0,25; 0,25; при за данном значении 0,23. Установите, есть ли систематическая ошибка в результатах измерения?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – криоскопический коэффициент (Кт), единица измерения – К·кг/моль; формула для расчета 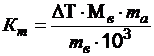 ; исходные данные: изменение температуры на 0,650С, Мв = 556 г/моль, mа = 0,7 кг, mв = 50,4 г.
; исходные данные: изменение температуры на 0,650С, Мв = 556 г/моль, mа = 0,7 кг, mв = 50,4 г.
ВАРИАНТ 27
Раскройте тему (оформите в виде реферата)
Химические процессы в живой природе и молекулярная самоорганизация (мутагенез, гомеостаз).
Решите задачи:
1. Определите равновесную концентрацию водорода в реакции 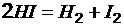 , если исходная концентрация HI составляет 0,55 моль/м3, а константа равновесия равна 0,12.
, если исходная концентрация HI составляет 0,55 моль/м3, а константа равновесия равна 0,12.
2. Дайте термодинамическую характеристику процесса
CaSO4 · 0,5 H2O(т) + H2O(ж) → CaSO4 · 2 H2O(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте селен по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Рассчитайте абсолютное и относительное значения стандартного отклонения следующих величин; 35,12; 35,17; 35,15; 35,11; 35,13. Все ли они входят в доверительный интервал с вероятностью 95 %?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – молярный объем (Vn), единица измерения – м3/моль; формула для расчета 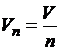 ; исходные данные: объем 550 дм3, количество вещества 0,15 кмоль.
; исходные данные: объем 550 дм3, количество вещества 0,15 кмоль.
ВАРИАНТ 28
Раскройте тему (оформите в виде реферата)
Единство человека и природы.
Решите задачи:
1. Реакция протекает по уравнению ![]() . Как изменится скорость реакции после разбавления реагирующей смеси в 4 раза?
. Как изменится скорость реакции после разбавления реагирующей смеси в 4 раза?
2. Дайте термодинамическую характеристику процесса
Ca(OH)2(т) + MgSO4(т) → CaSO4(т) + Mg(OH)2(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте молибден по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Сколько параллельных измерений необходимо выполнить для сужения доверительных границ до ± 0,1 если S = 2,5 с доверительной вероятностью 95 % и 99 %?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – удельный объем (Vm), единица измерения – 1000 · м3/кг; формула для расчета 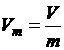 ; исходные данные: масса 200 г, объем 40 см3 .
; исходные данные: масса 200 г, объем 40 см3 .
ВАРИАНТ 29
Раскройте тему (оформите в виде реферата)
Понятие о внутреннем, активном, астрономическом и биологическом времени.
Решите задачи:
1. В каком направлении сместится равновесие реакции ![]() , если концентрации всех реагирующих веществ уменьшить в 3 раза?
, если концентрации всех реагирующих веществ уменьшить в 3 раза?
2. Дайте термодинамическую характеристику процесса
Fe(т) + O2(г) → FeO(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте олово по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Найти случайную ошибку измерения и доверительные границы для среднего значения измеряемой величины 21,0; 20,9; 22,0; 21,0; 20,5. Есть ли промах среди результатов измерений? Р = 0,95.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – плотность тока (i), единица измерения – А/м2; формула для расчета ![]() ; исходные данные: время 2 часа, площадь 150 см2, F=96484 Кл/моль, количество вещества 60 моль;
; исходные данные: время 2 часа, площадь 150 см2, F=96484 Кл/моль, количество вещества 60 моль; 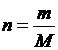 ; 1Кл = 1 А · с.
; 1Кл = 1 А · с.
ВАРИАНТ 30
Раскройте тему (оформите в виде реферата)
Разум и информационное поле.
Решите задачи:
1. Реакция идет по уравнению ![]() . Как изменится скорость реакции, если увеличить давление в 2 раза?
. Как изменится скорость реакции, если увеличить давление в 2 раза?
2. Дайте термодинамическую характеристику процесса
Ca(OH)2(т) + H2SO4(ж) → CaSO4(т) + H2O(ж)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте сурьму по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. При измерении массы были получены следующие результаты (мг): 238, 236, 238, 231, 233, 235 при истинном значении 235 мг. Рассчитайте среднее значение, размах варьирования, величину среднего абсолютного и относительного отклонения от среднего значения, абсолютную и относительную погрешности измерения, абсолютную и относительную погрешности среднего значения.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – эбуллиоскопический коэффициент (Эт), единица измерения – К · кг/моль; формула для расчета 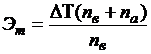 ; исходные данные: mв = 5,14 г, mа = 0,2 кг, Мв = 212 г/моль, Ма = 48 г/моль,
; исходные данные: mв = 5,14 г, mа = 0,2 кг, Мв = 212 г/моль, Ма = 48 г/моль, 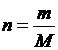 , повышение температуры на 0,475 градусов.
, повышение температуры на 0,475 градусов.
ВАРИАНТ 31
Раскройте тему (оформите в виде реферата)
Бифуркация, динамический хаос и теория катастроф.
Решите задачи:
1. Вычислите, при какой температуре реакция закончится за 45 минут, если при 293 К на это требуется 3 часа. Температурный коэффициент равен 3,2.
2.Дайте термодинамическую характеристику процесса
Ca(OH)2(т) + CO2(г) + H2O(ж) → Ca(HCO3)2(ж)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте кобальт по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Результаты измерения (мг) 398, 396, 398, 392, 393, 401 при эталонном значении 400 мг. Рассчитайте абсолютное и относительное отклонение и погрешности измерения. Все ли значения входят в доверительный интервал с вероятностью 0,95 ?
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – время (τ), единица измерения – секунда (с); формула для расчета 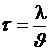 ; исходные данные: расстояние 3050 футов (1 фут=0,3048 м), скорость движения 50 км/час.
; исходные данные: расстояние 3050 футов (1 фут=0,3048 м), скорость движения 50 км/час.
ВАРИАНТ 32
Раскройте тему (оформите в виде реферата)
Основные проблемы экологии и роль окружающей среды для жизни.
Решите задачи:
1. Для практической остановки реакции применяют быстрое охлаждение реакционной смеси. Определите, во сколько раз изменится скорость реакции при охлаждении реакционной смеси с 40 0С до -10 0С, если температурный коэффициент реакции равен 2,7.
2. Дайте термодинамическую характеристику процесса
CaO(т) + SiO2(т) → CaSiO3(т)
по плану:
а) Выпишите термодинамические функции участвующих веществ.
б) Запишите стехиометрическое уравнение.
в) Рассчитайте изменение стандартной энтальпии химической реакции.
г) Определите, является реакция экзо - или эндотермической; увеличивается или уменьшается температура в системе в результате протекания данной реакции.
д) Рассчитайте изменение стандартной энтропии реакции, объясните изменение энтропии в ходе реакции.
е) Рассчитайте стандартное изменение энергии Гиббса по балансовому уравнению и уравнению Гиббса. Дайте анализ полученным данным.
ж) Для обратимой реакции рассчитайте равновесную температуру согласно уравнению Гиббса.
з) Сделайте вывод о самопроизвольности протекания химической реакции.
3. Охарактеризуйте ртуть по положению в Периодической системе по плану:
а) Укажите название элемента, его обозначение. Определите его порядковый номер, номер периода, группу, подгруппу.
б) Укажите количество электронов, протонов и нейтронов в атоме элемента, заряд ядра, массовое число.
в) Составьте полную электронную формулу элемента, определите электронное семейство, отнесите простое вещество к классу металлов или неметаллов.
г) Изобразите графически электронную структуру элемента (двух последних уровней).
д) Укажите число и тип валентных электронов.
е) Графически изобразите валентные состояния.
ж) Перечислите все возможные валентности и степени окисления.
4. Результаты измерения 25, 29, 23, 29, 26. Рассчитайте стандартное отклонение. Определите доверительный интервал для вероятности 0,95.
5. Определите значение физической величины и выведите для нее формулу размерности: физическая величина – масса (m), единица измерения – килограмм (кг); формула для расчета 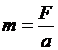 ; исходные данные: сила 60 Н (Н=кг·м·с-2), ускорение 80 см/с2.
; исходные данные: сила 60 Н (Н=кг·м·с-2), ускорение 80 см/с2.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



