2) Sr2+ б) NaCl
3) Ca2+ в) (NH4)2C2O4
г) (NH4)2SO4
8. УСТАНОВИТЕ СООТВЕТСТВИЕ МЕЖДУ ОКРАСКОЙ ВЕЩЕСТВА И ЕГО ХИМИЧЕСКОЙ ФОРМУЛОЙ
Цвет вещества Химическая формула
1) белый а) [Cu(NH3)4]SO4
2) черный б) CuCl2
3) голубой в) CuS
4) зеленый г) CuСl
д) Cu(OH)2
9. ДЕЙСТВИЕМ BACL2 + HCl ОБНАРУЖИВАЮТ __________ - АНИОНЫ.
10. СОГЛАСНО КЛАССИФИКАЦИИ АНИОНОВ, ОСНОВАННОЙ НА РАЗЛИЧНОЙ РАСТВОРИМОСТИ СОЛЕЙ БАРИЯ И СЕРЕБРА В ВОДЕ, АНИОНЫ SO4 2-, SO3 2-, S2O3 2- ОТНОСЯТ К ___ ГРУППЕ.
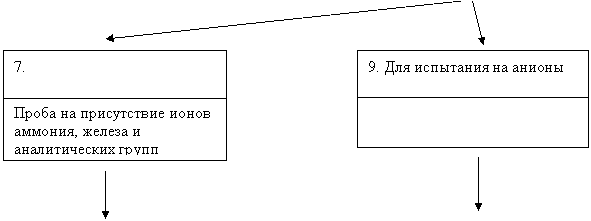
2) Дополните схему, вставив в пустые клетки нужные операции.
Анализ сухой соли
| |||||||||||||||||
| |||||||||||||||||
 | |||||||||||||||||
 | |||||||||||||||||
 | |||||||||||||||||
 |  | ||||||||||||||||
|
| ||||||||||||||||
 | |||||||||||||||||
|
| ||||||||||||||||
ЛАБОРАТОРНАЯ РАБОТА № 11
Определение кристаллизационной воды
в кристаллогидрате хлорида бария BaCl2· 2H2O
Цель: изучить гравиметрическое определение вещества, удаляемого в процессе выполнения анализа
Реактивы и оборудование: исследуемый образец (BaCl2 · 2H2O), бюкс, весы технические и аналитические, сушильный шкаф, эксикатор
Инструктаж по технике безопасности.
Порядок выполнения работы:
I. ПРОВЕДЕНИЕ ГРАВИМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ВЕЩЕСТВА
1. Тщательно вымытый бюкс высушите в сушильном шкафу при температуре 1250С в течение 30 минут.
2. Бюкс с крышкой охладите в эксикаторе до температуры весовой комнаты и взвесьте на аналитических весах.
3. После первого взвешивания бюкс вновь поставьте в сушильный шкаф на 15 минут при той же температуре, снова взвесьте его.
Если масса бюкса не изменилась или изменяется незначительно (не более чем на 0,0002 г), высушивание считается законченным
4. Расчет величины навески
Исходные данные:
М(BaCl2 · 2H2O) = 244,28 г/моль
М(H2O) = 18,02 г/моль
m (H2O) = 0,1 г.
Расчет:
244,28 г BaCl2 · 2H2O – 36,04 г H2O
х г BaCl2 · 2H2O – 0,1 г H2O
х = (244,28 · 0,1) / 36,04 = 0,7(г)
5. Необходимое количество растворимого вещества отвесьте на аналитических весах с точностью до четырех десятичных знаков.
6. В высушенный и взвешенный бюкс поместите рассчитанное количество исследуемого образца BaCl2 · 2H2O и определите точную массу бюкса с навеской.
7. Приоткрыв бюкс поставьте его в сушильный шкаф и пробу высушивайте при 1250С в течение часа.
8. После высушивания бюкс закройте крышкой, охладите в эксикаторе и взвесьте.
9. Пробу высушивайте второй раз в течение 30 минут, вторично охладите в эксикаторе и взвесьте.
Если изменение массы не превышает 0,0002г, то удаление воды следует считать законченным.
10. Операции по высушиванию, охлаждению и взвешиванию повторяйте до тех пор, пока масса бюкса не будет постоянной.
II. ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ
1. Взятие навески хлорида бария ВаС12 × 2 Н2О
Масса бюкса с хлоридом бария, г … 17,5831
Масса пустого бюкса с крышкой, г … 16,8223
Масса навески ВаС12 × 2 Н2О, г. … 0,7608
2. Высушивание навески хлорида бария.
Масса бюкса с хлоридом бария после высушивания, г
1-е взвешивание … 17,4896
2-е взвешивание … 17,4712
3-е взвешивание … 17,4712
3. Вычисление массы кристаллизационной йоды:
17,5831 – 17,4712 = 0,1119 г.
4. Содержание (%) кристаллизационной воды вычисляют по формуле:
Исходную навеску 0,7608 г принимаем за 100%
0,1119 - х %
х = 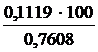 = 14,71%
= 14,71%
5. Ошибка определения.
Масса воды, входящая в формулу кристаллогидрата, является величиной теоретической и вычисляется из пропорции:
в 244,3 г ВаС12 × 2Н2О содержится 36 г Н2О
в 100г ВаС12 × 2Н2О - х Н2О
х = 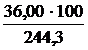 = 14,75%
= 14,75%
6. Абсолютная ошибка.
Разность между полученной и теоретической величинами является абсолютной ошибкой определения: 14,71– 14,75 = – 0,04 %.
7. Относительная ошибка:
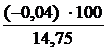 = – 0,27%
= – 0,27%
Контрольные вопросы:
1. В чем сущность гравиметрического метода анализа.
2. Для каких целей гравиметрический метод применяется в пищевых лабораториях?
3. Какая лабораторная посуда используется для гравиметрического анализа?
4. Каковы этапы гравиметрического метода?
5. Сколько меди содержится в 0,7 г СuSО4?
ЛАБОРАТОРНАЯ РАБОТА № 12
Приготовление рабочего раствора щелочи и
стандартного раствора щавелевой кислоты
Цель: научиться готовить рабочий раствор щелочи и стандартный раствор щавелевой кислоты
Реактивы и оборудование: свежеперекристаллизованная H2C2O4· 2Н2O, образец NaOH, раствор BaCl2 , раствор фенолфталеина, свежепрокипяченная дистиллированная вода, весы технические и аналитические, бюкс, измерительная посуда, титровальная установка
Инструктаж по технике безопасности.
Порядок выполнения работы:
I. ПРИГОТОВЛЕНИЕ РАСТВОРОВ
Приготовление раствора NaOH, С (NaOH) = 0,1 моль/л
Точный раствор NaOH приготовить из навески нельзя, так как при хранении гидроксид натрия как в твердом виде, так и в растворе поглощает из воздуха влагу и углекислый газ, поэтому он всегда содержит примесь карбоната.
Процесс взаимодействия NaOH с СО2 воздуха выражается уравнением: 2NaOH + СО2 = Na2СО3 + Н2O.
1. Расчет навески
Исходные данные:
С (NaOH) – 0,1 моль/л
Объем раствора – 250 мл
М (NaOH) – 40 г/моль
m(NaOH) = ![]() =
= ![]() = 1,0002 г
= 1,0002 г
Так как NaOH всегда содержит примеси, на технохимических весах берут большую навеску: 1,5 или 2,0 г.
2. Отмерьте 250 мл прокипяченной дистиллированной воды.
3. Навеску перенесите в фарфоровую кружку (растворение щелочи идет с сильным разогреванием).
4. Добавьте 15-20 мл дистиллированной воды, обмойте навеску, чтобы удалить примеси карбоната натрия с поверхности, и быстро слейте эту воду.
5. Залейте навеску частью отмеренного объема прокипяченной дистиллированной воды и растворите ее, затем прибавьте остальной объем воды.
6. Раствор хорошо перемешайте и сохраняйте в плотно закрытой склянке.
Приготовление установочного раствора Н2С2О2 · 2Н2О
1. Расчет навески
Исходные данные:
Емкость мерной колбы – 100 мл
М(½Н2С2О4 · 2Н2О) = ½ М(Н2С2О4 · 2Н2О)= ½ · 126,07=63,04 г/моль
С(½Н2С2О4 · 2Н2О) ≈ С(NaOH) ≈ 0,1 моль/л
m(Н2С2О4· 2Н2О) = [C(½Н2С2О4 · 2Н2О) · М(½Н2С2О4 · 2Н2О) · 100]/1000 =
= (63,04 · 0,1 · 100) / 1000 ≈ 0,63 г
2. Рассчитанную навеску H2C2O4 · 2H2O взвесьте на аналитических весах.
3. Перенесите в мерную колбу вместимостью 100 мл.
4. Растворите при перемешивании в дистиллированной воде, доводя объем до метки.
Контрольные вопросы:
1. В чем сущность метода нейтрализации? Какая химическая реакция лежит в основе этого метода?
2. Что называют стандартным раствором?
3. Каковы операции в титриметрическом методе?
4. Какая лабораторная посуда используется в титриметрическом анализе?
5. Как рассчитать навеску для приготовления раствора?
ЛАБОРАТОРНАЯ РАБОТА № 13
Определение нормальности и титра раствора щелочи
Цель: научиться определять нормальность и титр раствора щелочи
Реактивы и оборудование: свежеперекристаллизованная H2C2O4· 2Н2O, образец NaOH, раствор BaCl2, раствор фенолфталеина, свежепрокипяченная дистиллированная вода, весы технические и аналитические, бюкс, измерительная посуда, титровальная установка
Инструктаж по технике безопасности
Порядок выполнения работы:
I. ПРОВЕДЕНИЕ ТИТРОВАНИЯ
Реакция протекает по уравнению:
2NaOH+ Н2С2О4 = Na2С2O4 + 2Н2О
1. Бюретку заполните исследуемым раствором щелочи до нулевого деления, полученным в лабораторной работе № 12.
2. В колбу для титрования отмерьте пипеткой определенный объем приготовленного титрованного раствора щавелевой кислоты (5,0 мл) полученной в лабораторной работе № 12.
3. Добавьте 1–2 капли фенолфталеина и титруйте раствором щелочи до точки эквивалентности. Точка эквивалентности определяется по появлению светло-розового окрашивания, не исчезающего в течение 30 секунд.
4. Титрование проводите до получения 3-х сходящихся результатов.
II. ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ
Исходные данные:
N (1/2 H2C2O4) = 0,1 моль/л
V (Н2С2О4 · 2Н2О) = 5 мл
М (NaOH) = 40г/моль
М (½Н2С2О4) = ½М(Н2С2О4) = ½ · 98 = 49г/моль
Результаты титрования:
Объем NaOH, израсходованный на I-е титрование
Объем NaOH, израсходованный на 2-е титрование
Объем NaOH, израсходованный на 3-е титрование
Средний объем NaOH
Вычисления:
N (NaOH) · V (NaOH) = N (½Н2С2О4 · 2Н2О) · V (Н2С2О4 · 2Н2О)
Т (NaOH) = [N(NaOH) · М (NaOH)] / 1000
N (NaOH) = [N (½Н2С2О4 · 2Н2О)·V (Н2С2О4 · 2Н2О)] / V(NaOH)
Т (NaOH/Н2С2О4) = [N (NaOH) · М (½Н2С2О4)]/1000
Контрольные вопросы и задания:
1. Что такое титрованный раствор?
2. Что такое установочное вещество?
3. Что такое нормальная концентрация раствора, титр, титр по определяемому веществу?
4. Из каких этапов складывается определение титра и нормальной концентрации стандартного раствора?
5. Какова нормальность и титр раствора НСl, если на титрование 25 мл 0,2 н. раствора Na2СО3 затрачено 22 мл раствора соляной кислоты?
6. Сколько миллилитров 0,15 н. раствора NaОН пойдет на тирование 21мл НСl с титром 0,0038 г/мл?
7. Сколько грамм СаО нейтрализуют 10 мл 0,25 М НСl?
ЛАБОРАТОРНАЯ РАБОТА № 14
Определение содержания серной кислоты в растворе
Цель: научиться определять содержание серной кислоты в растворе
Реактивы и оборудование: исследуемый образец кислоты, стандартный раствор 0,1 н. NaOH, раствор фенолфталеина, дистиллированная вода, измерительная посуда, титровальная установка
Инструктаж по технике безопасности.
Порядок выполнения работы:
I. МЕТОДИКА ВЫПОЛНЕНИЯ РАБОТЫ
Реакция протекает по уравнению:
2 NaOH + Н2SO4 = Na2SO4 + 2Н2O
1. Контрольный раствор Н2SO4 разбавьте дистиллированной водой в мерной колбе вместимостью 100 мл и объем раствора доведите до метки, тщательно перемешайте.
2. Бюретку заполните исследуемым раствором щелочи до нулевого деления, полученным в лабораторной работе № 12.
3. В коническую колбу отберите при помощи пипетки определенный объем (10,00 мл) исследуемого раствора Н2SO4.
4. Прибавьте 1-2 капли фенолфталеина и титруйте стандартным раствором гидроксида натрия до появления бледно-розовой окраски.
5. Определение повторите трижды и для расчетов возьмите среднее значение.
II. ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ
Исходные данные:
C (NaOH) = 0,1 моль/л
V (Н2SO4) = 10,00 мл
М(NaOH) = 40 г/моль
М(½Н2SO4) = ½М(Н2SO4) = ½ · 98 = 49 г/моль
Vмерной колбы = 100 мл
Результаты титрования:
Объем NaOH, израсходованный на 1-е титрование
Объем NaOH, израсходованный на 2-е титрование
Объем NaOH, израсходованный на 3-е титрование
Средний объем NaOH
3. Вычисления
1-й способ.
Вычисляем нормальную концентрацию раствора Н2SO4:
С(Н2SO4) = 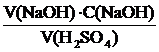
Титр раствора Н2SO4:
Т (Н2SO4) = 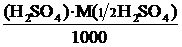
Отсюда содержание Н2SO4 в 100 мл раствора составляет:
m(Н2SO4) = Т(Н2SO4) · 100
2-й способ.
Вычисляем титр NaOH по серной кислоте:
Т(NaOH/Н2SO4) = 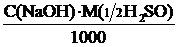
Отсюда содержание Н2SO4 в 100 мл раствора составляет:
m(Н2SO4) = 
Контрольные вопросы и задания:
1. В чем сущность метода нейтрализации? Какая химическая реакция лежит в основе этого метода?
2. Что такое стандартный или титрованный раствор?
3. Что такое индикатор? Как правильно подобрать индикатор к данному случаю титрования?
4. Как рассчитать содержание кислоты или щелочи в растворе?
5. Сколько миллилитров 0,2 н раствора HCl потребуется для реакции с 15 мл 0,075 н раствора Вa(OH)2?
ЛАБОРАТОРНАЯ РАБОТА № 15
Приготовление рабочего раствора перманганата калия и установление нормальной концентрации и титра по щавелевой кислоте
Цель: научиться готовить стандартный раствор перманганата калия и определять его концентрацию и титр (по щавелевой кислоте) в растворе
Реактивы и оборудование: образцы х. ч. Н2С2O4 · 2H2O, КMnO4, Н2SO4, водяная баня, склянка из темного стекла, измерительная посуда, весы технические и аналитические, бюкс, титровальная установка, промывалка
Инструктаж по технике безопасности
Порядок выполнения работы:
I. ПРИГОТОВЛЕНИЕ РАСТВОРА: КMnO4, С(1/5КMnO4) = 0,1 моль/л
Перманганат калия содержит примесь MnO2, а также часть его расходуется на окисление, имеющихся в воде восстановителей.
По этой причине стандартный раствор перманганата калия путем взятия точной навески готовить нельзя. Приготовление раствора начинают с расчета навески, необходимой для приготовления раствора заданной концентрации и объема.
1. Расчет величины навески
Исходные данные:
С (1/5КMnO4) = 0,1моль/л
V р-ра = 250 мл
М(1/5 КMnO4) = 1/5М(КMnO4) = 1/5 · 158,04 = 31,61 г/моль
Расчет:
m(КМnO4) = 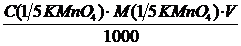 =
= 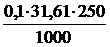 = 0,8 г
= 0,8 г
Так как часть КМnO4 будет израсходована на окисление органических примесей, попавших в дистиллированную воду из воздуха, навеску следует увеличить приблизительно на 10%, т. е. взять около 0,88 г.
2. Взяв навеску на технических весах, растворите в колбе вместимостью 250 мл и оставьте в темном месте.
3. Через 8-10 дней раствор отфильтруйте от выпавшего осадка через стеклянную вату (бумажным фильтром пользоваться нельзя, так как бумага восстанавливает перманганат).
II. ПРИГОТОВЛЕНИЕ УСТАНОВОЧНОГО РАСТВОРА Н2С2O4 · 2H2O
1. Расчет величины навески
Исходные данные:
С(½Н2С2O4·2H2O) = С(1/5 КMnO4) = 0,1 моль/л
V р-ра = 100 мл
М(½Н2С2O4·2H2O) = ½М(Н2С2O4·2H2O) = ½ · 126,07 = 63,04 г/моль
Расчет:
m(Н2С2O4·2H2O) = 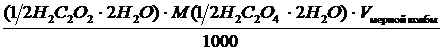
= 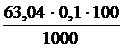 = 0,63 г
= 0,63 г
2. Количественные данные для приготовления установочного раствора
Н2С2O4· 2H2O
Масса бюкса с навеской
Масса бюкса с остатками навески
Масса навески
Объем мерной колбы
3. Точную навеску щавелевой кислоты Н2С2O4 · 2H2O растворите в мерной колбе на 100 мл и объем доведите до метки.
4. Полученный раствор хорошо перемешайте.
5. Рассчитайте титр и молярную концентрацию Н2С2O4· 2H2O
Т (Н2С2O4· 2H2O) = 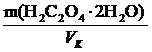
С (½Н2С2O4· 2H2O) = 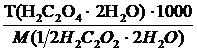
III. ОПРЕДЕЛЕНИЕ ТИТРА И МОЛЯРНОЙ КОНЦЕНТРАЦИИ ЭКВИВАЛЕНТОВ РАСТВОРА ПЕРМАНГАНАТА КАЛИЯ
Реакция протекает по уравнении:
2 КMnO4+ 5Н2С2O4 + 3Н2SO4= 2МnSO4+K2SO4+10CO2+8H2O
 |
МnO![]() + 8H+ + 5
+ 8H+ + 5![]() → Мn2+ + 4H2O 2
→ Мn2+ + 4H2O 2
C2O![]() -2
-2![]() → 2CO2 5
→ 2CO2 5
2 МnO![]() + C2O
+ C2O![]() + 16H+ = 2Mn2+ + 8H2O + 10CO2
+ 16H+ = 2Mn2+ + 8H2O + 10CO2
1. Бюретку ополосните раствором КMnO4 и заполните до нулевого деления.
2. Пипетку ополосните раствором щавелевой кислоты и 10 мл ее перенесите в колбу для титрования.
3. Туда же мерным цилиндром добавьте 8-10 мл 2 н. Н2SO4 и раствор нагрейте на водяной бане до 60-700С.
4. Горячий раствор щавелевой кислоты оттитруйте раствором КMnO4.
5. Добавляйте каплю раствора КMnO4 , интенсивно перемешивая раствор, добиваясь его обесцвечивания, и только после этого прибавляйте следующую.
6. Медленно обесцвечиваются только первые капли.
7. Когда будет достигнута точка эквивалентности, следующая капля стандартного раствора обесцвечиваться не будет и окрасит жидкость в бледно - розовый цвет.
8. Определение повторите трижды и для расчетов возьмите среднее значение.
9. Количественные данные определения точной концентрации раствора КMnO4
Концентрация установочного раствора Н2С2O4· 2H2O
Объем Н2С2O4· 2H2O, взятого на титрование
Объем КMnO4, израсходованного на 1-е титрование
Объем КMnO4, израсходованного на 2-е титрование
Объем КMnO4, израсходованного на 3-е титрование
Средний объем КMnO4
10. Расчет результата определения точной концентрации раствора КMnO4:
С(1/5КMnO4)·V(КMnO4) = С(½Н2С2O4· 2H2O)· V(Н2С2O4· 2H2O)
 С(½Н2С2O4· 2H2O)· V(Н2С2O4· 2H2O)
С(½Н2С2O4· 2H2O)· V(Н2С2O4· 2H2O)
С(1/5КMnO4)= V(КMnO4)
С(1/5КMnO4) · М(1/5КMnO4)
 T(КMnO4) = 1000
T(КMnO4) = 1000
Контрольные вопросы и задания:
1. На чем основан метод окисления - восстановления?
2. Каким требованиям должны отвечать реакции окисления - восстановления, чтобы их можно было использовать в количественном анализе?
3. Почему нельзя готовить точный раствор КMnO4 прямо из навески?
4. Определите нормальность раствора перманганата калия, если 20,00 мл его окисляют такую навеску щавелевой кислоты, которая может быть нейтрализована 15,60 мл 0,0950 н. раствора гидроксида натрия.
ЛАБОРАТОРНАЯ РАБОТА № 16
Определение содержания железа в соли Мора
Цели: научиться определять концентрацию железа (в соли Мора) в растворе
Реактивы и оборудование: исследуемый образец соли Мора, раствор Н2SO4, стандартный раствор КМnО4, мерная посуда, титровальная установка, промывалка
Инструктаж по технике безопасности.
Порядок выполнения работы:
I. МЕТОДИКА ВЫПОЛНЕНИЯ РАБОТЫ
1. Расчет величины навески
Исходные данные:
М[(NН4)2SО4 · FeSO4 · 6H2O] = 392,11 г/моль
М(1/5 КMnO4) = 1/5М(КMnO4) = 1/5 · 158,04 = 31,61 г/моль
V р-ра = 100 мл
С(1/5KMnO4) = 0,1 моль/л
С [(NН4)2SО4 · FeSO4 · 6H2O] = С(1/5KMnO4) = 0,1 моль/л
Расчет:
С[(NН4)2SО4 · FeSO4 · 6H2O] · М[(NН4)2SО4 · FeSO4 · 6H2O] ·V
 m[(NН4)2SО4 · FeSO4 · 6H2O] = =
m[(NН4)2SО4 · FeSO4 · 6H2O] = =
1000
 0,1· 392,11· 100
0,1· 392,11· 100
1000 = 3,92 г
2. Взвешенную навеску соли Мора растворите в мерной колбе вместимостью 100 мл, доведя объем до метки, тщательно перемешайте.
3. Бюретку заполните раствором КMnO4 до нулевого деления.
4. Пипетку ополосните раствором соли Мора и 10 мл ее перенесите в колбу для титрования.
5. Туда же прибавьте отмеренные мерным цилиндром 8-10 мл 2н. Н2SO4.
6. Не нагревая раствора, титруйте раствором перманганата калия до слабо - розового окрашивания.
7. Определение повторите трижды и для расчетов возьмите среднее значение.
8. Количественные данные определения концентрации раствора соли Мора
Объем КMnO4, израсходованного на 1-е титрование
Объем КMnO4, израсходованного на 2-е титрование
Объем КMnO4, израсходованного на 3-е титрование
Средний объем КMnO4
II. ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ
1-й способ.
1. Расчет результата определения концентрации раствора соли Мора:
С(1/5КMnO4)·V(КMnO4) = С(с. М)· V(с. М)
 С КMnO4) · V(КMnO4)
С КMnO4) · V(КMnO4)
С(с. М) = V(с. М)
2. Вычисление содержания железа в 100 мл раствора соли Мора:
C(с. М) · М[(NН4)2SО4 · FeSO4 · 6H2O] · 100
 m(Fe) = 1000
m(Fe) = 1000
2-й способ.
1. Вычисление титра перманганата калия по железу:
С(1/5КMnO4O4) · М(Fe2+)
 T(КMnO4/Fe) = 1000
T(КMnO4/Fe) = 1000
М(Fe2+) = 55,85 г/моль
2. Определение содержания железа в соли Мора:
m(Fe) = T(КMnO4/Fe) · V(КMnO4) · 10
Контрольные вопросы и задания:
1. На чем основан метод окисления - восстановления?
2. Какие вещества можно определять перманганатометрическим методом?
3. По какому веществу устанавливают титр и молярную концентрацию перманганата калия?
4. Расставить коэффициенты в уравнениях окислительно-восстановительных
реакций методом электронного баланса:
a) FeSO4 + KMnO4 + H2SO4 = Fe2 (SO4)3 + MnSO4 +K2SO4 + H2O
б) KJ + KMnO4 + H2SO4 = MnSO4 + J2 + K2SO4 + H2O
5. Какую навеску перманганата калия необходимо взять, чтобы приготовить 5 л раствора с титром 0,006321 г/мл?
ЛАБОРАТОРНАЯ РАБОТА № 17
Приготовление рабочего раствора нитрата серебра
и установление нормальной концентрации
Цель: научиться готовить рабочий раствор нитрата серебра и определять его нормальную концентрацию в растворе
Реактивы и оборудование: 0,005 н. р-р AgNO3, 5% р-р К2СrO4, измерительная посуда, весы аналитические, титровальная установка, промывалка
Инструктаж по технике безопасности.
Порядок выполнения работы:
В качестве стандартного раствора используется 0,05 н., титр и нормальную концентрацию которого устанавливают по раствору, индикатором является 5%-ный раствор К2СrO4. Определение хлорида натрия в растворе основано на уравнениях реакций:
NaCI + AgNO3 = AgCI↓ + NaNO
К2СrO4 + 2AgNO3 = Ag2СrO4↓ + 2KNO3
Образование AgCI – осадка белого цвета – происходит до тех пор, пока в растворе содержатся ионы CI-. По достижении точки эквивалентности добавление одной капли AgNO3 приводит к образованию красно-коричневого осадка Ag2СrO4. ТО, что осадок Ag2СrO4 образуется лишь после того как в реакцию вступили все ионы CI-, объясняется различием в растворимости этих осадков. Растворимость AgCI составляет 1,3 · 10-5 моль/л, Ag2СrO4 – 1,3 · 10-4 моль/л, т. е. хромат серебра обладает в десять раз большей растворимостью и, чтобы заметить его образование, нужно затратить некоторое избыточное количество раствора AgNO3.
Титрование по методу Мора проводят в нейтральной среде, так как в кислой среде хромат серебра растворяется, а в щелочной образуется бурый оксид серебра Ag2O, затрудняющий определение точки эквивалентности; в аммиачной среде и хлорид, и хромат серебра растворяются с образованием комплексного аммиаката серебра.
I. ПРИГОТОВЛЕНИЕ СТАНДАРТНОГО РАСТВОРА AgNO3.
1. Расчет величины навески
Исходные данные:
М(AgNO3) = 169,89 г/моль
V р-ра = 250 мл
С(AgNO3) = 0,05 моль/л
Расчет:
m (AgNO3) = 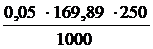 = 2,1236 г
= 2,1236 г
Нитрат серебра содержит примеси, поэтому готовят раствор приблизительной концентрации, а точные значения нормальной концентрации и титра устанавливают по раствору NaCI.
2. Навеску, близкую к рассчитанной, берут на технохимических весах.
3. Переносят в мерную колбу вместимостью 250 мл.
4. Растворяют в небольшом объеме дистиллированной воды, затем доводят объем раствора до метки дистиллированной воды и тщательно перемешивают.
5. Растворы AgNO3 разлагаются на свету, поэтому их хранят в темных склянках (или в обычной склянке, обернутой черной бумагой).
II. ПРИГОТОВЛЕНИЕ УСТАНОВОЧНОГО РАСТВОРА NaCI.
1. Расчет величины навески
Исходные данные:
М(NaCI) = 58,44 г/моль
V р-ра = 100 мл
С(NaCI) = 0,05 моль/л
Расчет:
m (NaCI) = 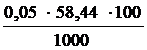 = 0,2922 г
= 0,2922 г
2. Взвешенную на аналитических весах навеску, близкую к рассчитанной, переносят в мерную колбу вместимостью 100 мл.
3. Растворяют, доводят объем раствора до метки дистиллированной водой и, закрыв пробкой, хорошо перемешивают.
III. УСТАНОВЛЕНИЕ НОРМАЛЬНОЙ КОНЦЕНТРАЦИИ РАСТВОРА
AgNO3
1. Бюретку заполните раствором AgNO3.
2. Пипетку ополосните раствором NaCI и 10 мл его перенесите в коническую колбу для титрования.
3. Добавьте в колбу 0,5 мл 5%-ного раствора К2СrO4 (раствор окрашивается в желтый цвет).
4. Из бюретки по каплям добавляйте раствор AgNO3, тщательно перемешивая раствор в колбе.
5. Титрование заканчивают, когда окраска раствора из желтой перейдет в красно-коричневую вследствие образования осадка хромата серебра.
6. Определение повторите трижды и для расчетов возьмите среднее значение.
7. Количественные данные определения концентрации раствора NaCI
Объем AgNO3, израсходованного на 1-е титрование
Объем AgNO3, израсходованного на 2-е титрование
Объем AgNO3, израсходованного на 3-е титрование
Средний объем AgNO3
IV. ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ
Вычисление нормальной концентрации AgNO3
С(AgNO3)·V(AgNO3) = С(NaCI)· V(NaCI)
С(NaCI) · V(NaCI)
 С(AgNO3) = V(AgNO3)
С(AgNO3) = V(AgNO3)
Контрольные вопросы и задания:
1. На чем основан метод осаждения?
2. Каким требованиям должна удовлетворять реакция осаждения, чтобы ее можно было использовать для количественных определений?
3. Что такое аргентометрия?
4. В чем состоит способ Мора?
5. Сколько граммов хлорида натрия содержится в растворе объемом 100 мл, если на титрование 10,00 мл его израсходавано 11,00 мл 0,05 н. AgNO3?
ЛАБОРАТОРНАЯ РАБОТА № 18
Определение содержание хлорида натрия в растворе
Цель: научиться определять содержание хлорида натрия в растворе
Реактивы и оборудование: стандартный раствор – 0,05 н. р-р AgNO3, установочное вещество – 0,05 н. NaCI; индикатор – 5%-ный К2СrO4
Инструктаж по технике безопасности.
Порядок выполнения работы
Приступая к аргентометрическому методу определения, следует помнить, что серебро – драгоценный металл, поэтому все использованные растворы нитрата серебра, а также осадки хлорида серебра нельзя сливать в раковину, а следует собирать в специально отведенные для этого склянки.
I. МЕТОДИКА ВЫПОЛНЕНИЯ РАБОТЫ
1. Получите от преподавателя раствор хлорида натрия в мерной колбе вместимостью 100мл.
2. Доводят объем его до метки дистиллированной водой.
3. Закройте пробкой и хорошо перемешайте.
4. Бюретку заполните раствором AgNO3.
5. Пипетку ополосните раствором NaCI и 10 мл его перенесите в коническую колбу для титрования.
6. Добавьте в колбу 0,5 мл 5%-ного раствора К2СrO4 (раствор окрашивается в желтый цвет).
7. Из бюретки по каплям добавляйте раствор AgNO3, тщательно перемешивая раствор в колбе.
8. Титрование заканчивают, когда окраска раствора из желтой перейдет в красно-коричневую вследствие образования осадка хромата серебра.
9. Определение повторите трижды и для расчетов возьмите среднее значение.
10. Количественные данные определения концентрации раствора NaCI
Объем AgNO3, израсходованного на 1-е титрование
Объем AgNO3, израсходованного на 2-е титрование
Объем AgNO3, израсходованного на 3-е титрование
Средний объем AgNO3
II. ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ
1. Вычисление титра раствора NaCI
Т (NaCI) = 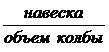 =
= 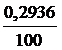 = 0,002936 г/мл
= 0,002936 г/мл
2. Вычисление нормальной концентрации раствора NaCI:
N (NaCI) = ![]()
3. Вычисление навески NaCI
1-й способ.
m (NaCI) = 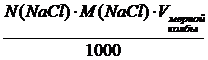
2-й способ. Вычислив Т (AgNO3 /NaCI):
Т (AgNO3 /NaCI) = 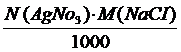
находим содержание NaCI в 100 мл раствора:
m (NaCI) = Т (AgNO3 /NaCI) · ![]() (AgNO3) · 10
(AgNO3) · 10
Контрольные вопросы и задания:
1. На чем основан метод осаждения?
2. Как рассчитать содержание поваренной соли (г) в заданном объеме раствора?
3. Каким требованиям должна удовлетворять реакция осаждения, чтобы ее можно было использовать для количественных определений?
4. Определите массу хлорида натрия, содержащегося в 1 л анализируемого раствора, если на титрование было израсходовано 12,5 мл раствора нитрата серебра с молярной концентрацией 0,096.
Библиографический список
1. Барсукова, химия. – М.: Высшая школа, 2006.
2. Воскресенский, задач и упражнений по аналитической химии. / , , . – М.: Просвещение, 1985.
3. Жванко, химия и технохимический контроль в общественном питании. / , , . – М.: Высшая школа, 1989.
4. www. *****
Приложение 1
Периодическая система химических элементов
Приложение 2
Таблица растворимости |
Условные обозначения:
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


Методические указания к выполнению лабораторных работ по дисциплине «Аналитическая химия» специальность: 260502 Технология продукции общественного питания» |
Рецензенты: , преподаватель дисциплины «Аналитическая химия» ФГОУ СПО «ОКТЭС»; , зав. ОПК, преподаватель высшей категории БОУ ОО СПО «ТЭК». |
Компьютерный набор: |
Ответственный за выпуск: |
Подписано в печать: 18.01.2013. Формат 60х90/16 |
Бумага офсетная. Печать RISO. |
Усл. печ. л. 4,2 Тираж 3 экз. |
Отпечатано в научно-методическом центре ФГОУ СПО «ОКТЭС»: г. Омска, ул.24-я Северная, 123Б |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |