В процессе изучения курса химии студент-заочник должен выполнить самостоятельно одну контрольную работу (в тетради 10-12 листов или на листах формата А4 в компьютерном оформлении). Решение задач и ответы на теоретические вопросы должны быть коротко, но четко обоснованы. При решении задач нужно приводить весь ход решения и математические преобразования.
Контрольная работа должна быть аккуратно оформлена, написана четко и ясно, и иметь поля для замечаний рецензента. Номера и условия задач необходимо переписывать в том порядке, в каком они указаны в задании. В начале работы следует указать учебный шифр студента, номер варианта и полный список номеров задач этого варианта. В конце работы следует дать список использованной литературы с указанием года издания.
Работа должна иметь подпись студента и дату.
Если контрольная работа не зачтена, ее следует выполнить повторно в соответствии с указаниями рецензента и представить вместе с не зачтенной работой. Исправления следует выполнять в конце работы, после рецензии, а не в тексте.
Контрольная работа, выполненная не по своему варианту, преподавателем не рецензируется и не засчитывается как сданная.
Каждый студент выполняет вариант контрольных заданий, обозначенный двумя последними цифрами номера студенческого билета (86594, две последние цифры 94, им соответствует вариант контрольного задания 94)
Графики и рисунки должны быть выполнены аккуратно с использованием чертёжных инструментов или компьютерной технологии.
К защите допускаются правильно оформленные работы, с достаточно полным раскрытием темы. Студент должен во время защиты дать пояснения по всему материалу контрольной работы.
Контрольная работа №1. Темы работы:
· строение атома,
· химическая связь и строение молекул,
· химическая термодинамика,
· химическая кинетика,
· химическое равновесие,
· гидролиз солей,
· жесткость воды и методы ее устранения,
· способы выражения концентраций,
· произведение растворимости,
· электродные потенциалы и электродвижущие силы,
· электролиз,
· коррозия металлов,
· полимеры.
Краткое содержание: определение типа химической связи, построение атомных электронных орбиталей, расчет энтальпии, энтропии и свободной энергии Гиббса химического процесса и определение направления протекания химической реакции, расчет энергии активации и температурного коэффициента по правилу Вант-Гоффа, определение эквивалентов различных веществ, расчет произведения растворимости солей и растворимости различных ионов, составление схем гальванических элементов и расчет электродных потенциалов с поправкой на концентрацию по уравнению Нернста, составление электронных уравнений катодного и анодного процессов коррозии различных металлов в разных средах, подбор защитных металлических покрытий, расчет массы и объема продуктов электролиза, определение степени полимеризации.
1.7 Самостоятельная работа
Разделы и темы для самостоятельного изучения | Виды и содержание самостоятельной работы | Коли-чество часов |
1. Раздел «Строение вещества» 5.2. Химия металлов Зависимость свойств металлов от их положения в периодической системе . Интерметаллические соединения и твердые растворы металлов. Основные методы получения металлов. Физико - химические процессы при сварке и пайке металлов, d - элементы IV - VII групп. Химия элементов семейства железа, их химические соединения. Химия платиновых металлов. Химия металлов подгрупп меди и цинка.[2, 341-370; 3, 275-302] 5.3. Химия неметаллических элементов Неметаллы и полуметаллы. Зависимость свойств неметаллов от их положения в периодической системе . Бор и его соединения. Элементы VI и VII групп и их соединения.[2, 382-410; 3, 325-341] 5.4. Неорганическая химия элементов IV группы. Химия полупроводников Углерод и его аллотропные формы. Монооксид и диоксид углерода. Карбонаты. Силикаты. Стекла. Ситаллы. Фарфор, техническая и строительная керамика. Сверхпроводящие материалы. Элементные полупроводники. Полупроводниковые соединения. Физико - химические способы обработки полупроводников.[4, 254-272] 5.10. Ядерная химия. Радиохимия Состав атомных ядер. Изотопы. Радиоактивность. Радиоактивные ряды. Химическое воздействие ионизирующих излучений на вещества. Использование радиоактивных изотопов. Искусственная радиоактивность. Ядерные реакции. Ядерная энергетика. Химия тория, урана, плутония и других радиоактивных элементов и материалов.[4,501-511; 2, 516-530] | Проработка учебного материала по учебной и научной литературе, работа с вопросами для самопроверки. Обсуждение проблемных вопросов с преподавателями в рамках индивидуальных консультаций. Выполнение тестов и заданий, размещенных в системе КОСМОС для самопроверки. | 19 |
2. Раздел «Растворы» 5.1.Свойства растворов. растворимость, буферные растворы [ 1,; 2, ].Равновесие в гетерогенных системах. Фазовое равновесие и понятие фаз. Экстракция. Сорбция. Поверхностные вещества. Адсорбция. Адсорбционное равновесие [ 1,; 2, ].Гетерогенные дисперсные системы. Коллоидные системы и их получение. Строение коллоидных частиц. Агрегативная и кинетическая устойчивость систем. Коагуляция. Эмульсии. Суспензии [ 1,; 2, ]. 5.7. Химия воды Строение молекул и свойства воды. Диаграмма состояния воды. Диаграмма плавкости систем типа вода - соль. Кристаллизация воды и водных растворов в различных условиях. Химические свойства воды. Взаимодействие воды с простыми веществами и химическими соединениями. Природные воды и их состав. Жесткость воды. Коллоидные вещества природных вод и их удаление. умягчение и обессоливание воды. Методы осаждения, ионного обмена и мембранные методы.[1, 267-273; 2, 490-495; 6, схема 8] | Проработка учебного материала по учебной и научной литературе, работа с вопросами для самопроверки. Обсуждение проблемных вопросов с преподавателями в рамках индивидуальных консультаций. Выполнение тестов и заданий, размещенных в системе КОСМОС для самопроверки. | 19 |
3. Раздел «Полимеры» 5.5. Химия вяжущих веществ Определение и классификация вяжущих веществ и их свойства. Воздушные и гидравлические вяжущие вещества. Известковые и гипсовые вяжущие вещества. Портландцемент. Процессы схватывания и твердения. Бетон. Коррозия бетонов и методы борьбы с ней.[3, 65-90] 5.6. Элементы органической химии. Органические полимеры материалы Строение, классификация и свойства органических соединений. Углеводороды и их производные. Кремнийорганические соединения.[1, 179-194; 2, 419-430] Состав и свойства органического топлива. Термохимия топлива. Твердое топливо и его переработка. Жидкое и газообразное топливо. Понятие о физико - химических процесса горения топлива. Химия смазочно - охлаждающих средств, применяемых при обработке металлов и сплавов. Физико - химические свойства и механизм воздействия рабочих сред гидравлических систем. Химия полимеров. Метод получения полимеров. Зависимость свойств полимеров от состава и структуры. Химия полимерных конструкционных материалов. Химия композиционных материалов. Полимерные покрытия и клеи. Химия полимерных диэлектриков. Химия полимерных проводников.[1, 195-211; 2, 450-461; 6, модель IX, схема 10] | Проработка учебного материала по учебной и научной литературе, работа с вопросами для самопроверки. Обсуждение проблемных вопросов с преподавателями в рамках индивидуальных консультаций. Выполнение тестов и заданий, размещенных в системе КОСМОС для самопроверки. | 19 |
4. Раздел «Электрохимические процессы» 5.8. Электрохимические процессы в энергетике и машиностроении Химические источники тока. Электрохимические генераторы. Электрохимические преобразователи (хемотроны). Электрохимическкя обработка металлов и сплавов. Получение и свойства гальванопокрытий.[1, 106-213; 2, 290-298] | Проработка учебного материала по учебной и научной литературе, работа с вопросами для самопроверки. Обсуждение проблемных вопросов с преподавателями в рамках индивидуальных консультаций. Выполнение тестов и заданий, размещенных в системе КОСМОС для самопроверки. | 19 |
5. Раздел «Химия и охрана окружающей среды» 5.9. Химия и охрана окружающей среды Технический прогресс и экологические проблемы. Роль химии в решении экологических проблем. Продукты горения топлива и защита воздушного бассейна от загрязнения. Метод малоотходной технологии. Водородная энергетика. Получение и использование водорода.[1, 241-251; 2, 284-290] Охрана водного бассейна. Характеристика сточных вод. Методы очистки сточных вод. Методы замкнутого водоворота.[1, 265-278] | Проработка учебного материала по учебной и научной литературе, работа с вопросами для самопроверки. Обсуждение проблемных вопросов с преподавателями в рамках индивидуальных консультаций. Выполнение тестов и заданий, размещенных в системе КОСМОС для самопроверки. | 18 |
Результаты самостоятельной работы контролируются при аттестации студента при защите контрольной работы.
1.8 Учебно-методическое обеспечение дисциплины
Основная литература
1. Глинка, химия: Учебник/ . -17-е изд. - М.: Издательство Юрайт, 2010.
2. Коровин, химия: Учебник/ . -11-е изд. - М.: Высшая школа, 2009.
3. Ахметов, и неорганическая химия: Учебник/ . - 4-е изд.-М.: Высшая школа, 2001.
4. Угай, и неорганическая химия: Учебник/ . -2-е изд. - М.: Высшая школа, 2000.
5. Зубрев, химия на железнодорожном транспорте: Учебное пособие/ . -2-е изд. - М.: Желдориздат, 2002.
6. Заглядимова, в моделях, схемах и таблицах: Учебное пособие/ . – М.: МИИТ, 2011.
Дополнительная литература
1. Ахметов, и семинарские занятия по общей и неорганической химии: Учебное пособие/ , , . -4-е изд.-М.: Высшая школа, 2002.
2. Физическая химия. В 2 кн. Кн. 1. Строение вещества. Термодинамика: Учебник для вузов/ , , и др.; Под ред. . -3-е изд. - М.: Высшая школа, 2001.
3. Физическая химия. В 2 кн. Кн.2. Электрохимия. Химическая кинетика и катализ: Учебник для вузов/ , , и др.; Под ред. . -3-е изд. - М.: Высшая школа, 2001.
4. Задачи и упражнения по общей химии: Учебное пособие/ Под ред. . -4-е изд. - М.: Высшая школа, 2008.
5. Пузаков, задач и упражнений по общей химии: Учебное пособие/ , , . - М.: Высшая школа, 2004.
1. 9 Материально-техническое и информационное обеспечение дисциплины
В учебном процессе для освоения дисциплины используются следующие технические средства:
· химическая лаборатория, химические реактивы;
· компьютерное и мультимедийное оборудование (на лекциях, для самоконтроля знаний студентов, для обеспечения студентов методическими рекомендациями в электронной форме);
· приборы и оборудование учебного назначения (при выполнении лабораторных работ);
· пакет прикладных обучающих программ (для самоподготовки и самотестирования);
· электронная библиотека курса (в системе КОСМОС - электронные лекции, тесты для самопроверки, тесты для сдачи зачёта).
КОНСПЕКТ ЛЕКЦИЙ ПО ДИСЦИПЛИНЕ «ХИМИЯ»
ВВЕДЕНИЕ
Основной целью изучения курса Химии в инженерном вузе является умение увидеть в конкретной производственной ситуации химическую проблему и квалифицированно разрешить ее. Выполнение такой задачи требует многостороннего, т. е. системного изучения вещества – его природы и свойств, взаимодействия с другими веществами, практического использования. Именно поэтому общая структура курса Химии представлена следующими тремя взаимосвязанными блоками:
1. Строение веществ.
2. Поведение веществ.
3. Инженерная химия (использование веществ).
Учитывая дефицит времени как аудиторных лекционных часов (4 часа), так и недостаток времени у студентов, обучающихся без отрыва от производства, Вам предлагается способ интенсивного изучения предмета с использованием пособия модульного типа «Химия в моделях, схемах, таблицах», где курс в целом и его отдельные блоки представлены в виде графических моделей и конспект-схем.
Если на конспект-схемах представлен конкретный материал темы, то структурированные модели дают его обобщение, т. е. связи между основными теоретическими понятиями курса, разделов.
Рассмотрим последовательно модели и конспект-схемы.
Графических моделей всего 10, из них: одна представляет курс Химии в целом; три – модели блоков; шесть – модели подблоков (две модели на каждый блок).
Каждая модель начинается с четкой постановки цели изучения конкретного блока или подблока. А сама структура модели показывает путь достижения этой цели. Общий вид модели показан на рис. 1.1. Как видите, модель блока состоит из двух ромбов – верхнего (предмет изучения) и нижнего (результат), которые соединены между собой внутренним, а иногда и внешним циклами.
Следует отметить, что все модели между собой взаимосвязаны. Например, первые два блока характеризуют теоретическое содержание курса, третий - его практическое приложение; одновременно третий блок, например, отражает в своих подблоках два различных аспекта прикладной химии - использование вещества (конструкционные и др. материалы) и энергии (электрохимические процессы).
Общий вид графической модели
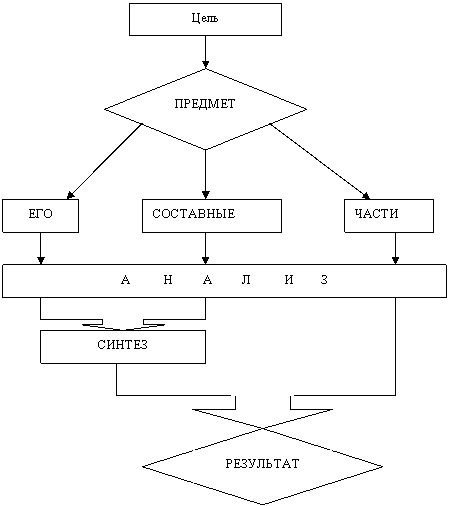
Рис. 1.1
Чтобы увидеть эту диалектичность в моделях, необходимо научиться использовать определенные мыслительные приемы, такие как:
- анализ (деление на элементы),
- сравнение (сходство и различие),
- классификация (выделение основных признаков),
- следствие (логический вывод) и др.
Так как графические модели содержат не конкретный материал, а его обобщение, ориентировку в нём, то одной модели может соответствовать несколько конспект-схем (например, модель VI содержит материал 3-х схем). Конкретный материал всего курса Общей химии представлен концентрированно на 12 конспект-схемах (им соответствуют 6 моделей подблоков), что позволяет успешно и достаточно быстро его усвоить. Каждая схема начинается с постановки вопроса, отражающего суть проблемы данной темы. Изучив этот материал с помощью конспект-схемы (и соответствующей модели), студенты должны уметь четко ответить на поставленный вопрос и тем самым разрешить выдвинутую учебную или инженерную проблему.
Предметом изучения курса химии является вещество в реакции, прогнозирование его свойств. Для достижения этой цели необходимо знание количественных характеристик этих свойств и практического применения веществ, обладающих данными свойствами. При этом следует иметь в виду, что количественные показатели в целом должны отражать три аспекта изучения вещества: структурный, термодинамический, кинетический. Табл. 1 в III части пособия наглядно демонстрирует это, указывая для каждого из аспектов:
- основные количественные показатели и законы;
- свойства вещества в реакции;
- применение вещества и энергии.
Итак, предлагаемый структурный способ компактного изображения учебного материала делает его наглядным и доступным для изучения каждым студентом. Однако использование данного пособия не исключает индивидуальной работы с литературой, а лишь направляет её, облегчая поиски наиболее важной информации в учебниках.
СТРУКТУРА КУРСА ОБЩЕЙ ХИМИИ
Структура курса Общей химии представлена в виде системы трех основных блоков (рис. 1.2):
I. Строение веществ
II. Поведение веществ
III. Инженерная химия
В структурном представлении учебного материала очень важным является понятие системы как множества взаимосвязанных между собой элементов. С этой точки зрения мы и предлагаем подходить к изучению курса Химии.
Первый блок рассматривает вещество (свойства атома, свойства веществ) как систему в статичном, дореакционном состоянии на основе его внутренней структуры (строение атома, периодичность, химическая связь).
Но поведение вещества в каждой конкретной ситуации зависит не только от его собственных свойств, но и от реагирующих с ним веществ той же химической системы. Иными словами, вещество познается во взаимодействии, т. е. его внутренняя структура (I блок) проявляется в химических реакциях (II блок). В этом смысл II блока, который рассматривает основные закономерности протекания химических реакций (термодинамические и кинетические) и влияние реакционной среды (растворы), т. е. поведение веществ в процессе.
Наиболее важные инженерные проблемы курса Химии составляют содержание III блока. Материал этого блока (конструкционные и др. материалы, электрохимические процессы) следует изучать на основе первых двух, т е. опираясь на внутреннее строение вещества и используя общие закономерности протекания химических процессов.
Такое системное изучение курса является наиболее целесообразным, показывая как предмет в целом, так и место каждого, раздела в нем.
На модели I курс «Общая химия» представлен через структурные элементы учебой деятельности: цель - предмет - средства реализации (анализ, синтез) - результат (рис. 1.3).
СТРУКТУРА КУРСА ОБЩЕЙ ХИМИИ
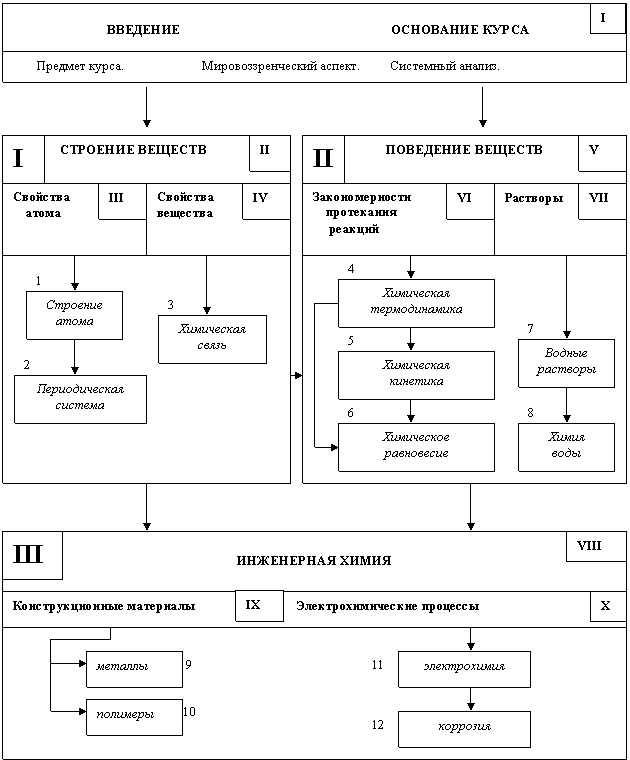
ВВЕДЕНИЕ В КУРС ОБЩЕЙ ХИМИИ (модель I)
Рис. 1.2
Рис. 1.2
Основной предмет изучения курса Химии - вещество в реакции - рассматривается с точки зрения его строения, поведения и применения.
Строение веществ определяется их положением в периодической системе и энергией химических связей Есв.
Поведение же веществ в реакции - это, прежде всего возможность протекания данной реакции, т. е. направление процесса (![]() G) и его скорость (V), характеризуемая энергией активации (Еа).
G) и его скорость (V), характеризуемая энергией активации (Еа).
В сочетании со строением поведение веществ дает основные закономерности химических реакций – структурные, термодинамические, кинетические.
Применяя выделенные закономерности к изучению свойств различных материалов, энергетике (химические источники тока) и коррозии металлов, получаем общий курс химии в целом.
Модель I
ОБЩАЯ ХИМИЯ
Цель: Прогнозирование поведения вещества в реакции с целью практического использования
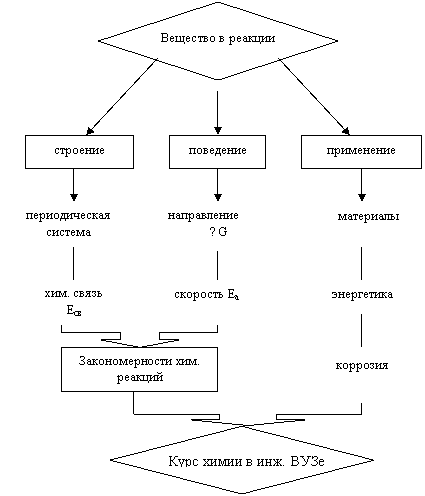
Рис. 1.3

СТРОЕНИЕ ВЕЩЕСТВ
ВВЕДЕНИЕ В БЛОК «СТРОЕНИЕ ВЕЩЕСТВ»
(модель II)
Предметом изучения блока «Строение веществ» является вещество, точнее свойства вещества как отражение его строения на разных уровнях: электронном (Э), атомном (А), молекулярном (М) и кристаллическом (К) (рис. 1.4).
СТРОЕНИЕ ВЕЩЕСТВ
I блок Модель II
Цель: Прогнозирование свойств веществ на основе структуры
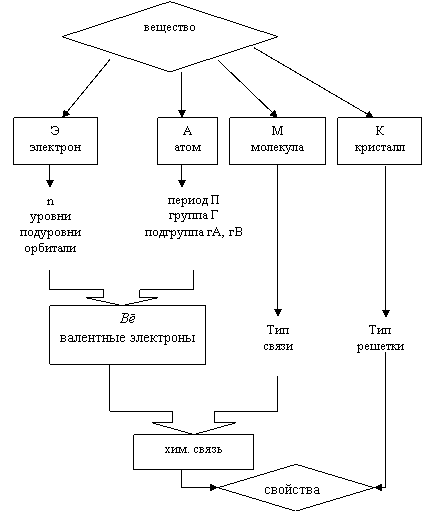 |
Рис. 1.4
Хотя свойства вещества в целом определяются тремя уровнями: А, М и К, тем не менее основное внимание уделим электронному строению атома как ответственному за химизм (в процессе химического превращении ядро неизменно).
Главным носителем химических свойств веществ являются наиболее подвижные валентные электроны (Вē), структура которых определяется положением элемента в периодической системе (периоде, группе, подгруппе), отражающей сложную электронную структуру атома - уровни, подуровни, орбитали.
На основе знания структуры Вē, типа связи и типа решетки можно прогнозировать физико-химические свойства веществ (реакционная способность, металличностъ, неметалличность, растворимость, электрические, механические и др. свойства).

I блок включает два подблока – «Свойства атома» (модель III) и «Свойства вещества» (модель IV).
СВОЙСТВА АТОМА (модель III)
Свойства атома, как известно, определяются местонахождением его в периодической системе, которая и является предметом изучения данного подблока (рис. 1.5). Место же каждого атома в периоде, группе, подгруппе, в свою очередь, определяется его внутренним строением (ядро, электроны, их взаимосвязь - радиус). Так как электрон - «волна» (не только частица), атом обладает сложной структурой, состоящей из уровней, подуровней, орбиталей. Поэтому понятие орбитали (s, p, d, f) является основным (исходным) для понимания энергетической структуры и свойств атома.
Внутренний цикл модели раскрывает структуру валентных электронов Вē, ответственных за химические свойства.
Номер периода показывает количество электронных уровней и подуровней, а также номер внешнего уровня (n). Номер группы дает общее (суммарное) число валентных электронов (∑Вē). В группе А - валентными электронами заполняется только внешний n уровень (s-и p-электроны),а в группе В - внешний nS и предвнешний (n-1)d, иногда (n-2)f. В связи с этим группу А составляют s и р электронные семейства, а группу В - соответственно d и f. Так определяется структура Вē.
Пользуясь правилом Хунда, можно определить валентность (по числу неспаренных электронов). Эти знания дают возможность прогнозирования химических свойств атомов - металличности (Ме) и неметалличности (нМе).
Однако для количественной оценки этих свойств (внешний цикл) необходимо использовать такие характеристики атомов как энергия ионизации (J) и электроотрицательность (ЭО) зависящие от порядкового номера (Z) и радиуса атома (r). При этом не забывайте периодический закон, согласно которому химические свойства являются функцией структуры внешних электронов (n слоя) и, в конечном счете, заряда ядра атома Z.
СВОЙСТВА АТОМА
I подблок Модель III
Цель: Прогнозирование свойств атома по положению в Периодической системе
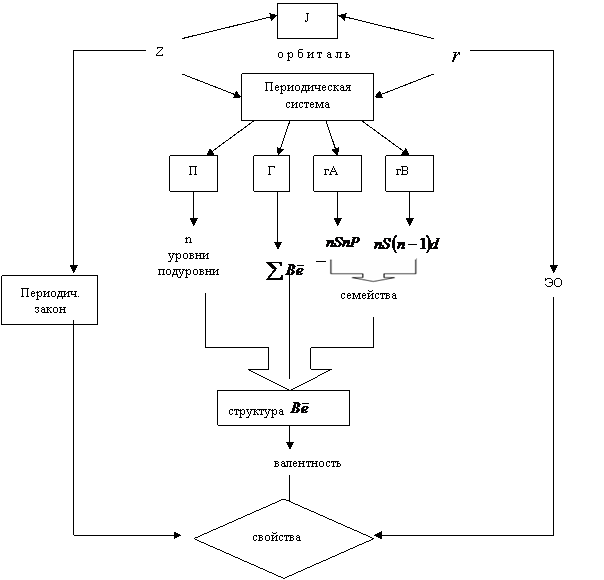 |
Рис. 1.5
 Вывод Свойства веществ на атомном уровне прогнозируются на основе структуры Вē с учетом периодического закона, а количественно измеряются величинами J (Ме) и ЭО (нМе), а также Z и r.
Вывод Свойства веществ на атомном уровне прогнозируются на основе структуры Вē с учетом периодического закона, а количественно измеряются величинами J (Ме) и ЭО (нМе), а также Z и r.
СВОЙСТВА ВЕЩЕСТВА (модель IV)
Так как возможность протекания реакции, зависит от перераспределения связей между атомами в молекуле, химическую связь можно считать ответственной за реакционную способность веществ и все его физико-химические свойства. Поэтому тип связи, определяемый свойствами соединяющихся атомов (∆ЭО), является основным предметом изучения данной темы (рис. 1.6). Различают ковалентную (нМе-нМе), ионную (Ме-нМе) и металлическую (Ме-Ме) химические связи.
В основе наиболее прочной ковалентной связи (К), реализуемой через общие электронные пары, лежит ее жесткая пространственная направленность – геометрическая форма (следствие формы перекрывающихся орбиталей).
Взаимодействие ионов в случае ионной связи (И) происходит за счет электростатического притяжения разноименных зарядов, в результате чего образуется кристалл.
Металлическая же связь (Ме) осуществляется делокализованными электронами (ē), что приводит к появлению особых специфических свойств металла (электропроводимость, теплопроводность, пластичность и др.).
Кроме основных химических сил в конденсированном состоянии вещества возможны дополнительные межмолекулярные связи – силы Ван-дер-Ваальса и водородные связи, изменяющие свойства веществ (tкип, tпл, теплоемкость и др.).
По типу связи можно прогнозировать и агрегатное состояние веществ. Если ионные и металлические связи дают только кристаллические вещества, то ковалентные – и газы, и кристаллы. А межмолекулярные связи дают не только жидкость, но и молекулярные кристаллы. Отметим, что любой кристалл характеризуется определенным значением координационного числа (К. Ч.), от которого зависят многие его свойства, особенно механические. Таким образом, все рассмотренное выше составляет внутренний цикл модели.
Внешний же цикл характеризует количественно свойства связи, которые, в конечном счете, определяют свойства вещества. Самой главной характеристикой связи является ее энергия (Есв), зависящая от длины (rсв) и числа связей.
Важнейшей характеристикой связи (кроме Есв, rсв) является и величина электроотрицательности ЭО. Разность ЭО взаимодействующих атомов определяет тип связи и ее ионность (в ковалентных молекулах – полярность). С ионностью связаны, прежде всего, электрические свойства веществ, их растворимость и, конечно, реакционная способность.
СВОЙСТВА ВЕЩЕСТВА
1,2 подблок Модель IV
Цель: Прогнозирование свойств вещества на основе типа связи
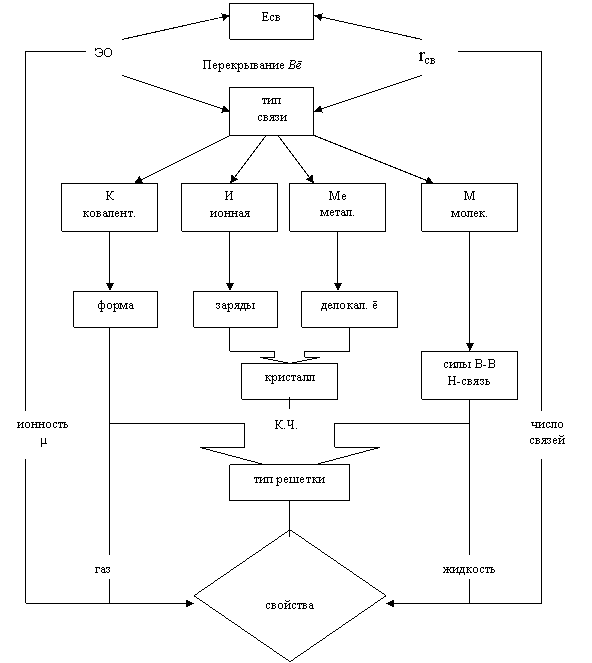 |
Рис. 1.6

Вывод Физико-химические свойства веществ (реакционная способность, растворимость, механические, электрические) прогнозируются на основе типа химической связи (Есв, rсв, ЭО), типа кристаллической решетки (К. Ч.) и агрегатного состояния веществ.
ПОВЕДЕНИЕ ВЕЩЕСТВ
ВВЕДЕНИЕ В БЛОК «ПОВЕДЕНИЕ ВЕЩЕСТВ»
(модель V)
Основным предметом изучения II блока является химическая реакция, к общим свойствам которой относятся: направление процесса, его скорость, выход продукта и определенная среда протекания (рис.2.1).
ПОВЕДЕНИЕ ВЕЩЕСТВ
II блок Модель V
Цель: Реализация химического процесса на основе его общих свойств
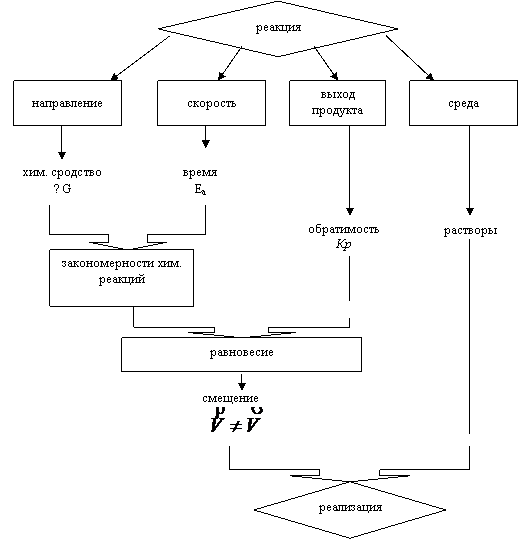 |
Рис. 2.1
Химическое сродство взаимодействующих веществ друг к другу, определяемое величиной энергии Гиббса (∆G), и протекание реакции во времени, связанное с энергией активации (Еа), составляют соответственно термодинамические и кинетические закономерности протекании реакций.
Химически обратимые реакции (Кр), подчиняющиеся общим законам термодинамики и кинетики, характеризуются состоянием химического равновесия. В результате смещения в ту или иную сторону (V1≠V2) под действием внешних условий (С, Т, Р и др.) в определенной среде взаимодействия (растворы) получаем реальный процесс (практическая реализация реакции).
 Вывод Для реализации химического процесса необходимо знание внутренней движущей силы процесса – его химического сродства (∆G), внешних условий его протекания (С, Т, Р, К) и направления смещения равновесия (Кр) с учетом среды реакции (раствора).
Вывод Для реализации химического процесса необходимо знание внутренней движущей силы процесса – его химического сродства (∆G), внешних условий его протекания (С, Т, Р, К) и направления смещения равновесия (Кр) с учетом среды реакции (раствора).
Данный блок состоит из двух подблоков – «Закономерности протекания реакций» (модель VI) и «Растворы» (модель VII).
ЗАКОНОМЕРНОСТИ ПРОТЕКАНИЯ РЕАКЦИЙ (модель VI)
Для управления процессом необходимо, прежде всего, вскрыть термодинамические и кинетические законы протекания реакции. Эти законы и составляют основной предмет изучения данного раздела (рис. 2.2).
Поскольку термодинамические величины характеризуют реакцию при заданных условиях (Р, Т=const), являясь функцией состояния системы, не зависящей от промежуточных стадий, а кинетика, напротив, изучает сам механизм (стадии) реакции в реальных изменяющихся условиях, то термодинамический подход определяет теоретическую возможность процесса (по ΔG0), а кинетический – практическую осуществимость его (на основе Еа).
Сравнивая эти два подхода, следует иметь в виду, что универсальный критерий осуществимости процесса ΔG0 зависит преимущественно от внутренних факторов – энтальпийного (ΔН0) и энтропийного (ΔS0), а реальное протекание его – от внешних условий (С, Т, Р, Кат). Но на скорость химического процесса влияет и природа реагирующих веществ, так как реакция идет только между активными молекулами.
Чтобы целенаправленно управлять процессом, необходимо уметь подбирать оптимальные условия смещения его равновесия с помощью принципа Ле-Шателье и величины константы равновесия Кр. Таким образом, мы проанализировали внутренний цикл – использование общих законов протекания реакций для управления ими. Обратите внимание на изменение скорости химических реакций и смещении химического равновесия основаны методы управления технологическими процессами.
ЗАКОНОМЕРНОСТИ ПРОТЕКАНИЯ РЕАКЦИЙ
II. 1 подблок Модель VI
Цель: Управление процессом на основе общих закономерностей его протекания
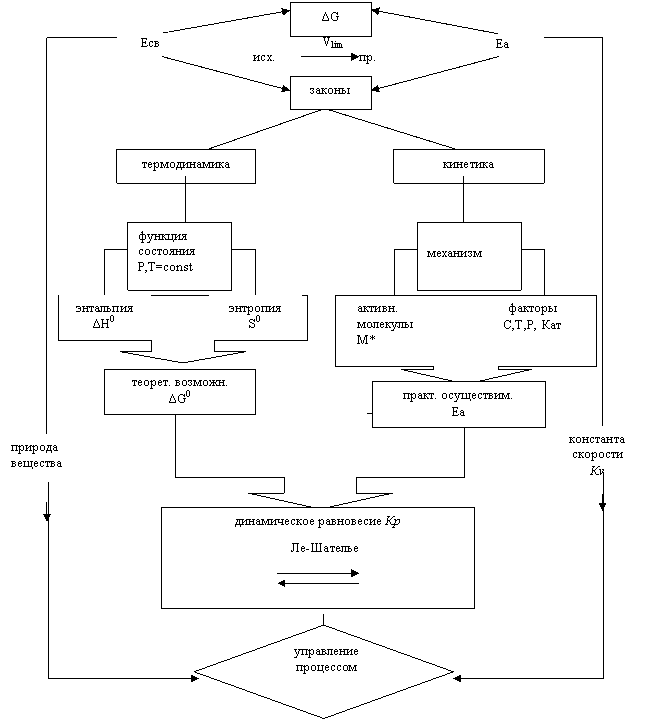 |
Рис. 2.2
Обращаясь к количественной стороне превращения исходных веществ в продукты (исх.®пр.), следует выделить в качестве главной величины энергию Гиббса (ΔG), затем ее химическую часть – энергию активации (Еа), ответственную за скорость (Кv), и наконец, энергию связи (Есв) как исходную характеристику, отражающую природу реагирующих веществ.

Вывод Управление процессом следует осуществлять на основе знаний законов термодинамики (закон Гесса, ΔG0=ΔН0-ТΔS0), кинетики (закон действия масс, закон Аррениуса, правило Вант-Гоффа), принципа Ле-Шателье (Кр) с учетом структурного подхода (Есв).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



