43. Во сколько раз изменится скорость реакции 2А+В→А2В, если концентрацию вещества А увеличить в 2 раза, а концентрацию вещества В уменьшить в 2 раза?
44. Во сколько раз следует увеличить концентрацию вещества В2 в системе 2А2(г.)+В2(г.) →2А2В(г.), чтобы при уменьшении концентрации вещества А в 4 раза скорость реакции не изменилась?
45. В 2 сосуда одной и той же вместимости помещены: в первый – 1 моль газа А и 2 моля газа В, во второй – 2 моля газа А и 1 моль газа В при одинаковой температуре. Будет ли различаться скорость реакции между газами А и В в этих сосудах, если скорость реакции выражается: а) уравнением v1=k1[А][В]; б) уравнением v2=k2[А]2[В] ?
46. Через некоторое время после начала реакции 3A+B→2C+D концентрации веществ составляли: [A]=0,03 моль/л; [B]=0,01 моль/л; [C]=0,008 моль/л. Каковы исходные концентрации веществ А и В?
47. Как изменится скорость реакции 2NO(г.)+О2(г) →2NO(г.), если: а) увеличить давление в системе в 3 раза; б) уменьшить объём системы в 3 раза; в) повысить концентрацию NO в 3 раза?
48. Две реакции протекают при 25 0С с одинаковой скоростью. Температурный коэффициент скорости первой реакции равен 2, второй – 2,5. Найти отношение скоростей этих реакций при 95 0С.
49. Чему равен температурный коэффициент скорости реакции, если при увеличении температуры на 30 градусов скорость реакции увеличивается в 15,6 раза?
50. Температурный коэффициент скорости некоторой реакции равен 2,3. Во сколько раз увеличится скорость реакции при повышении температуры на 25 градусов.
51. При 150 0С некоторая реакция заканчивается за 16 мин. Принимая температурный коэффициент скорости реакции равным 2,5, рассчитать, через какое время закончится эта реакция, если её проводить при 80 0С;
52. Во сколько раз увеличится скорость реакции, протекающей при 298 К, если её энергию активации уменьшить на 4 кДж/моль?
53. Чему равна энергия активации реакции, если при увеличении температуры от 290 до 300 К скорость её увеличится в 2 раза?
54. Каково значение энергии активации реакции, скорость которой про 300 К в 10 раз больше, чем при 280 К?
55. Энергия активации реакции равна 10 кДж/моль. Во сколько раз изменится скорость реакции при повышении температуры от 27 до 37 0С?
56. Рассчитайте энергию активации реакции, если при увеличении температуры от 500 до 1000К константа скорости химической реакции возросла в 105 раз.
57. На основе молекулярной структуры оцените энергию активации реакции
CH4(г) + H2O(г) = CO(г) + 3H2(г)
Предложите оптимальный режим ее проведения.
58. Реакция идет по уравнению
N2 + 3Н2 = 2NH3
Концентрация участвующих в ней веществ были (моль/л): [N2] =0,80; [Н2] =1,5; [NН3] =0,1. Вычислить концентрации веществ в момент, когда концентрация N2 стала 0,50 моль/л.
59. Окисление аммиака идет по уравнению
4NH3 + 5O2 + 4NO + 6H2O
Через некоторое время после начала реакции концентрации участвующих в ней веществ были (моль/л): [NН3] =0,009; [О2] =0,02; [NО] =0,003. Вычислить: а) концентрацию водяного пара в этот момент; б) исходную концентрацию аммиака и кислорода.
60. Реакция идет по уравнению
Na2S2O3 + H2SO4 = Na2SO4 + H2SO3 + S
Как изменится скорость реакции вследствие разбавления реагирующей смеси в 2 раза?
ХИМИЧЕСКОЕ РАВНОВЕСИЕ
Все химические процессы делятся на два типа: обратимые и необратимые.
Обратимые реакции в одних и тех же условиях идут в двух противоположных направлениях (![]() ), а необратимые – в одном (
), а необратимые – в одном (![]() ). К необратимым относятся реакции, сопровождающиеся выделением газа, образованием осадка, или малодиссоциирующих веществ (например, воды), устойчивых комплексов, а также очень большим выделением тепла.
). К необратимым относятся реакции, сопровождающиеся выделением газа, образованием осадка, или малодиссоциирующих веществ (например, воды), устойчивых комплексов, а также очень большим выделением тепла.
Большинство реакций являются обратимыми. Например,
H2(г) + I2 (г) | (9) |
Реакцию, идущую слева направо (в данном случае – образование HI), принято считать прямой, а реакцию, идущую справа налево (в данном случае – разложение HI) – обратной.
 Реакция смеси эквимолярных количеств (1:1) газообразных водорода и иода при нагревании в закрытом сосуде до 3560С идет до тех пор, пока не образуется 80% того количества иодистого водорода, которое должно образоваться по уравнению (9). Остальные 20% остаются в виде H2 и I2 независимо от длительности нагревания. В первый момент времени скорость прямой реакции vпр. будет наибольшей, скорость обратной vобр. – равна нулю (рис.2). С течением времени концентрации H2 и I2 уменьшаются, концентрация HI увеличивается, происходит уменьшение скорости прямой реакции и увеличение скорости обратной реакции. Наконец, наступает момент, когда скорость прямой и обратной реакций становятся равными. С этого времени концентрации всех веществ перестают изменяться, скорость образования HI равна скорости его разложения. Наступает химическое равновесие.
Реакция смеси эквимолярных количеств (1:1) газообразных водорода и иода при нагревании в закрытом сосуде до 3560С идет до тех пор, пока не образуется 80% того количества иодистого водорода, которое должно образоваться по уравнению (9). Остальные 20% остаются в виде H2 и I2 независимо от длительности нагревания. В первый момент времени скорость прямой реакции vпр. будет наибольшей, скорость обратной vобр. – равна нулю (рис.2). С течением времени концентрации H2 и I2 уменьшаются, концентрация HI увеличивается, происходит уменьшение скорости прямой реакции и увеличение скорости обратной реакции. Наконец, наступает момент, когда скорость прямой и обратной реакций становятся равными. С этого времени концентрации всех веществ перестают изменяться, скорость образования HI равна скорости его разложения. Наступает химическое равновесие.
Таким образом, с точки зрения химической кинетики, химическое равновесие – это такое состояние обратимой реакции, при котором скорости прямой и обратной реакции равны: vпр = vобр
Концентрации реагирующих веществ, которые устанавливаются при химическом равновесии, называются равновесными. Соотношение между равновесными концентрациями не зависит от того, какие вещества берут в качестве исходных (например, H2 и I2 или HI), то есть к состоянию равновесия можно подойти с обеих сторон (рис.2)
КОНСТАНТА ХИМИЧЕСКОГО РАВНОВЕСИЯ
Выведем константу равновесия для обратимых химических реакций (в общем виде)
aA + bB = сС + dD. | (10) |
Применим закон действия масс и запишем выражения скорости прямой и обратной реакций:
· скорость прямой реакции: vпр. = k1[A]a[B]b (11)
· скорость обратной реакции: vобр. = k2[C]c[D]d (12)
· в состоянии равновесия: vпр. = vобр. , т. е. k1[A]a[B] b= k2[C]c[D]d (13)
Переносим постоянные величины (константы скорости) в левую часть равенства, а переменные (концентрации) – в правую часть равенства, т. е. записываем данное равенство в виде пропорции:
| (11) |
Так как величины k1 и k2 в определенных условиях постоянны, то и отношение их тоже будет постоянной величиной для данной системы. Её обозначают К и называют константой равновесия.
| (12) |
В выражение константы равновесия входят равновесные концентрации веществ, взятые в степенях, равных коэффициентам перед веществом в уравнении реакции.
Константа равновесия отражает глубину протекания процесса. Чем больше величина константы равновесия, тем выше концентрация продуктов реакции в момент равновесия, т. е. тем полнее протекает реакция.
Константа равновесия зависит от природы реагирующих веществ, но не зависит от присутствия катализатора, так как он в равной степени ускоряет как прямую, так и обратную реакции. Влияние других факторов (концентрации веществ, давления газов и температуры) на величину константы равновесия мы разберем ниже на конкретных примерах.
СМЕЩЕНИЕ ХИМИЧЕСКОГО РАВНОВЕСИЯ
Состояние равновесия очень устойчивое, поэтому система может находиться в этом состоянии до тех пор, пока не изменятся параметры процесса: концентрации каких-либо веществ (или одного из реагентов), давление газовой смеси, температура. При этом вмешательстве извне изменяются скорости обеих реакций. Если обе скорости увеличиваются или уменьшаются в одинаковое число раз, т. е. сохраняется равенство vпр = vобр, то равновесие в данном случае не нарушается. Если изменение скоростей приводит к неравенствам vпр > vобр или vпр < vобр, то происходит смещение равновесия в направлении процесса, идущего с большей скоростью.
Направление смещения равновесия определяет принцип Ле-Шателье: если в системе, находящейся в состоянии равновесия, изменить одно из условий (концентрацию, давление или температуру), то равновесие смещается в направлении реакции, противодействующей данному изменению.
Разберем влияние внешних факторов на смещение химического равновесия.
Следствие 1. При увеличении температуры равновесие смещается в сторону эндотермической реакции, а при уменьшении – в сторону экзотермической.
Следствие 2. При увеличении давления в газовых смесях равновесие смещается в сторону образования меньшего числа молей газов, а при увеличении давления – в сторону образования большего числа молей газов.
Следствие 3. При увеличении концентрации какого либо компонента системы равновесие смещается в сторону расхода этого компонента.
Пример1 . В состоянии равновесия химической реакции N2+3H2=2NH3 концентрации азота, водорода, аммиака соответственно равны: 2,4, 7,2, 0.4 моль/л. Вычислите константу равновесия. Определите исходные концентрации азота и водорода.
Решение. Константа равновесия данной реакции выражается соотношением:
![]()
Подстановка значений концентраций дает К=1,7·10-4. В момент равновесия концентрация аммиака 0,4 моль/л. Из стехиометрического уравнения реакции следует, что прореагировало 0,4/2=0,2 моля азота и 0,4·3/2=0,6 молей водорода. Исходные концентрации: [N2]=0,2+2,4=2,6 моль/л; [Н2]=0,6+7,2=7,8 моль/л.
Пример 2. Напишите выражение для константы равновесия системы:
N2(г) + 3H2(г)Û 2NH3(г); DH = -92,4 кДж/моль. Изменением какого фактора (концентрации, давления или температуры) можно добиться уменьшения константы равновесия. В какую сторону сместится при этом равновесие системы?
Решение. Константа равновесия этой системы имеет вид:
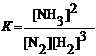
В соответствии с законом сохранения массы веществ, константа равновесия не зависит от концентрации веществ и давления газов (см. Пример 5 на стр.9), следовательно изменение Кравн. может вызвать лишь изменение температуры реакции (влияние природы веществ; Пример 8, стр.11). Для того, чтобы уменьшить Кравн. надо чтобы концентрация NH3 стала меньше концентрации N2 и H2, т. е. равновесие в системе должно смешаться влево. Такое смещение вызовет повышение температуры в системе, в соответствии с принципом
Ле шателье, т. к. обратная реакция эндотермическая.
Возможно одновременное изменение давления и температуры в системе. В этом случае надо отдельно разобрать влияние каждого фактора и сделать вывод о направлении смещения равновесия.
Пример 3. Используя справочные данные, найти значение температуры, при которой константа равновесия реакции образования водяного газа равна единице. С(графит)+Н2О(г.)↔СО(г.)+Н2(г.)
Решение. Из уравнения lnKp=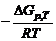 следует, что при Кр=1 стандартная энергия Гиббса химической реакции равна нулю. Тогда из соотношения
следует, что при Кр=1 стандартная энергия Гиббса химической реакции равна нулю. Тогда из соотношения 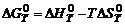 вытекает, что
вытекает, что ![]() . Воспользовавшись табличными данными находим, что ΔН=131,3 кДж, а ΔS=0,1336 кДж/К, отсюда Т=131,3/0,1336=983 К.
. Воспользовавшись табличными данными находим, что ΔН=131,3 кДж, а ΔS=0,1336 кДж/К, отсюда Т=131,3/0,1336=983 К.
Ответ: 983 К.
Пример 4. В какую сторону сместится равновесие гомогенной системы 2А![]() 2С+Д; DH<0, если увеличить давление в системе в 2 раза и одновременно понизить температуру на 300. Температурный коэффициент скорости прямой и обратной реакций равен, соответственно, 2,0 и 3,0.
2С+Д; DH<0, если увеличить давление в системе в 2 раза и одновременно понизить температуру на 300. Температурный коэффициент скорости прямой и обратной реакций равен, соответственно, 2,0 и 3,0.
Решение. Разберем влияние изменения давления на скорость каждой реакции. По закону действия масс:
v1 = k1[A]2, | v2 = k2[С]2[Д] |
Увеличение давления в 2 раза вызывает увеличение концентрации каждого из веществ в 2 раза (все вещества – газы), следовательно, скорости то же увеличиваются:
v1 =k1(2[A])2=4 k1[A]2, т. е. увеличилась в 4 раза, | v2 = k2(2[С])2(2[Д])=8k2[С]2[Д], |
т. е. увеличилась в 8 раз.
Изменение скоростей реакции, вызванное понижением температуры, рассчитываем на основании правила Вант-Гоффа: ![]() .
.
1. Для прямой реакции: 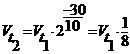 , т. е. скорость уменьшилась в 8 раз.
, т. е. скорость уменьшилась в 8 раз.
2. Для обратной реакции: 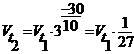 , т. е. скорость уменьшилась в 27 раз.
, т. е. скорость уменьшилась в 27 раз.
В итоге произведенных действий скорость прямой реакции изменилась в ![]() раз, а скорость обратной реакции – в
раз, а скорость обратной реакции – в ![]() раза, т. е. обе скорости уменьшились, но скорость прямой реакции все же больше скорости обратной реакции, следовательно, равновесие сместится в сторону прямой реакции.
раза, т. е. обе скорости уменьшились, но скорость прямой реакции все же больше скорости обратной реакции, следовательно, равновесие сместится в сторону прямой реакции.
Контрольные вопросы.
61. Напишите выражение для константы равновесия системы:
4HCl(г)+O2(г) Û 2H2O(г) + 2Cl2(г) , DHo298=-114,5кДж. Изменением какого фактора (концентрации, давления или температуры) можно добиться увеличения константы равновесия? В какую сторону сместится при этом равновесие системы?
62. Как можно добиться повышения выхода аммиака (изменяя концентрацию веществ, давление и температуру) в реакции, протекающей по схеме: N2 +3H2 Û 2NH3 ; DH < 0. Вывод сделайте на основании принципа Ле Шателье и подтвердите расчетом (в случае изменения давления, при условии, что давление изменяется соответственно в 3 раза) Напишите выражение константы равновесия.
63. В каком направлении сместится равновесие реакции: А2(г)+2В(г) Û 2АВ(г), если давление увеличить в 2 раза и одновременно повысить температуру на 500С? Температурный коэффициент прямой и обратной реакции равен соответственно 2 и 3. Каков знак DH0 этой реакции?
64. Напишите выражение Кр для гомогенной системы
N2 + 3H2 ![]() 2NH3,
2NH3, ![]() H = - 46 кДж
H = - 46 кДж
Какими изменениями концентрации, температуры и давления можно повысить выход NH3?
65. Напишите выражение Кр для гетерогенной системы CO2 + C![]() 2CO Какими изменениями концентрации и давления сместить влево равновесие системы?
2CO Какими изменениями концентрации и давления сместить влево равновесие системы?
66. Почему при изменении давления смещается равновесие системы
4HCl(г) + O2(г) ![]() 2H2O(г) + 2Cl2(г) и не смещается равновесие системы
2H2O(г) + 2Cl2(г) и не смещается равновесие системы
H2(г) + J2(г) ![]() 2HJ(г)? Напишите выражение Кр для каждой из систем.
2HJ(г)? Напишите выражение Кр для каждой из систем.
67. При 500 К константа равновесия равна 3,4·10-5. Вычислите для этой реакции ![]() .
.
68. Из приведенных ниже значений термодинамических функций укажите те, которые являются критерием состояния равновесия в изолированной системе (Р, Т=const):
а) DH < 0, б) DG < 0, в) DS > 0, г) DG = 0, д) DS = 0
Дайте обоснованный ответ. Возможно ли самопроизвольное изменение физической величины в выбранном Вами критерии после установления равновесия? Если нет, то как достичь изменения физической величины в выбранном Вами критерии с помощью внешнего воздействия?
69. Из приведенных ниже значений термодинамических функций укажите те, которые являются критерием состояния равновесия в закрытой системе (Р, Т=const):
а) DH > 0, б) DS = 0, в) DG > 0, г) DG = 0, д) DS > 0
Дайте обоснованный ответ. Можно ли изменять термодинамические параметры системы без нарушения равновесного состояния?
70. Для реакции Si(к)+2Н2О(г)«SiО2(к)+2Н2(г) укажите правильно записанное выражение для константы равновесия Кр:
а) 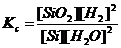 б)
б) ![]()
в) 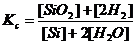 г)
г) ![]()
д) 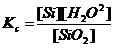 е)
е) ![]() ж)
ж) ![]()
Проанализируйте ошибки в неверно записанных выражениях. На основе какого закона составляется выражение для константы равновесия Кр?
71. При некоторых условиях для реакции 2NO(г)+Cl2(г)«2NOCl(г) константа равновесия равна 10. Какие выводы Вы можете сделать из этого значения?
72. В обратимой химической реакции А + 2В Û С равновесие наступило при следующих равновесных концентрациях: [А] = 0,6 моль/л; [В] = 1,2 моль/л; [С] = 2,16 моль/л. Определить константу равновесия и исходные концентрации веществ А и В.
73. Укажите, к какому из значений константы равновесия
Кр→0, Кр→∞, Кр→1
относятся утверждения (условия стандартные):
а) реакция протекает в прямом направлении практически необратимо,
б) реакция в прямом направлении почти не протекает, но практически полностью протекает в обратном направлении,
в) оба направления протекания реакции (прямое и обратное) практически равновероятны.
74. Рассмотрите следующую равновесную систему:
SO2(г)+ O2(г) = SO3(г) – 378 кДж
Как будет изменяться число молей SO3 в реакционной смеси, если:
а) добавить в систему O2;
б) удалить из системы SO2;
в) добавить катализатор;
г) уменьшить температуру?
75. Пользуясь принципом Ле-Шателье, укажите оптимальные условия (температуру и давление), обеспечивающие увеличение выхода аммиака при его прямом синтезе из азота и водорода. Объясните, почему в реальных условиях производственный процесс проводят при температурах С и используют катализатор?
76. В каком направлении сместится равновесие системы N2+3Н2=2NН3 DН0=-192 кДж/моль, при понижении температуры? Как объяснить, что на практике синтез аммиака ведут при повышенной температуре (не ниже С)?
77. В системе А(г.)+2В(г.)=С(г.) равновесные концентрации равны: [А]=0,06 моль/л; [В]=0,12 моль/л; [С]=0,216 моль/л. Найти константу равновесия реакции и концентрации веществ А и В.
78. Рассчитать константу равновесия реакции: 2SO3/г/«2SO2/г/+О2/г/., пользуясь справочными данными DG.
79. В закрытом сосуде установилось равновесие: СО2(г.)+Н2(г.)↔СО(г.)+Н2О(г.); константа равновесия равна единице. Определить: а) сколько процентов СО2 подвергнется превращению в СО при данной температуре, если смешать 1 моль СО2 и 5 молей Н2? б) в каких объёмных соотношениях были смешаны СО2 и Н2, если к моменту наступления равновесия в реакцию вступило 90% первоначального количества водорода?
80. При состоянии равновесия в системе N2(г.)+3Н2(г.)↔2NН2(г.); ΔН0=-92,4 кДж, концентрации участвующих веществ равны: [N2]=3 моль/л; [Н2]=9 моль/л; [NН3]=4 моль/л. Определить: исходные концентрации водорода и азота; б) в каком направлении сместится равновесие с ростом температуры? в) в каком направлении сместится равновесие с повышением давления?
81. Константа равновесия реакции FеО(к.)+СО(г.)↔Fе(к.)+СО2(г.) при некоторой температуре равно 0,5. Найти равновесные концентрации СО и СО2, если начальные концентрации составляли соответственно 0,05 и 0,01 моль\л.
82. Для реакции Н2(г.)+Br2(г.)↔2НВr(г.) при некоторой температуре Кр=1. Определить состав (в процентах по объёму) равновесной реакционной смеси, если исходная смесь состояла из трёх молей водорода и двух молей брома.
83. Константа равновесия реакции А(г.)+В(г.)↔С(г.)+D(г.) равна единице. Сколько процентов вещества А подвергнется превращению, если смешать 3 моля вещества А и 5 молей вещества В.
84. После смешивания газов А и В в системе А(г.)+В(г.)↔С(г.)+D(г.) устанавливается равновесие при следующих концентрациях: [А]=0,05 моль/л, [С]=0,02 моль/л. Константа равновесия равна 4·10-2. Найти исходные концентрации веществ А и В.
85. Найти константу равновесия реакции N2О4↔2NО2, если начальная концентрация N2О4 составляла 0,08 моль/л, а к моменту наступления равновесия диссоциировало 50% молекул N2О4.
86. В каком направлении сместятся равновесия
2Н2(г.)+О2(г.)↔2Н2О(г.), ΔН0= -483,6 кДж
СаСО3(к.)↔СаО(к.)+СО2(г.) ΔН0= 179 кДж
а) при повышении давления; б) при повышении температуры.
Ответ обосновать.
87. В каком направлении сместятся равновесия
2СО(г.)+О2(г.)↔2СО2(г.), ΔН0= -556 кДж
N2(г.)+О2(г.)↔2NО(г.) ΔН0= 180 кДж
а) при понижении температуры; б) при повышении давления.
Ответ обосновать.
88. Пользуясь табличными данными, вычислить константы равновесия следующей реакции при 298 К и при 1000К. СО(г.)+Н2О(г.)↔СО2(г.)+Н2 (г.)
89. Вычислить температуру, при которой константа равновесия реакции 2NО2(г.)↔N2О4(г.) равна единице. В каком направлении сместится равновесие при температуре более низкой, чем найденная.
90. Стандартное изменение энергии Гиббса для реакции А+В↔АВ при 298 К равно –8 кДж/моль. Начальные концентрации веществ А и В равны 1 моль/л. Найти константу равновесия и концентрации веществ А, В и АВ.
Растворы. Гидролиз солей. жесткость ВОДЫ.
Истинные растворы, которые Вам предстоит изучить, принадлежат к высокодисперсным системам. Кроме них существуют низкодисперсные системы типа суспензий и эмульсий и коллоидные системы (золи), занимающие промежуточное положение между ними по степени дисперсности.
Благодаря своим особым свойствам и характеристикам (адсорбция, поверхностное натяжение, коагуляция и др) дисперсные системы представляют большой практический интерес.
Обращение к изучению истинных растворов связано прежде всего с тем, что физико-химические свойства веществ зависят не только от их структуры, термодинамических и кинетических условий, но и характера среды реакции - неэлектролитов и электролитов. Тип раствора и является предмет изучения данной темы.
Физико-химическая природа процесса растворения (ключевое понятие) включает в себя как диффузию (физическая часть), так и сольватацию (химическая часть), последняя преобладает в электролитах.
Диффузия лежит в основе фазового перехода, характеризуемого величинами ∆Hф. п. и ∆Sф. п. (в случае электролита добавляется еще ∆Hсольв. и ∆Sсольв.). Именно от их сочетания
(∆G=∆H-T∆S) зависит растворимость веществ. Законы же Рауля объясняют такие физические свойства веществ в растворах, как повышение температуры кипения (∆tкип) и понижение температуры замерзания (∆tзам) по сравнению с чистыми веществами.
В свою очередь сольватация (гидратация) является причиной процесса электролитической диссоциации веществ, характеризуемого величиной константы диссоциации (Кд). Применительно к диссоциации воды Кд превращается в ионное произведение воды (![]() ) и затем в pH (водородный показатель).
) и затем в pH (водородный показатель).
Таким образом, в растворе вода может быть или просто реакционной средой, или реагентом. В первом случае она изменяет в основном физические свойства веществ (агрегатное состояние, растворимость, tкип, tзам). Во втором - физико-химические свойства (реакционная способность, кислотные, основные, окислительно-восстановительные, электрические).
Применяя рассматриваемые выше общие закономерности протекания химических реакций, следует учитывать роль среды как дополнительного фактора, влияющего на ход процесса.
В этой связи давайте обратимся к растворам и, прежде всего, водным, так как вода является наиболее распространенным компонентом растворов и обладает поистине уникальными свойствами.
Нельзя не заметить, что подавляющее большинство легко доступных материалов являются растворами или гетерогенными смесями, а не чистыми веществами или соединениями. Так, например, чистый атмосферный воздух - раствор, в котором кислород составляет около 1/5 части.
Повсеместность распространения растворов обусловлена самопроизвольным протеканием процессов растворения (∆G < 0) за счет увеличения энтропии в результате смешивания частиц. Изучая растворы, следует помнить о физико-химической природе происхождения растворов, знать основные признаки истинных растворов.
Изучая термодинамику процесса растворения, необходимо учитывать как его физическую сторону (фазовый переход, диффузия), так и химическую (сольватация). При этом следует помнить, что сольватация (гидратация) всегда является экзотермическим процессом (∆Hсольв.<0) и сопровождается уменьшением энтропии (∆Sсольв.<0).
Известно, что существуют растворы неэлектролитов и электролитов. Изучая неэлектролиты, следует знать основные свойства их разбавленных растворов такие, как давление насыщенного пара, температуры кипения и замерзания (законы Рауля)
При изучении электролитов, следует обратить внимание на их важнейшую характеристику - силу электролита, оцениваемую величинами степени диссоциации (a) и константы диссоциации (Кд)1. При этом необходимо иметь в виду, что сильные электролиты диссоциируют практически нацело (![]() G<<0, Кд≥1), а слабые – незначительно (
G<<0, Кд≥1), а слабые – незначительно (![]() G>0, Кд<1), причем ступенчато (Кд1>Кд2>Кд3)2. Следствием этого является тот важный факт, что реакции в растворах протекают между ионами. Известно, что сильные электролиты существуют преимущественно в виде ионов, а слабые - в виде недиссоциированных молекул.
G>0, Кд<1), причем ступенчато (Кд1>Кд2>Кд3)2. Следствием этого является тот важный факт, что реакции в растворах протекают между ионами. Известно, что сильные электролиты существуют преимущественно в виде ионов, а слабые - в виде недиссоциированных молекул.
Изучая слабые электролиты, не забывайте и об амфотерных - диссоциирующих двояко (по кислотному и основному типу). Это имеет большое практическое значение (например, алюминиевые конструкции устойчивы только в нейтральной среде).
Ярким примером такого амфотерного электролита является и вода, диссоциация которой количественно характеризуется постоянной величиной ионного произведения воды3
(К![]() =10-14). Эта константа дает возможность определить среду раствора (нейтральную, кислую, щелочную) через величину водородного показателя pH4.
=10-14). Эта константа дает возможность определить среду раствора (нейтральную, кислую, щелочную) через величину водородного показателя pH4.
Эта величина приобретает особое значение при изучении явления гидролиза5 как особого типа ионообменных реакций в растворах3
Глубина протекания данного процесса количественно оценивается величиной константы гидролиза Кг.
Вода играет столь большую роль в природе, технике и технологических процессах, что изучение ее свойств и поведения является совершенно необходимым для будущего инженера. Достаточно вспомнить, что почти ¾ поверхности земного шара покрыты водой, образующей океаны, моря, реки и озера. Много воды находится в газообразном состоянии в виде паров в атмосфере, а также в виде огромных масс снега и льда.
Широкое распространение воды и ее значение объясняется особыми свойствами, резко отличающими воду от других веществ.
Известно, что вода является хорошим растворителем вследствие высокой полярности ее молекул (µ=1,84Д). Самопроизвольно протекающие реакции гидратации (∆Нгидр<0,∆Gp<0) служат тому доказательством
А в реакциях гидролиза солей вода является основным сореагентом
Вода обладает также каталитической способностью. Только в присутствии воды протекают процессы электролитической диссоциации (ионные реакции идут только в растворах). В отсутствии следов влаги не протекают многие химические реакции, например, фтороводород HF не разъедает стекло, натрий не окисляется в атмосфере воздуха и т. п.
 Весь этот комплекс физических и химических свойств воды обуславливает ее огромную роль и в природе, и в технике. Использование воды в технике многосторонне. Вода используется не только как реагент или катализатор некоторых производств, но и как рабочая среда - ведь без снабжения водой не может работать ни одна отрасль народного хозяйства.
Весь этот комплекс физических и химических свойств воды обуславливает ее огромную роль и в природе, и в технике. Использование воды в технике многосторонне. Вода используется не только как реагент или катализатор некоторых производств, но и как рабочая среда - ведь без снабжения водой не может работать ни одна отрасль народного хозяйства.
1Кд есть величина Кр для процесса диссоциации слабых электролитов, так как этот процесс обратим (к нему применим принцип Ле-Шателье).
2Чем больше Кд, тем больше ионов в растворе слабого электролита.
3Зависит только от температуры и не зависит от состава раствора.
4pH = - lg[H+] вводится из-за удобства пользования логарифмической шкалой.
5Гидролиз соли - процесс обменного взаимодействия ее с молекулами воды, сопровождающийся изменением pH раствора. Не забывайте, что в холодных и умеренно концентрированных растворах гидролиз практически ограничивается первой стадией.
Рассматривая роль воды в технике, имейте в виду, что природная вода не бывает совершенно чистой, а всегда содержит некоторое количество растворенных и взвешенных веществ органического и минерального происхождения. Вода, содержащая значительное количество солей кальция и магния, называется жесткой, в отличие от мягкой воды, например, дождевой. Суммарное содержание этих солей в воде называется ее общей жесткостью, которая подразделяется на карбонатную (временную) и некарбонатную (постоянную). Первая из них обусловлена присутствием гидрокарбонатов кальция, магния, вторая - присутствием солей сильных кислот - сульфатов, хлоридов кальция и магния.
Присутствие в воде значительного количества солей кальция и магния делает воду непригодной для многих технических целей, в частности, для охлаждения. А при продолжительном питании паровых котлов жесткой водой их стенки постепенно покрываются плотным слоем накипи. Такой слой даже при толщине 1 см сильно понижает передачу теплоты стенками котла, что ведет к увеличению расхода топлива. Все это требует очистки воды от примесей. В частности, удаление солей кальция и магния, т. е. умягчение воды входит в систему водоподготовки - обработки природной воды.
В ходе водоподготовки воду освобождают от грубодисперсных и коллоидных примесей и от растворенных веществ.
Кроме указанных на схеме методов (кипячение, обработка Na2CO3, NaOH, Na3PO4 и др.) для умягчения воды применяют методы осаждения и ионного обмена - катионирования, а для биологической очистки используется озонирование. Применение ионного обмена исключительно многообразно. С помощью ионитов можно извлечь из производственных растворов многие металлы и их соли, уходившие ранее вместе со сточными водами безвозвратно (Ag, Au, Pt, Ni, Zn, Mo и др).
Для очистки естественных и сточных вод в настоящее время широко используется также явление взаимной коагуляции коллоидов. Коагуляция коллоидов коллоидами играет большую роль и в почвенных процессах.
С очисткой воды тесно связаны вопросы создания безотходных производств, составляющих одно из важных звеньев общей экологической проблемы. Со всем этим непременно должен быть знаком квалифицированный инженер.
Пример 1. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: a) KCN, б) Nа2СО3, в) ZnSО4. Определите реакцию среды растворов этих солей.
Решение: а) Цианид калия KCN - соль слабой одноосновной кислоты HCN и сильного основания КОН. При растворении в воде молекулы KCN полностью диссоциируют на катионы К+ и анионы CN-. Катионы К+ не могут связывать ионы ОН - воды, так как КОН — сильный электролит. Анионы CN - связывают ионы Н+ воды, образуя молекулы слабого электролита HCN. Соль гидролизуется, как говорят, по аниону. Ионно-молекулярное уравнение гидролиза:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



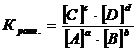 .
.