РАСТВОРЫ (модель VII )
Истинные растворы, которые Вам предстоит изучить, принадлежат к высокодисперсным системам. Кроме них существуют низкодисперсные системы типа суспензий и эмульсий и коллоидные системы (золи), занимающие промежуточное положение между ними по степени дисперсности.
Благодаря своим особым свойствам и характеристикам (адсорбция, поверхностное натяжение, коагуляция и др) дисперсные системы1 представляют большой практический интерес.
Обращение к изучению истинных растворов связано прежде всего с тем, что физико-химические свойства веществ зависят не только от их структуры, термодинамических и кинетических условий, но и характера среды реакции - неэлектролитов и электролитов. Тип раствора и является предмет изучения данной темы (рис. 2.3)
Физико-химическая природа процесса растворения (ключевое понятие) включает в себя как диффузию (физическая часть), так и сольватацию (химическая часть), последняя преобладает в электролитах.
Диффузия лежит в основе фазового перехода, характеризуемого величинами ∆Hф. п. и ∆Sф. п. (в случае электролита добавляется еще ∆Hсольв. и ∆Sсольв.). Именно от их сочетания (∆G=∆H-T∆S) зависит растворимость веществ. Законы же Рауля объясняют такие физические свойства веществ в растворах, как повышение температуры кипения (∆tкип) и понижение температуры замерзания (∆tзам) по сравнению с чистыми веществами.
____________________________
1Дисперсными системами называются такие, в которых одно вещество раздроблено (диспергировано) в другом. Раздробленное вещество называют дисперсной фазой, а среду в которой она распределена – дисперсионной средой (в случае истинных растворов имеем соответственно растворенное вещество и растворитель).
II. 2 подблок Модель VII
РАСТВОРЫ
Цель: Прогнозирование изменений физико-химических свойств веществ в растворах
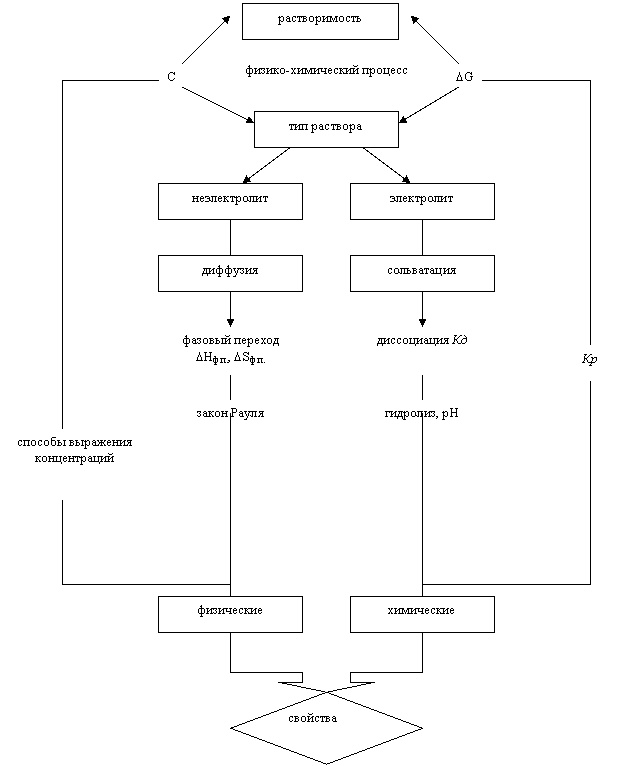 |
Рис. 2.3
В свою очередь сольватация (гидратация) является причиной процесса электролитической диссоциации веществ, характеризуемого величиной константы диссоциации (Кд). Применительно к диссоциации воды Кд превращается в ионное произведение воды (![]() ) и затем в pH (водородный показатель).
) и затем в pH (водородный показатель).
Таким образом, в растворе вода может быть или просто реакционной средой, или реагентом. В первом случае она изменяет в основном физические свойства веществ (агрегатное состояние, растворимость, tкип, tзам). Во втором - физико-химические свойства (реакционная способность, кислотные, основные, окислительно-восстановительные, электрические).
Известные Вам величины ∆G и Кр лежат соответственно в основе теоретического прогноза растворимости веществ и всех равновесных процессов, происходящих в растворах.
Обратите внимание, что за счет управления растворимостью повышается эффективность многих технологических процессов.

Вывод Прогнозирование изменений физико-химических свойств веществ в растворах осуществляется на основе знаний типа раствора (по типу связи) и таких его характеристик, как ∆G, Кр, С.
При изучении данной темы не забывайте и другие дисперсные системы (коллоиды, эмульсии, суспензии, пены), их основные свойства и области применения.
ИНЖЕНЕРНАЯ ХИМИЯ
ВВЕДЕНИЕ
Модельно-структурное наглядное представление учебного материала, лежащее в основе первых двух частей, находит свое продолжение в заключительной части пособия.
Как вы помните, было выделено всего 3 обобщенных блока курса химии:
1. Строение веществ;
2. Поведение веществ;
3. Инженерная химия.
Все блоки объединены общей идеей изучения вещества с точки зрения его природы (внутренней структуры), поведения в процессах, практического использования в профессиональной деятельности инженера.
Два первых общетеоретических блока «Строение веществ» и «Поведение веществ» составляли содержание соответственно первой и второй частей данного пособия. Материал третьего блока «Инженерная химия», который необходимо изучать на основе первых двух, изложен в данной практической части методического пособия. Здесь рассмотрены основные химические проблемы инженерной практики. Особое внимание следует уделить учебно-профессиональным задачам, решение которых дает возможность использовать теоретические знания курса Химии в конкретных инженерных ситуациях.
Кроме традиционного приложения справочных таблиц инженерного характера данное пособие содержит две обобщенные таблицы с описаниями. Одна из них рассматривает фундаментальные понятия курса в развитии, а вторая является как бы синтезом моделей и схем. Последняя тем самым концентрированно представляет курс Химии в целом и одновременно дает способ работы с ним.
ВВЕДЕНИЕ В БЛОК «ИНЖЕНЕРНАЯ ХИМИЯ»
(модель VIII)
Во внутреннем цикле модели VIII рассмотрены элементы основного предмета изучения данного блока - вещество и реакция. В качестве вещества изучаются конструкционные материалы - металлы и полимеры с их основными свойствами - металличностью и эластичностью (рис. 3.1).
В качестве реакции рассматриваются преимущественно окислительно-восстановительные процессы, лежащие в основе химических источников тока (ХИТ), используемых в энергетике, а также коррозии и электролиза, знание теории которых дает возможность химически грамотно защитить металлические конструкции от коррозии.
Практическое применение конструкционных материалов и энергетики базируется на фундаментальных знаниях строения и поведения веществ, что и отражено во внешнем цикле.
 Вывод Практическое использование веществ и процессов возможно только на основе системного изучения двух теоретических блоков – «Строение веществ» и «Поведение веществ».
Вывод Практическое использование веществ и процессов возможно только на основе системного изучения двух теоретических блоков – «Строение веществ» и «Поведение веществ».
Данный блок включает два подблока: «Конструкционные материалы» (модель IX) и «Электрохимические процессы» (модель Х).
III блок Модель VIII
ИНЖЕНЕРНАЯ ХИМИЯ
Цель: Практическое использование веществ и процессов на основе теоретического знания о них
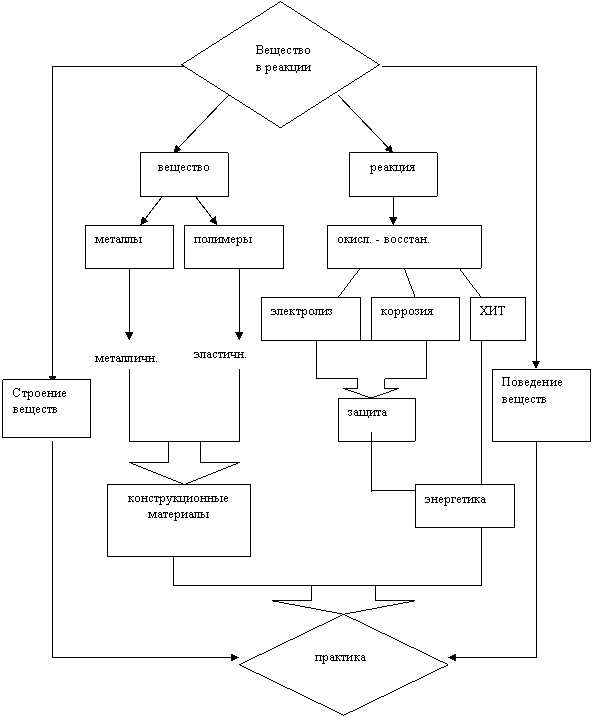 |
Рис. 3.1
КОНСТРУКЦИОННЫЕ МАТЕРИАЛЫ (модель IХ)
Сфера практического применения конструкционного материала определяется прежде всего его характером. Поэтому вид материала и является основным предметом изучения данной темы (рис. 3.2).
КОНСТРУКЦИОННЫЕ МАТЕРИАЛЫ
III. I подблок МодельIX
Цель: Практическое применение металлических и полимерных материалов на основе прогнозирования их свойств
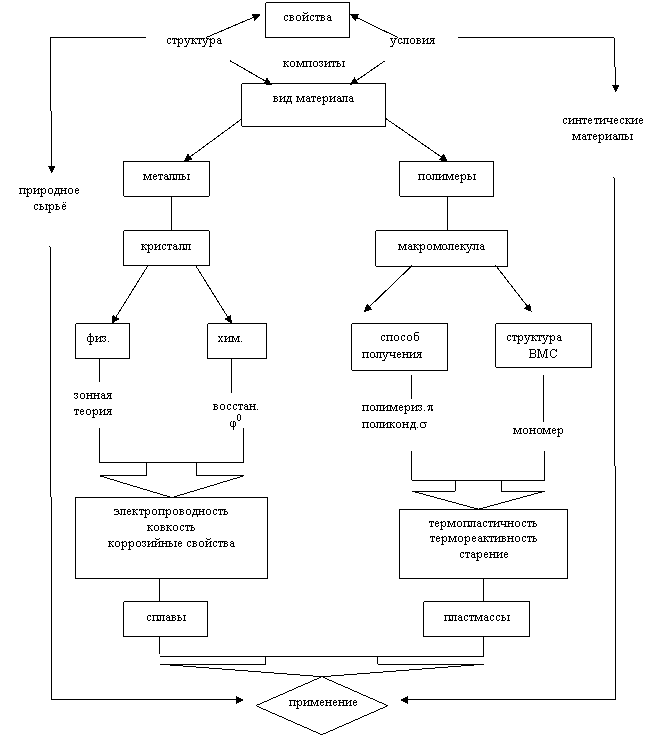 |
Рис. 3.2
Потребность в таких свойствах как высокая электропроводность, ковкость, износостойкость, термическая устойчивость, удовлетворяется металлами, основой которых является кристалл. В случае же необходимости иметь материалы, обладающие эластичностью, термопластичностью, коррозионной стойкостью, диэлектрическими свойствами и т. д., используют полимерные материалы, у которых макромолекулярное строение.
Физические свойства металлов (электропроводимость, пластичность, твердость, тугоплавкость, коррозионные свойства) диагностируются на основе знания металлической связи (ее специфики в конкретном металле) и зонной теории твердого тела. Химические же свойства (восстановительная способность) - величиной стандартного электродного потенциала φ0 (функция ∆G0).
Свойства полимеров зависят от очень многих факторов. Во-первых, от способа получения - полимеризации (разрыв π-связи) и поликонденсации (наличие функциональных групп при σ-связи). Во-вторых, от структуры, определяемой внутренней природой мономеров и связями между ними.
На практике чаще используются композиты (ключевое понятие), а не «чистые» металлы и полимеры. Это связано с тем, что как сплавы (смесь, твердый раствор), так и пластмассы (полимер, наполнитель) резко меняют свойства отдельных компонентов, что дает возможность получения материалов с нужными свойствами.
Во внешнем цикле показано, что свойства как металлических (природное сырье), так и полимерных (синтетических) материалов определяются, прежде всего, их структурой и конечно же условиями получения.
 |
ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ (модель X)
Различают электрохимические процессы двух типов: одни идут самопроизвольно (∆G < 0) за счет превращения химической энергии в электрическую X®Э, другие - только под действием электрического тока Э®Х (∆G > 0). Этим и определяется их практическое использование. Следовательно, тип процесса является основным предметом изучения данной темы (рис. 3.3).
Химизм любого электрохимического процесса отражает следующее ключевое уравнение обратимой реакции
|
направление которой и определяет тот или иной тип процесса. Первый тип процессов включает химические источники тока и коррозию и характеризуется величиной ЭДС (исходя из
DG0 = - nFE0). В основе электрохимической коррозии лежит механизм образования локальных микрогальванических элементов (пар), на подавлении работы которых и основана защита металлов от коррозии.
ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
III.2 подблок Модель X
Цель: Использование электрохимических процессов в зависимости от их типа
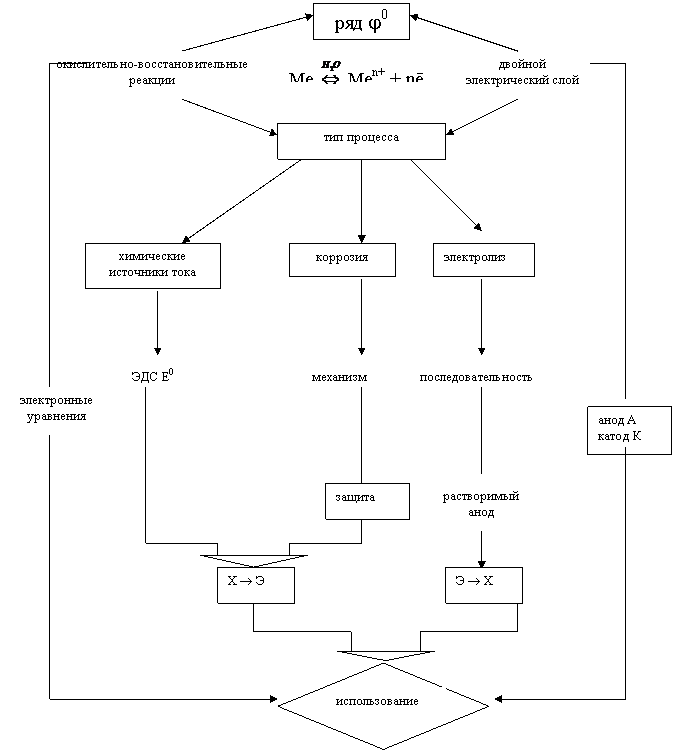
Рис. 3.3
Второй тип процессов представляет электролиз, который используется для получения веществ (металлов, кислот, щелочей и др.), а в инженерной практике с помощью растворимого анода производятся металлические покрытия, очистка металлов, электрохимическая обработка их. Конкретное протекание электролиза определяется последовательностью выделения веществ на электродах (катод, анод), характеризуемой значениями электродных потенциалов.
Именно ряд φ есть самая важная количественная характеристика в электрохимии. Стандартный электродный потенциал (φ°) возникает вследствие образования двойного электрического слоя на границе фаз (Ме - раствор). Двойной электрический слой, в свою очередь, - результат гетерогенной окислительно-восстановительной реакции, в которой процессы окисления и восстановления пространственно разделены. Поэтому анодный А (окисление) и катодный К (восстановление) процессы, составляющие химическую сущность электрохимии, есть не что иное, как электронные уравнения.
 гальванический элемент или электролиз) в зависимости от знака ЭДС (?К - ?А). Ряд ?0 позволяет составить уравнения анодного и катодного процессов, с тем чтобы предвидеть возможность практического применения их.
" width="635" height="154"/>
гальванический элемент или электролиз) в зависимости от знака ЭДС (?К - ?А). Ряд ?0 позволяет составить уравнения анодного и катодного процессов, с тем чтобы предвидеть возможность практического применения их.
" width="635" height="154"/>
ЗАДАНИЕ НА КОНТРОЛЬНУЮ РАБОТУ И
Общие указания к выполнению контрольной работы
В процессе изучения курса химии студент должен выполнить одну контрольную работу. Решение задач и ответы на теоретические вопросы должны быть коротко, но четко обоснованы. При решении задач нужно приводить весь ход решения и математические преобразования.
Контрольная работа должна быть аккуратно оформлена, написана четко и ясно и иметь поля для замечаний рецензента. Номера и условия задач необходимо переписывать в том порядке, в каком они указаны в задании. В начале работы следует указать учебный шифр студента, номер варианта и полный список номеров задач этого варианта. В конце работы следует дать список использованной литературы с указанием года издания.
Работа должна иметь подпись студента и дату.
Если контрольная работа не зачтена, ее следует выполнить повторно в соответствии с указаниями рецензента и представить вместе с не зачтенной работой. Исправления следует выполнять в конце работы, после рецензии, а не в тексте.
Контрольная работа, выполненная не по своему варианту, преподавателем не рецензируется и не засчитывается как сданная.
Каждый студент выполняет вариант контрольных заданий, обозначенный двумя последними цифрами номера студенческого билета (86594, две последние цифры 94, им соответствует вариант контрольного задания 94)
Варианты контрольного задания
Номер варианта | Номера задач | ||||||||||
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | ||||
01 | 31 | 61 | 91 | 1 | 31 | 61 | 91 | 121 | 151 | 181 | 211 |
02 | 32 | 62 | 92 | 2 | 32 | 62 | 92 | 122 | 152 | 182 | 212 |
03 | 33 | 63 | 93 | 3 | 33 | 63 | 93 | 123 | 153 | 183 | 213 |
04 | 34 | 64 | 94 | 4 | 34 | 64 | 94 | 124 | 154 | 184 | 214 |
05 | 35 | 65 | 95 | 5 | 35 | 65 | 95 | 125 | 155 | 185 | 215 |
06 | 36 | 66 | 96 | 6 | 36 | 66 | 96 | 126 | 156 | 186 | 216 |
07 | 37 | 67 | 97 | 7 | 37 | 67 | 97 | 127 | 157 | 187 | 217 |
08 | 38 | 68 | 98 | 8 | 38 | 68 | 98 | 128 | 158 | 188 | 218 |
09 | 39 | 69 | 99 | 9 | 39 | 69 | 99 | 129 | 159 | 189 | 219 |
10 | 40 | 70 | 00 | 10 | 40 | 70 | 100 | 130 | 160 | 190 | 220 |
11 | 41 | 71 |
| 11 | 41 | 71 | 101 | 131 | 161 | 191 | 221 |
12 | 42 | 72 |
| 12 | 42 | 72 | 102 | 132 | 162 | 192 | 222 |
13 | 43 | 73 |
| 13 | 43 | 73 | 103 | 133 | 163 | 193 | 223 |
14 | 44 | 74 |
| 14 | 44 | 74 | 104 | 134 | 164 | 194 | 224 |
15 | 45 | 75 |
| 15 | 45 | 75 | 105 | 135 | 165 | 195 | 225 |
16 | 46 | 76 |
| 16 | 46 | 76 | 106 | 136 | 166 | 196 | 226 |
17 | 47 | 77 |
| 17 | 47 | 77 | 107 | 137 | 167 | 197 | 227 |
18 | 48 | 78 |
| 18 | 48 | 78 | 108 | 138 | 168 | 198 | 228 |
19 | 49 | 79 |
| 19 | 49 | 79 | 109 | 139 | 169 | 199 | 229 |
20 | 50 | 80 |
| 20 | 50 | 80 | 110 | 140 | 170 | 200 | 230 |
21 | 51 | 81 |
| 21 | 51 | 81 | 111 | 141 | 171 | 201 | 231 |
22 | 52 | 82 |
| 22 | 52 | 82 | 112 | 142 | 172 | 202 | 232 |
23 | 53 | 83 |
| 23 | 53 | 83 | 113 | 143 | 173 | 203 | 233 |
24 | 54 | 84 |
| 24 | 54 | 84 | 114 | 144 | 174 | 204 | 234 |
25 | 55 | 85 |
| 25 | 55 | 85 | 115 | 145 | 175 | 205 | 235 |
26 | 56 | 86 |
| 26 | 56 | 86 | 116 | 146 | 176 | 206 | 236 |
27 | 57 | 87 |
| 27 | 57 | 87 | 117 | 147 | 177 | 207 | 237 |
28 | 58 | 88 |
| 28 | 58 | 88 | 118 | 148 | 178 | 208 | 238 |
29 | 59 | 89 |
| 29 | 59 | 89 | 119 | 149 | 179 | 209 | 239 |
30 | 60 | 90 |
| 30 | 60 | 90 | 120 | 150 | 180 | 210 | 240 |
Химическая термодинамика
Энергетика химических процессов
Одной из важнейших характеристик всякого технологического процесса является его энергетика.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



