Перенапряжением на электродах зависит от состава электролита, его концентрации, положения металла в ряду стандартных электродных потенциалов, плотности тока, температуры, состояния поверхности электродов.
Потенциалы разложения электролитов обычно определяют опытным путем. Последовательность разряда ионов на электродах зависит от величины перенапряжения. Особенно велико перенапряжение при выделении газов на металлах. Так, при выделении водорода на цинке создается перенапряжение около 0,7В, а ![]() , поэтому при электролизе солей металлов средней активности одновременно разряжаются и ионы металла, и ионы водорода. Вследствие этого выход металла по току средний.
, поэтому при электролизе солей металлов средней активности одновременно разряжаются и ионы металла, и ионы водорода. Вследствие этого выход металла по току средний.
Анодное выделение О2 тоже имеет значительную величину перенапряжения. Величины перенапряжений при катодном выделении металлов значительно меньше. Электрохимические процессы на электродах подчиняются законам Фарадея:
1. Количество вещества, выделенного на электродах при электролизе, прямо пропорционально количеству тока, прошедшего через электролит.
2. При электролизе различных электролитов равные количества электричества выделяют на электродах количества вещества, прямо пропорциональные их эквивалентам.
При пропускании через электролит 96500 Кл электричества выделяется
1г×экв вещества. Это число обозначают через F=96500 Кл и называют числом Фарадея. Математически закон Фарадея записывается так:
![]() , (19)
, (19)
где m – масса выделенного вещества, г;
Э – химический эквивалент или масса 1 г×экв;
Q – количество протекшего электричества, Кл;
I – сила тока, А;
t – время электролиза, с.
![]() показывает количество вещества, выделившегося при пропускании одного кулона электричества. Это электрохимический эквивалент. Между химическим и электрохимическим эквивалентом существует зависимость
показывает количество вещества, выделившегося при пропускании одного кулона электричества. Это электрохимический эквивалент. Между химическим и электрохимическим эквивалентом существует зависимость
Э = а×F, (20)
здесь Э – химический эквивалент;
а– электрохимический эквивалент.
При электролизном выделении газов в формулу закона Фарадея вводят пропорциональные величины:
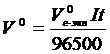 (21)
(21)
где V0 – объем выделенного газа при нормальных условиях;
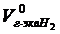 =11,2 л;
=11,2 л; 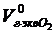 =5,6 л – объемы грамм-эквивалентов водорода и кислорода.
=5,6 л – объемы грамм-эквивалентов водорода и кислорода.
Для определения выхода по току используют следующую формулу:
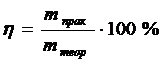 . (22)
. (22)
ЭЛЕКТРОЛИЗ С РАСТВОРИМЫМ АНОДОМ
Растворимые металлические аноды, которые окисляются, используются для очистки металлов, анодной обработки их, рафинирования, анодирования, хромированния и т. д.
Для примера рассмотрим электролиз водного раствора Cu(NO3)2 с растворимым медным анодом:
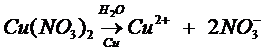
![]()
![]()
Сu
К А
Составим возможные процессы на аноде и катоде:
К: Cu2+ +2e ® Cuo В
2Н2О+2е® Н2+2ОН- ![]() В
В
Т. к. >![]() на катоде образуется медь Cu
на катоде образуется медь Cu
А: ![]() не разряжается
не разряжается
2Н2О -4е® О2+4Н+ 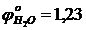 В
В
Т. к. <![]() - на аноде преобладает окисление меди.
- на аноде преобладает окисление меди.
Пример 1. Сколько граммов свинца выделится на катоде при пропускании через раствор Pb(NO3)2 тока силой 7А в течение 15 мин?
Решение. В растворе содержатся ионы соли ![]() и
и ![]() , а также молекулы Н2О. При пропускании тока на катоде восстанавливаются в основном ионы
, а также молекулы Н2О. При пропускании тока на катоде восстанавливаются в основном ионы![]() и частично водород, а на аноде окисляются молекулы Н2О и выделяется кислород.
и частично водород, а на аноде окисляются молекулы Н2О и выделяется кислород.
 |  |
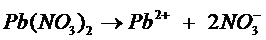
![]()
![]()
К А
Составим возможные процессы на аноде и катоде:
 К: Pb2+ +2e ® Pbo В
К: Pb2+ +2e ® Pbo В
2Н2О+2е® Н2+2ОН- ![]() В
В
А: ![]() не разряжается
не разряжается
 2Н2О -4е® О2+4Н+
2Н2О -4е® О2+4Н+ 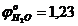
По закону Фарадея масса выделенного свинца
![]() г.
г.
где t – время, с
Э – химический эквивалент свинца, равный 103,6.
Пример 2. Рассчитайте, сколько выделилось водорода и кислорода при электролизе водного раствора NaOH при пропускании электрического тока в течение 2 ч 30 мин при силе тока в 3А.
Решение. В растворе содержатся ионы Na+ и ОН- и молекулы Н2О. В соответствии с порядком разряда ионов на электродах идут процессы:
 |  |
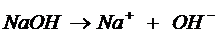
![]()
![]()
К А
К: Na+ +e ® Nao
![]() 2Н2О+2е® Н2+2ОН-
2Н2О+2е® Н2+2ОН- ![]()
Т. к. ![]() >> на катоде преобладает Н2
>> на катоде преобладает Н2
А: 4 ОН - -4е ® 2Н2О+О2 ![]()
2Н2О -4е® О2+4Н+ 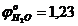
Т. к. ![]() <
<![]() на аноде окисляется ОН-.
на аноде окисляется ОН-.
По закону Фарадея
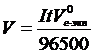 ;
; ![]() л,
л, ![]() л.
л.
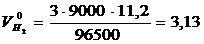 л;
л; ![]() л.
л.
Пример 3. Какие процессы протекают при электролизе раствора AgNO3 с инертным анодом, с серебряным анодом? Сколько выделится вещества на инертном аноде если на катоде образовалось 10,8 г серебра?
Решение.


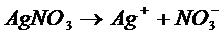
![]()
![]()
Ag
К А
В обоих случаях на катоде преобладает процесс (![]() >
>![]() ):
):
К: Ag+ + е®Ago,
а на аноде в случае инертного анода преобладает процесс окисления Н2О
А: ![]() не разряжается
не разряжается
2Н2О -4е® О2+4Н+ 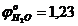
с серебряным анодом
А: Ag - е® Ag+
Происходит растворение анода ![]() <
<![]()
На основе второго закона Фарадея имеем, что при выделении 1 г×экв. Ag (108г) выделится 1 г×экв. O2 (5,6 л), тогда образование 10,8г Cu соответственно даст
108 г - 5,6 л
10,8 г - Х
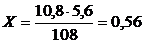 л О2
л О2
Контрольные вопросы.
151. Сколько электричества надо пропустить через раствор NaCl, чтобы получить 500 кг NaOH?
152. Какое количество металлов выделится при электролизе расплавов MgCl2 и CaCl2 при пропускании тока силой 4А в течение 5 ч?
153. Сколько времени пропускали через раствор щелочи ток силой 3А, если при этом выделилось 2,24 л кислорода, измеренного при нормальных условиях? Составьте электронные уравнения процессов, происходящих на электродах.
154. В какой последовательности протекают процессы на электродах при электролизе растворов солей равной концентрации Na3PO4, NiSO4, AgNO3, CuSO4? Составьте электронные уравнения процессов.
155. Сколько времени пропускали ток силой 8А через раствор сульфата никеля, если масса никелевого анода стала меньше на 0, 8805 г.
156. Сколько выделится металла на катоде при электролизе раствора CuSO4 при 95% выходе металла по току в течение 40 минут при силе тока в 4А?
157. Сколько граммов воды разложилось, если через раствор пропустить ток силой 5А в течение 2,5 часа?
158. Определить эквивалент олова, если при электролизе раствора SnCl2 в течение 1 часа при силе тока в 3А выделилось 6,64 г металла.
159. Через раствор хлористого кальция пропускали электрический ток при силе тока 3А. Какие ионы разряжались при этом у катода и у анода? Какие продукты и в каком количестве выделились у катода и анода?
160. Через раствор CoSO4 пропускали ток до тех пор, пока весь кобальт не выделился из раствора. Какие процессы происходили при этом у катода и у анода? Что представляет собой оставшаяся жидкость?
161. Сколько времени протекал электролиз, если при силе тока в 4А восстановился 1 мг×экв. алюминия?
162. Сколько времени надо пропускать электрический ток через раствор NiSO4 с никелевым анодом при силе тока 3,5А, чтобы покрыть пластину площадью 10 см2 слоем никеля в 2 мм. Плотность никеля 8,9 г/см3 (4,6 часа).
163. Раствор содержит ионы Fe2+, Bi3+, Рb2+ в одинаковой концентрации. В какой последовательности будут разряжаться эти ионы при электролизе раствора?
164. В растворе находились 0,1 моля HgCl2 и 0,2 моля СuCl2. Какие вещества и в каком количестве выделяются на угольных электродах, если через раствор пропустить ток в 10 А в течение 1 часа?
165. Какие процессы происходят на аноде и катоде при электролизе раствора FeCl2, если электроды:
а) угольные;
б) железные?
166. Какие вещества и в каком количестве выделяются на угольных электродах при электролизе раствора KBr в течение 1ч. 35мин при силе тока 15А.
167. Определите выход по току, если при прохождении через раствор AgNO3 96500Кл электричества на катоде выделилось 100г серебра. Составьте электронные уравнения процессов, протекающих на угольных электродах.
168. Определите массу хрома, которая выделится на катоде при электролизе сульфата хрома в течение 3-х часов при токе 13,4 А, если выход хрома по току равен 50%. Приведите схему электролиза раствора сульфата хрома.
169. Какие реакции протекают на электродах при электролизе раствора сульфата цинка: а) с графитовым анодом; б) с цинковым анодом. Как изменится концентрация ионов цинка в растворе в обоих случаях, если через раствор пропустить ток силой 26,8 А в течение 1 часа. Выход по току на катоде цинка 50%, на аноде - 100%.
170. При пропускании тока, силой 2 А в течение 1 часа 14 мин 24 с через водный раствор хлорида металла (II) на одном из графитовых электродов выделился металл массой 2,94 г. Чему равна атомная масса металла, если выход по току 100%, и что это за металл. Напишите уравнения реакций, протекающих на электродах.
171. При пропускании тока, силой 2 А в течение 1 часа 14 мин 24 с через водный раствор хлорида металла (II) на одном из графитовых электродов выделился металл массой 2,94 г. Чему равна атомная масса металла, если выход по току 100%, и что это за металл. Напишите уравнения реакций, протекающих на электродах.
172. При электролизе сульфата натрия получили при н. у. Н2 объемом 448 л. Напишите уравнение реакций, протекающих на нерастворимых аноде и катоде и рассчитайте, сколько времени протекал электролиз, если ток был 100 А.
173. При электролизе раствора сульфата меди на аноде выделился кислород объемом 560 мл, измеренный при н. у. Сколько граммов меди выделилось на катоде? Приведите схему электролиза.
174. Электролиз раствора сульфата цинка проводили с нерастворимым анодом в течении 6,7 часов, в результате чего выделился кислород объемом 5,6 л, измеренный при н. у. Вычислите ток и массу осажденного цинка при выходе его по току 70%. Приведите схему электролиза.
175. Напишите уравнение реакций, протекающих на нерастворимых электродах при электролизе водного раствора КОН. Какие вещества и в каком объеме можно получить при н. у., если пропустить ток 13,4 А в течении 2-х часов.
176. Напишите уравнение реакций, протекающих на графитовых электродах при электролизе: а) расплава MgCl2, б) раствора MgCl2. Сколько времени необходимо вести электролиз при токе 2 А, чтобы на катоде выделилось вещество массой 2,43 г (для реакций а) и б) ).
177. Через раствор PbSO4 пропущено 2 F электричества. Как изменится количество Pb2+ в растворе, если электроды: а) графитовые, б) свинцовые. Выход по току свинца составляет на катоде 50%, на аноде - 100%.
178. Найти эквиваленты олова, зная, что при токе, силой 2,5 А из раствора SnCl2 за 30 минут выделяется 2,77 г олова. Написать схему электролиза раствора SnCl2.
179. При электролизе водного раствора Cr2(SO4)3 током, силой 2 А масса катода увеличилась на 8 г. В течении какого времени проводили электролиз? Составьте электронные уравнения процессов, происходящих при электролизе.
180. Сколько времени пропускали ток силой 8 А через раствор сульфата никеля, если масса никелевого анода стала на 0,8805 г меньше? (Написать схему электролиза сульфата никеля).
КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ
Коррозией называется процесс непреднамеренного разрушения металлов вследствие физико-химического взаимодействия их с окружающей средой.
Коррозия – это самопроизвольно (DG<0) протекающий гетерогенный окислительно-восстановительный процесс разрушения металлов и их сплавов в результате взаимодействия с окружающей средой, происходящий с выделением энергии (DН<0) и рассеиванием продуктов реакции (DS>0).
В общем виде реакцию разрушения (коррозии) металла можно представить упрощенно уравнением:
![]()
Гетерогенные реакции коррозионного разрушения металлов в зависимости от среды по механизмам процессов разделяются на два основных типа: коррозия химическая и электрохимическая.
Химическая коррозия
Принципиальная возможность или невозможность самопроизвольного процесса химической коррозии определяется характером изменения функции Гиббса (DG).
Когда процессы окисления металла и восстановления окислительного компонента (например, кислород воздуха, серосодержащие соединения в углеводородах нефти) коррозионной среды протекают в одном акте:
![]()
имеет место химическая коррозия.
Различают химическую коррозию двух видов: газовую и коррозию в неэлектролитах. При химической коррозии механизм процесса заключается в диффузии атомов или ионов металла через утолщающуюся пленку продуктов коррозии к среде и молекул среды к металлу. Например, при газовой коррозии металла в атмосфере воздуха на поверхности металла образуется оксид, через слой которого происходит диффузия молекул кислорода к металлу и ионов металла к поверхности. Примеры газовой коррозии: образование окалины при термообработке металла, коррозия клапанов цилиндров, поршней и выхлопных труб двигателей внутреннего сгорания и т. п.
Жидкостная коррозия (коррозия в неэлектролитах) проявляется при соприкосновении металлов с жидкостями, не проводящими электрического тока (жидкие углеводороды, смазочные масла и др.).
При химической коррозии в отличие от электрохимической, процессы окисления и восстановления реализуются в одном месте и электрических явлений не наблюдается.
ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
Когда при взаимодействии металла с электролитом окисление (ионизация) его атомов
![]() (1)
(1)
и восстановление окислительного компонента коррозионной среды, например, растворение в воде кислорода
2Н2О+О2+4е®4ОН-
протекают раздельно на возникающих анодных и катодных участках короткозамкнутого гальванического элемента, тогда возникает электрохимическая коррозия.
Электрохимическая коррозия сопровождается электрическими явлениями и может быть разделена на два вида: гальванокоррозию и электрокоррозию.
1. Гальванокоррозия – анодный процесс окисления металла возникает вследствие образования микрогальванической цепи.
2. При электрокоррозии металл окисляется под воздействием электрического тока от внешнего источника. Например, коррозия металлов под действием блуждающих токов.
Скорость электрохимической коррозии определяется, главным образом, электродным потенциалом металла, электропроводностью электролита и рядом других факторов.
Возможность и интенсивность коррозионного разрушения металла может быть оценена по величине уменьшения значения функции Гиббса
DG=-nF(jК - jА) (2)
где jК и jА – потенциалы предполагаемых электродов коррозионного гальванического элемента;
F – число Фарадея;
n – число электронов, участвующих в ионизации атомов Ме.
Из уравнения (1) следует, что коррозионный процесс теоретически возможен, если потенциал анодного процесса будет (jА) меньше потенциала катодного процесса (jК)
jА < jК (3)
При электрохимической коррозии возникает коррозионный гальванический элемент, который в общем виде можно записать так:
Ме1 / среда / Ме2 (4)
где Ме1 и Ме2 – металлы с электродными потенциалами j1 и j2, причем j1 < j2
Под средой понимается – окружающая среда, обычно указываются окислительные компоненты, например, Н+; Н2О; О2. В данном случае анодом является металл Ме1, имеющий меньший электродный потенциал, а катодом является Ме2.
Работа коррозионного гальванического элемента включает следующие одновременно протекающие сопряженные реакции:
- анодный процесс – переход ионов из металла в раствор (электролит) с образованием гидратированных ионов:
![]() (5)
(5)
- катодный процесс, проходящий на поверхности второго металла Ме2, - присоединение электронов каким-либо окислителем называемым деполяризатором (Д)*, находящимся в растворе электролита:
 *Деполяризатор – вещество, снижающее или устраняющее поляризацию электродов при работе Г-Э.
*Деполяризатор – вещество, снижающее или устраняющее поляризацию электродов при работе Г-Э.
![]() (6)
(6)
В результате этих реакций электроны в металле движутся от анода к катоду, а в электролите перемещаются ионы.
При этом на катоде происходит процесс деполяризации - кислородной и водородной.
Коррозия с кислородной деполяризацией состоит в присоединении избыточных электронов к растворенному в электролите кислороду воздуха. При рН ≥ 7 на катоде происходит реакция:
О2+2Н2О+4е→4ОН- (7)
Процесс коррозии металла, у которого катодная деполяризация осуществляется ионами водорода, называют коррозией с водородной деполяризацией:
2Н++2е→Н2 (8)
Поскольку основным конструкционным материалом всех отраслей производства являются стали различных марок, то с их коррозионным разрушением мы встречаемся наиболее часто.
Сталями называются железоуглеродные сплавы, содержащие меньше 2,14% углерода, который находится в виде цементита (Fe3C), а в нержавеющих сталях в виде твердого раствора в кристаллах железа.
Интенсивное разрушение металлов вследствие электрохимической коррозии происходит в следующих случаях: во влажной загрязненной атмосфере, в различных электролитах, при контакте двух различных металлов, а также в случае неоднородного состава металла. Например, в техническом железе величина электродных потенциалов включений Fe3C (j=0,1В) выше, чем у железа (j=-0,44В), поэтому в электролитах они будут выполнять роль катодных участков, на их поверхности будут протекать процессы восстановления. Железо в этом случае, являясь анодом, будет окисляться и превращаться в ионы. Схема коррозионного разрушения стали с кислородной деполяризацией представлена на рис.1.
Электролит рН ≥ 7
 |
Рис. 1. Схема электрохимической коррозии стали3 (Fe-Fe3C)
с кислородной деполяризацией
ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
Разнообразные методы защиты от коррозии можно разделить на четыре основных вида:
1. Защитные покрытия
2. Электрохимические методы защиты
3. Изменение свойств коррозионной среды
4. Применение сплавов, стойких против коррозии
Защитные покрытия изолируют металл от агрессивной среды. Они могут быть металлическими, неорганическими и органическими.
Неметаллическая защита состоит в изолировании поверхности металла, сплавов от агрессивной среды (электролита) при помощи консистентных смазок - лаков, красок, пластмасс, эластомеров.
Металлические покрытия называются анодными, если они состоят из более активного металла, имеющего меньший потенциал, чем защищаемый.
Металлы менее активные, имеющие больший потенциал, чем защищаемый, называют катодными покрытиями. Некоторые металлы, энтропия оксидов которых мала, защищаются окисными пленками (пассивация).
При электрохимической защите металлы соединяют или с катодом внешнего источника тока, или с более отрицательным металлом.
В первом случае защита называется электрозащитой, во втором – протекторной. Принцип действия в обоих случаях состоит в том, что металл, получая электроны от внешнего источника, становится катодом (по отношению к электролиту) и не должен корродировать.
При электрозащите в качестве анода применяют металлический лом, который корродирует, предохраняя от коррозии защищаемую конструкцию.
Полученный отрицательный потенциал должен быть настолько большим, чтобы все анодные участки металла стали катодными. Если этого нет, коррозия будет продолжаться, но значительно медленнее чем без защиты. Использовать электрохимическую защиту можно только в хорошо проводящей среде – в растворах электролитов, в почве, морской воде, но не в атмосферных условиях.
Вещества, вводимые в среду для замедления коррозии, называются ингибиторами. Молекулы ингибиторов адсорбируются на поверхности, препятствуя деятельности катодных или анодных участков или тех и других одновременно. По своему химическому составу ингибиторы относятся к различным классам химических соединений. Ингибиторы широко применяются для замедления коррозии.
Прочные пленки на металлах образуются действием сильных окислителей – хроматов и бихроматов щелочных металлов, концентрированных кислот (HNO3, H2SO4 и др), а также органических веществ (желатины, алкалоидов и пр.). Защитные пленки могут быть образованы также веществами, которые при взаимодействии с ионами металла образуют труднорастворимые продукты коррозии, тормозящие дальнейшую ионизацию металла (карбонаты, фосфаты, силикаты щелочных металлов, едкий натр и др.)
Пример 1. Опишите процессы коррозии луженого железа на воздухе в случае нарушения целостности покрытия.
Решение. Луженое железо представляет собой железо, покрытое оловом. В воздухе присутствуют водяные пары, конденсирующиеся на поверхности металла и кислород. При нарушении целостности покрытия возникает коррозионный гальванический элемент.
Fe / H2O, O2 / Sn (1)
Работа этого элемента обуславливает протекание коррозионных разрушений.
Из табл. 5 определяем 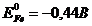 ,
, 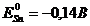 . Так как
. Так как ![]() <
<![]() , то железо будет анодом, на котором будет протекать процесс окисления железа
, то железо будет анодом, на котором будет протекать процесс окисления железа
Анод:
Fe - 2e = Fe2+ (2)
Олово будет катодом, на котором идет процесс кислородной деполяризации.
Катод:
Sn / O2+2H2O+4e = 4OH- (3)
Суммарное уравнение коррозионного процесса
2Fe + O2+2H2O =2Fe(OH)2 (4)
В результате вторичных процессов на железе образуется ржавчина:
4Fe(OH)2+O2+2H2O=4Fe(OH)3 (5)
Fe(OH)2→Fe(OH)3→xFeO∙yFe2O3∙zH2O (6)
Пример 2. Медная пластинка, склепанная с серебряной, опущена в кислоту. Составить электронные уравнения процесса коррозии этой пластинки. Какой металл будет разрушаться?
Решение. Эта пластинка, опущенная в кислоту, образует гальваническую пару Cu0-Ag0, в которой анодом будет медь, так как ее электродный потенциал меньше потенциала серебра (![]() ;
; ![]() ), а катодом - серебро. Медь будет разрушаться. Коррозия меди выразится следующими электронными уравнениями.
), а катодом - серебро. Медь будет разрушаться. Коррозия меди выразится следующими электронными уравнениями.
А: Cu0 - 2e = Cu2+ анодный процесс;
К: 2H+ + 2e = H2 катодный процесс.
(Ag)
на катоде - водородная деполяризация
Пример 3. Железное изделие покрыли никелем. Какое это покрытие – анодное или катодное? Ответ мотивировать. Какой металл будет корродировать при повреждении защитного слоя? Составить электронные уравнения происходящих процессов во влажном воздухе.
Решение. Покрытие никелем железного изделия является катодным покрытием, так как электродный потенциал никеля больше потенциала железа.
![]() ;
; 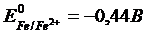
При повреждении защитного слоя корродировать будет железо. В образующейся гальванической паре Fe0-Ni0 анодом будет железо, а Ni – катодом. На катоде - кислородная деполяризация. Происходящие процессы выражаются следующими электронными уравнениями:
А Fe0 - 2e = Fe2+ анодный процесс;
К 2H2O + O2 + 4e = 4OH - катодный процесс.
(Ni)
Контрольные вопросы
181. Составьте схему атмосферной коррозии алюминия в контакте с медью.
182. В контакте с цинком или железом коррозия магния будет протекать быстрее? Составить схемы процесса коррозии.
183. Какие металлы в гальванических парах Cu-Fe, Zn-Fe, Zn-Cu являются анодом, какие катодом в процессе коррозии? Ответ мотивировать.
184. Составьте схему коррозии железа в кислой среде: а) покрытого медью; б) покрытого марганцем (в случае нарушения целостности покрытия).
185. Составьте схемы коррозии луженого и оцинкованного железа.
186. Какое из покрытий – анодное или катодное эффективнее защищает металл от коррозии? Приведите примеры. Составьте электронные уравнения происходящих процессов.
187. Железное изделие покрыли кадмием. Какое это покрытие – анодное или катодное? Какой металл будет корродировать в случае нарушения целостности покрытия? Составьте электронные уравнения (среда кислая).
188. В раствор хлорида натрия опущены железная пластинка, склепанная с цинковой, и железная пластинка, склепанная с медной. В каком случае коррозия железа будет протекать быстрее? Составьте электронные уравнения протекающих процессов.
189. Составьте электронные уравнения процессов при погружении в электролит луженого железа и луженой меди.
190. Для защиты паровых котлов от коррозии в них вводятся листы цинка (протекторная защита). Объясните механизм этой защиты.
191. Чем можно объяснить, что такой активный металл как алюминий, хорошо сопротивляется атмосферной коррозии?
192. В растворе хлорида натрия коррозия железа протекает энергично. Если добавить к этому раствору равный объем щелочи коррозия прекращается. Дать объяснение этому явлению.
193. Кусочек железа, опущенный в раствор медного купороса, покрывается слоем меди. Если железо предварительно смочить концентрированным раствором бихромата калия (K2Cr2O7) и, ополоснув водой, поместить в раствор CuSO4, медь не выделится. Объясните наблюдаемые явления. Напишите уравнения реакции.
194. Две железные пластинки, частично покрытые, одна оловом, другая - медью, находятся во влажном воздухе. На какой из этих пластинок быстрее образуется ржавчина? Почему? Ответ подтвердите составлением электронных уравнений анодного и катодного процессов коррозии этих пластинок.
195. Как влияет рН среды на скорость коррозии железа и алюминия? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этих металлов в разных средах.
196. Одну из цинковых пластин поместили в раствор СuSO4, другую - в СиCl2. На какой из этих пластинок коррозия протекает быстрее? Почему?
197. Предложите катодное покрытие для защиты меди от атмосферной коррозии. Составьте электронные уравнения катодного и анодного процессов в случае нарушения сплошности покрытия.
198. Предложите анодное покрытие для защиты цинка от коррозии. Составьте электронные уравнения катодного и анодного процессов в кислой среде в случае нарушения сплошности покрытия.
199. Объясните с точки зрения электрохимической коррозии (образования микрогальванопар) явление обесцинкования латуни (сплав меди и цинка).
200. На медные изделия часто наносят покрытия из олова или серебра. Составьте электронные уравнения процессов, происходящих при коррозии таких изделий в кислой среде в случае повреждения покрытий. Какое из этих покрытий является анодным?
201. При травлении пленок Al на кремниевой подложке кислотными растворами иногда наблюдается потемнение проводника. С чем это связано? Составьте электронные уравнения процессов.
202. В радиоприборостроении нередко используют контакты Al-Au. С какой деполяризацией протекает коррозия такого контакта в кислых средах? Составьте электронные уравнения процессов.
203. Сравните, как пойдет коррозия металлических сооружений:
а) в воде - при низких и высоких температурах (зима - лето, север - юг);
б) в водной и неводной частях - при одной и той же температуре.
204. Трубопроводы водопроводной системы, сделанные из латуни, со временем становятся хрупкими и приобретают красный цвет. Объясните это явление. Напишите уравнения реакций, описывающих возможный механизм.
205. Легированная сталь, также как и сталь-3 химически неоднородна. Как Вы можете объяснить тот факт, что первая, в отличие от второй, коррозионно устойчива? Приведите схему коррозии стали-3.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



