1-исследуемая группа; 2- контроль
Параллельно с клинико-биохимическими исследованиями проводилась разработка комплексной реабилитации детей, употребляющих ПАВ, и детей, перенесших внутриутробную алкогольную и наркотическую интоксикацию. Комплексная реабилитация составлялась с учетом выявленных особенностей состояния здоровья и развития детей на основе индивидуального подхода. В комплекс реабилитации включались как общеоздоровительные мероприятия (коррекция режима дня, питания, лечебная физкультура, спортотерапия, закаливание, массаж, лечебная гимнастика), так и специальные лечебные воздействия. Дети школьного возраста, употребляющие ПАВ, получали дезинтоксикационную терапию, ноотропы с седативным эффектом, корректоры поведения, транквилизаторы (по показаниям), физиотерапию, витамины, метаболиты и постоянно находились под пристальным наблюдением нарколога, педиатра, психолога и педагога.
В комплексную реабилитацию детей, перенесших внутриутробную наркотическую интоксикацию, были внесены коррективы, согласно выстроенным индивидуальным прогностическим сценариям и выявленным особенностям развития. Детям назначались курсы ноотропных и сосудистых препаратов, улучшающих мозговое кровообращение, микроциркуляцию и метаболизм, а также витаминотерапия, иммуномодуляторы, препараты железа и физиотерапия. Большое внимание уделялось занятиям ребенка с психологом, логопедом и педагогом.
В качестве дополнительных средств реабилитации были выбраны препараты метаболического ряда: биотредин и глицин. Они применялись под контролем показателей активности СДГ и a-ГФДГ лимфоцитов периферической крови.
Оценка эффективности предложенных комплексных реабилитационных мероприятий осуществлялась по результатам динамического наблюдения за состоянием здоровья, физического и нервно-психического развития детей и цитохимического исследования активности ферментов лимфоцитов.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Анализ показателей заболеваемости и болезненности наркологическими расстройствами среди несовершеннолетних Астраханской области за год показал, что 95% зарегистрированных наркологических расстройств представлено УВП для здоровья ПАВ, без формирования синдрома зависимости. Самым распространенным ПАВ в детской среде является алкоголь, который употребляют 70% учтённых несовершеннолетних потребителей ПАВ. Вместе с тем, показатели болезненности и заболеваемости УВП наркотических веществ сохраняются на стабильно высоком уровне и в 2 -3 раза превышают данные по РФ. Что касается показателей болезненности и первичной заболеваемости вследствие УВП ненаркотических веществ, то они имеют неравномерный характер, периодически повышаясь и снижаясь в несколько раз.
В процессе анонимного анкетирования 359 социально благополучных учащихся Астраханских школ (1 группа) и 160 социально неблагополучных детей, проживающих в детских домах и школах-интернатах (2 группа), выявлено, что среди воспитанников домов-интернатов курение распространено в 3 раза больше (в 31,9% случаев), чем среди социально благополучных школьников (р<0,001). Примерно одинаковое количество детей 1 и 2 исследуемых групп (соответственно 7,0% и 11,3%, р>0,05) признались в употреблении ПАВ и заявили об употребление ПАВ их друзьями (соответственно 5,3% и 9,4%, р>0,05). Большинство детей, употребляющих ПАВ (73,7%- 1 группа; 92,3% - 2 группа, р>0,05), отдают предпочтение производным каннабиса.
Обследование детей, употребляющих ПАВ, выявило, что средний возраст детей при постановке на учет в наркологическом диспансере составляет 14,8±0,2 лет. Самыми популярными в детской среде ПАВ являются никотин и алкоголь, их применяют, соответственно, 93,1% и 92,1% потребителей ПАВ. На третьем месте стоят производные каннабиса (73,3%), на четвертом - ЛР (45,5%). Большинство детей начинают знакомство с ПАВ именно с никотина и алкоголя, причем в достаточно раннем возрасте (соответственно 9,5±0,4 лет и 11,1±0,3 лет). Несколько позже дети начинают использовать ЛР (в 11,6±0,4 лет) и производные каннабиса (в 13,2±0,3 лет). Таким образом, первые пробы ПАВ происходят значительно раньше взятия ребенка на учет.
Среди наркологических расстройств у 93,0% детей отмечается УВП ПАВ (чаще сочетанное - у 60,4%), у 2,0% - наркомания и у 5,0% - токсикомания. Сформированная табачная зависимость встречается у 44,6%. Чаще всего дети злоупотребляют алкоголем (76,2%), производными каннабиса (62,4%), никотином (42,6%) и ЛР (39,6%). Главным мотивом потребления ПАВ является чувство подражания компании (33,7%). Вместе с тем, большинство детей имеют отягощенный социальный анамнез. 85,2% детей воспитываются в неполных семьях и 61,4% несовершеннолетних имеют наследственную отягощенность по наркомании и алкоголизму. Бродяжничество стало «болезнью» 40,6% детей. Более половины детей когда-либо участвовали в преступлениях (58,4%) и имеют судимость (51,5%).
Клинический осмотр выявил у 49,5% несовершеннолетних отставание в физическом развитии, у 12,9% - отставание или задержку в нервно-психическом развитии и у 76,2% детей - снижение интеллектуально-мнестических функций. При этом установлено, что снижение интеллектуально-мнестических функций связано с употреблением ЛР (r=0,25, р<0,05). Редко у детей отмечаются признаки соматической патологии в виде нарушений ритма сердца (18,8%), приглушенности сердечных тонов (9,0%), мягкого систолического шума (8,0%), жесткого (4,0%) или ослабленного дыхания (1,0%) и увеличения печени (3,0%). Из нозологий у детей встречается хронический бронхит (4,0%), хронический гастрит (3,0%), энурез (3,0%), хронический пиелонефрит (2,0%) и токсический фарингит (2,0%). Определяются единичные случаи химического ожога полости рта, острого трахеита, кардиопатии, миокардиодистрофии, бронхиальной астмы, синдрома вегето-сосудистой дистонии, эндометриоза, туберкулеза (по 1,0%).
ЭКГ-исследование установило изменения в работе сердца у 43,7% детей. У каждого четвертого обследованного ребенка отмечаются нарушения ритма (23,4%) и проводимости (23,4%). В 6,2% случаев выявляется нарушение внутрижелудочковой проводимости, в 17,2% - признаки неполной блокады правой ножки пучка Гиса. Реже на ЭКГ фиксируются изменения метаболического и дистрофического характера (15,6%). У 4,7% детей определяется перегрузка желудочков сердца с признаками гипертрофии.
Изучение биохимических маркеров поражения миокарда выявило повышение миоглобина (р<0,05), КФК-МВ (р<0,001) и АсАТ (р<0,05) у детей, употребляющих ПАВ, по сравнению с детьми контрольной группы (табл.3). Вместе с тем, у всех детей исследуемой группы уровень миоглобина и АсАТ укладывался в рамки референтных значений. В то же время, показатель КФК-МВ у 14,0% детей исследуемой группы превышал пределы референтных значений и в среднем составлял 7,5±0,8 нг/мл. Корреляционный анализ выявил прямую зависимость между уровнем КФК-МВ и употреблением никотина (r=0,30, р<0,05), а также между показателем КФК-МВ и отказами детей от лечения (r=0,36, р<0,01). Прямая корреляция отмечена также между показателем NT-proBNP и использованием алкоголя (r=0,36, р<0,01).
При исследовании печеночных ферментов было выявлено статистически достоверное повышение активности ЛДГ-П у детей, употребляющих ПАВ, по сравнению с детьми контрольной группы. У двух детей (4,0%) показатель ЛДГ-П превышал референтные пределы, максимально достигая значения 517 Ед/л. Увеличение ЛДГ-П происходило при злоупотреблении ребенка табаком (r=0,42, р<0,01) и систематическом злоупотреблении ЛР (r=0,65, р<0,05). Вычисленный коэффициент де Ритиса (АсАТ/АлАТ=1,63) свидетельствовал о преобладании процессов деструкции и изменениях циркуляции в сердечной мышце у детей, злоупотребляющих ПАВ.
У всех детей значение ТТГ было в пределах референтных значений и не отличалось от показателей в контрольной группе (р>0,05). Уровень Т4 в среднем также не отличался от данных контроля (р>0,05), но у 14,0% детей исследуемой группы был ниже референтных норм, что свидетельствует о субклиническом течении гипотиреоза в условиях йоддефицитного и возможно, белководефицитного состояния. Средний показатель Т3 у детей, употребляющих ПАВ, превышал среднее значение контроля и у 12% детей был выше референтных норм. Увеличению показателя Т3 способствовало ежедневное употребление алкоголя (r=0,55, р<0,001) и ЛР с развитием галлюцинаций (r=0,58, р<0,01).
Табл.3
Биохимические показатели детей, употребляющих ПАВ
Показатель | Референтные значения | Значение показателя, М±m | Р | ||
муж | жен | Исследуемая группа | Контроль | ||
Тропонин Т (нг/мл) | < 0,01 | 0,009±0,0001 | 0,009±0,0003 | >0,05 | |
Миоглобин (нг/мл) | 25-72 | 29,2±0,4 | 22,0±0,2 | <0,05 | |
КФК-МВ (нг/мл) | 0,1-4,94 | 3,8±0,3 | 2,5±0,1 | <0,001 | |
NT-proBNP (пг/мл) | <125 | 39,1±6,4 | 28,3±2,2 | >0,05 | |
АсАТ(Ед/л) | <37 | <31 | 18,4±0,6 | 13,6±1,1 | <0,05 |
АлАТ(Ед/л) | <41 | <31 | 11,3±0,6 | 9,9±0,9 | >0,05 |
ЛДГ-П (Ед/л) | 230 – 460 | 311,4±10,4 | 273,8±8,9 | <0,05 | |
ТТГ (мкМЕ/мл.) | 0,27 - 4,2 | 1,4±0,1 | 1,6±0,1 | >0,05 | |
Т3(пмоль/л) | 3,5-7,7 | 6,2±0,3 | 5,3±0,1 | <0,05 | |
Т4(пмоль/л) | 12,0-22,0 | 16,0±0,5 | 15,7±0,4 | >0,05 |
Концентрация тестостерона у большинства мальчиков (78,7%) исследуемой группы (16,9±1,4 нмоль/л) и всех мальчиков контрольной группы (14,8±2,1 нмоль/л) превышала возрастные референтные значения. Вместе с тем, у 20,0% детей исследуемой группы (10 мальчиков или 21,3% мальчиков), двое из которых страдали токсикоманией, отмечался резко сниженный уровень тестостерона (1,8±0,7 нмоль/л, р<0,001) по сравнению с контролем и возрастными нормами. Это явилось следствием патогенного воздействия ПАВ непосредственно на гонадную систему ребенка, в особенности при злоупотреблении или регулярном употреблении ЛР (r=-0,31, р<0,05; r=-0,48, р<0,05 соответственно). Изучение уровня ДГЭА-С не выявило статистически значимых различий между показателями исследуемой (1,9±0,1мкг/мл) и контрольной группы (1,5±0,2 мкг/мл, р>0,05), но обозначило корреляционные связи между уровнем ДГЭА - С и, соответственно токсикоманией, влечением к ЛР и употреблением алкоголя (r=-0,31, р<0,05; r=-0,35, р<0,05; r=0,30, р<0,05), которые могут выступать прогностически неблагоприятными факторами риска нарушения гормонопродуцируемой функции надпочечников при продолжении использования ПАВ.
У большинства детей исследуемой группы (90,2%) значение пролактина (223,9±12,7 мМЕД/л) укладывалось в возрастные нормы, но было ниже уровня контрольной группы (288,4±21,0 мМЕД/л, р<0,05). У 9,8% детей показатель пролактина был повышен (в среднем 541,3±45,1 мМЕД/л). Наличие гиперпролактинемии у детей сопровождалось развитием жалоб на слабость, усталость (r=0,44, р<0,01), неустойчивость настроения (r=0,31, р<0,05), бродяжничество (r=0,39, р<0,05).
По мнению (2000) такие изменения биохимических показателей правомерно назвать «метаболическим хаосом» - дисметаболическим состоянием вследствие функциональных изменений органов адаптационного или реактивного типа на ранних этапах злоупотребления ПАВ. Они носят нестабильный, преходящий характер и объясняются функциональными нагрузками на органы и системы ребенка при злоупотреблении ПАВ, а также специфическими последствиями фармако-химического взаимодействия различных ПАВ с функциональными системами организма. В связи с вышеизложенным, столь развитое в детской среде сочетанное потребление ПАВ, выдвигает определенные требования к диагностике и лечению этой категории больных.
Анализ заболеваемости и болезненности наркологическими расстройствами среди женского населения Астраханской области показал, что самой распространенной и прогрессирующей нозологией является хронический алкоголизм. На втором месте стоит наркомания, показатели учтенной распространенности которой превышают данные РФ.
За период с гг. в МУЗ «Клинический родильный дом» г. Астрахани поступило 186 женщин, страдающих наркоманией. Из них 59,1% женщин находились на диспансерном учете в ГУЗ «Наркологический диспансер». Все наркозависимые использовали внутривенный способ введения наркотиков, предпочтение отдавалось производным опийного ряда. 36,4% женщин употребляли ПАВ в течение 1-5 лет, а 63,6 % - более 5 лет. 58,9% человек также занимались табакокурением и 9,1% женщин поступили на роды в состоянии алкогольного опьянения.
Женщины, страдающие наркозависимостью, в анамнезе имели высокий процент абортов (57,0%, р<0,001). У 34,4% женщин роды стали преждевременными, тогда как в группе сравнения таковыми были только 4,3% родов (р<0,001). Необходимо отметить, что у 1,6% женщин исследуемой группы произошел поздний выкидыш, у 4,2% - антенатальная гибель плода и у 3,9% - смерть ребенка в раннем неонатальном периоде.
Отличительной особенностью новорожденных исследуемой группы явилась незрелость и ЗВУР, которые встречались в 56,2% (р<0,001) и 46,1% случаев (р<0,01) соответственно. В связи с высокой частотой признаков незрелости и недоношенности у 24,7% детей отмечались СДР ( р<0,001) и у 9,0% - пневмопатия (р<0,05). Характерным было перинатальное поражение ЦНС (ПЭП) новорожденных (93,0%, р<0,001). Чаще всего встречался синдром угнетения (33,2%, р<0,05) и внутричерепной гипертензии (23,6%, р<0,001). Синдром отмены имел место у 16,9% детей (р<0,01). У половины детей (48,9%, р<0,001) в первые дни жизни отмечались признаки ВУИ (рис.1).
Изучение психомоторного развития 92 детей, перенесших внутриутробную наркотическую (44 ребенка), алкогольную (38 детей) и сочетанную (10 человек) интоксикацию, выявило отклонения в их развитии в раннем возрасте.
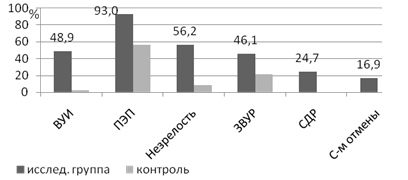
Рис.1 Особенности состояния здоровья новорожденных от наркозависимых женщин
Так, на момент обследования, двое детей (2,2%) имели детский церебральный паралич и по одному ребенку (1,1%) - эпилепсию и микроцефалию. В возрасте 6 месяцев жизни отставание в нервно-психическом развитии отмечалось у 56,7% исследуемых, а задержка развития была характерна для 28,4% детей. В 1 год жизни отставание в развитии отмечалось у 20,0% детей, а задержка нервно-психического развития - 68,0% у детей. К 2 годам задержку в нервно-психическом развитии имели уже 80,7%, а в 3 года - 88,9% детей. У всех детей, перенесших внутриутробную интоксикацию ПАВ, после 2-х летнего возраста отмечалась задержка в моторном развитии, тогда как у детей из группы сравнения, проживающих в доме ребенка и не имеющих в анамнезе сведений о наркомании и алкоголизме матери, моторное развитие соответствовало возрасту (15,0%) или опережало его (85,0%, р<0,001). У большинства исследуемых детей отмечалась более выраженная, по сравнению с другими детьми домов ребенка, задержка развития навыков социальной адаптации (у 72,4% до года и у 48,3% после года, р<0,001), ручной умелости на протяжении всего раннего детства (62,1%, р<0,001) и речевой активности до года (55,2%, р<0,05). Задержка речевого развития после года отмечалась примерно одинаково часто у детей исследуемой группы и группы сравнения (соответственно 93,1% и 90,0%, р>0,05), что является характерной особенностью детей, проживающих в условиях социальной депривации.
В ходе детального исследования стало ясно, что наибольший вред психическому здоровью ребенка наносит алкоголь, регулярно принимаемый матерью во время беременности, особенно в сочетании с наркотическими веществами. К 3 годам жизни все дети, рожденные алкогользависимыми женщинами или женщинами, употребляющими как наркотики, так и алкоголь, имели задержку нервно-психического развития. Вместе с тем, в подгруппе детей, рожденных от наркозависимых матерей, задержка развития встречалась только в половине случае.
Важной частью комплексной оценки состояния здоровья 116 детей, рожденных от матерей, употребляющих ПАВ, было изучение их физического развития. В период новорожденности большинство детей исследуемой группы (73,5%, р<0,001) имели отклонения в физическом развитии и развивались хуже своих сверстников – воспитанников домов ребенка (группа сравнения). В дальнейшем процент детей исследуемой группы, имеющих отклонения в физическом развитии колебался от 76,5% до 84,4% и статистически достоверно не отличался от показателей группы сравнения. К 3 годам жизни физическое развитие детей группы сравнения в большинстве случаев пришло в норму (66,7%), задержки в физическом развитии не отмечалось. Однако данная тенденция не распространялась на детей, рожденных алкоголь - и наркозависимыми матерями. Отклонения в физическом развитии имели 82,4% детей исследуемой группы (рис.2). Задержка физического развития отмечалась у 11,8%, отставание – у 70,6% детей (р<0,01).
Отклонения в физическом развитии чаще отмечались у детей, перенесших внутриутробную алкогольную интоксикацию. К 2 годам жизни у всех детей данной подгруппы отмечались отклонения в физическом развитии (100%, р<0,05), тогда как у детей, испытавших наркотическую внутриутробную интоксикацию, отклонения в физическом развитии встречались в 71,4% случаев.
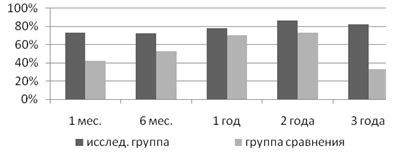
Рис.2 Динамика отклонений в физическом развитии у детей, перенесших внутриутробную интоксикацию ПАВ
Характерным для детей, чьи матери принимали алкоголь во время беременности, было наличие задержки физического развития с 1 года жизни (3,2%, рис.3). К двум годам случаи задержки физического развития отмечались только у детей данной подгруппы (27,3%, р<0,05). С трех лет жизни задержка физического развития стала появляться и в подгруппе детей, перенесших внутриутробную наркотическую интоксикацию, но отмечалась реже (10,0%).
Рис. 3 Динамика задержки физического развития детей, перенесших внутриутробную алкоголь - и наркоинтоксикацию
В 4 года жизни половина детей, испытавших внутриутробную алкогольную интоксикацию, и 20% детей, рожденных наркозависимыми матерями, имели задержку физического развития.
Особенностью детей, рожденных алкогользависимыми женщинами, было низкое (85,7%, р<0,01) и резко дисгармоничное физическое развитие (45,5%, р<0,05) в раннем возрасте (2 года), которое в других подгруппах встречалось реже или не отмечалось вовсе.
Изучив преморбидный фон 96 детей, рожденных алкоголь - и наркозависимыми женщинами, было отмечено, что отставание в физическом и нервно-психическом развитии является скорее закономерностью, нежели случайностью. 89,6% детей на первом месяце и 97,9% на первом году жизни страдали перинатальными поражениями ЦНС. Все дети на первом году жизни переносили те или иные инфекционные заболевания. Более половины детей неоднократно болели ОРВИ (61,5%, р<0,05).
Анализ фенотипических особенностей детей, испытавших внутриутробную интоксикацию ПАВ, позволил определить повышенный уровень стигматизации детей, перенесших опийную интоксикацию, (в среднем 5,9 стигм) и специфические для опийной внутриутробной интоксикации стигмы дисэмбриогенеза (широкое пупочное кольцо с явлением пупочной грыжи (р<0,001), выступающий лоб (р<0,05), брахицефалию (р<0,01), страбизм (р<0,01) и гипоплазию нижней челюсти (р<0,001)).
ЭХО-КГ и УЗИ внутренних органов детей, перенесших внутриутробную химическую интоксикацию, выявило высокий уровень врожденных аномалий развития. У 76,0% детей были диагностированы врожденные аномалии развития сердца. В 22,0% случаев были определены пороки развития сердца в виде ДМПП (12,0%), ДМЖП (6,0%), ОАП (4,0%), двухстворчатого клапана аорты (2,0%). У одного ребенка регистрировался сочетанный порок в виде ООО, ДМПП и ОАП. МАРС отмечались у 54,0% детей. Изменения миокарда в виде гипертрофии и дилатации правых отделов сердца определялись у 5,3% детей с аномалиями развития сердца. Кроме того, у 8,0% детей были диагностированы аномалии и пороки развития почек (дистопия гипоплазированной почки, удвоение почки, расширение или удвоение чашечно-лоханочной системы почки и ротация почки).
ЭКГ-исследование детей, рожденных ПАВ-зависимыми женщинами, зафиксировало изменения у 60,0% детей. У 44,0% детей они заключались в нарушениях ритма, которые выражались в синусовой тахикардии (16,0%) и аритмии (28,0%). Непосредственное токсическое воздействие ПАВ на сердце проявлялось на ЭКГ изменениями метаболического, дистрофического характера (18,0%) и нарушениями проводимости. В 16,0% случаев регистрировались признаки неполной блокады правой ножки пучка Гиса, в 2,0% - нарушение внутрижелудочковой проводимости. У 12,0% детей отмечалось нарушение процессов реполяризации и у 2,0% - перегрузка желудочков или правых отделов сердца с явлениями гипертрофии последних.
Как показали результаты биохимических исследований (табл.4), у всех детей исследуемой группы уровень тропонина Т, был достоверно выше показателей контрольной группы и коррелировал с нарушениями внутрижелудочковой проводимости (r=0,36, р<0,001). Исследование АсАТ не выявило статистически значимых различий данного показателя у детей исследуемой и контрольной группы. Вместе с тем, у 16,0% детей исследуемой группы отмечалось выраженное повышение АсАТ (до 326 Ед/л), что сопровождалось признаками аритмии на ЭКГ (r=0,59, р<0,001). Средний уровень NT-proBNP у детей исследуемой и контрольной групп был примерно одинаковым. Уровень КФК-МВ был повышен у 70,0% детей исследуемой группы. В контрольной группе детей повышенный уровень КФК-МВ отмечался в 2 раза реже (31,0% случаев) и в среднем был ниже в 1,5 раза (р<0,001).
Изучение АлАТ и АсАТ выявило статистически значимое увеличение АлАТ у детей исследуемой группы. При этом у детей, чьи матери употребляли во время беременности алкоголь, уровень АлАТ был статистически достоверно выше (18,9 ±3,1 Ед/л., р<0,05), по сравнению с детьми, испытавшими внутриутробную наркотическую интоксикацию (12,7±0,5 Ед/л). Данное обстоятельство можно объяснить гепатотропным действием алкоголя. Вместе с тем, коэффициент де Ритиса (АсАТ/АлАТ) составил 2,17 и свидетельствовал о преобладании дистрофических процессов в сердечной мышце у детей, перенесших внутриутробную наркотическую и алкогольную интоксикацию.
Табл.4
Биохимические показатели детей, перенесших внутриутробную алкогольную и наркотическую интоксикацию
Показатель | Референтные значения | Значение показателя, М±m | Р | ||
муж | жен | Исследуемая группа | Контроль | ||
Тропонин Т (нг/мл) | < 0,01 | 0,0096±0,0002 | 0,008±0,0003 | <0,001 | |
Миоглобин (нг/мл) | 25-72 | 27,8±0,4 | 28,4±0,5 | >0,05 | |
КФК-МВ (нг/мл) | 0,1-4,94 | 6,9±0,5 | 4,5±0,1 | <0,001 | |
NT-proBNP (пг/мл) | <125 | 105,2±22,1 | 100,3±11,1 | >0,05 | |
АсАТ(Ед/л) | <37 | <31 | 36,9±6,2 | 30,5±1,2 | >0,05 |
АлАТ(Ед/л) | <41 | <31 | 17,0±2,1 | 12,4±0,6 | <0,05 |
ЛДГ-П (Ед/л) | 230 – 460 | 467,6±14,5 | 431,5±19,2 | >0,05 | |
ТТГ (мкМЕ/мл.) | 0,27 - 4,2 | 2,1±0,2 | 2,0±0,2 | >0,05 | |
Т3(пмоль/л) | 2,4-9,8 | 7,4±0,5 | 6,0±0,3 | <0,05 | |
Т4(пмоль/л) | 12,0-22,0 | 15,1±0,6 | 15,8±0,6 | >0,05 |
Исследование гормонального статуса щитовидной железы не выявило статистически значимых различий ТТГ и Т4 у детей исследуемой и контрольной групп. У примерно одинакового процента детей исследуемой (18,0%) и контрольной (13,3%, р>0,05) группы отмечался низкий уровень Т4 при нормальном показателе ТТГ, что было интерпретировано как проявления субклинического гипотиреоза, связанные с йоддефицитным состоянием детей в г. Астрахани. Вместе с тем, средний показатель Т3 у детей, испытавших внутриутробную интоксикацию ПАВ, был достоверно выше среднего уровня Т3 в контроле и у 14,0% детей превышал референтные значения. Ранее данный факт был отмечен у детей, употребляющих ПАВ, и может объясняться как токсическими изменениями в органах-мишенях синтеза гормона, так и изменениями в сторону активации ферментативной системы (монодейодиназы), участвующей в образовании Т3.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



