· Эффективность обезболивания определяется оценкой интенсивности боли до и после назначения каждого анальгетика или метода анальгезии.
· В хирургических ОРИТ и прочих подразделениях, где находятся пациенты с болью высокой интенсивности, оценка на начальном этапе лечения осуществляется каждые 15-30 минут, а затем, по мере снижения интенсивности, каждые 2 часа.
· В хирургических отделениях периодичность оценки интенсивности боли составляет 4-8 часов, что зависит как от выраженности боли, так и от эффективности обезболивания.
· При решении вопроса о необходимости обезболивания необходимо ориентироваться на критерии максимально допустимой интенсивности боли (пороги вмешательства). В частности, по 10-балльной визуально-рейтинговой шкале максимально допустима интенсивность боли 3 балла в покое и 4 балла при движениях (кашле).
· Внезапное усиление интенсивности боли, особенно связанное с появлением гипотензии, тахикардии, лихорадки, требует немедленной комплексной оценки состояния пациента, поскольку может быть связано с развитием хирургических осложнений, тромбоза глубоких вен и другой экстренной патологией.
· Интенсивность боли до и после лечения, неблагоприятные эффекты при проведении обезболивания должны быть четко зарегистрированы в доступных формах (дневник наблюдения и лист интенсивной терапии).
· Пациенты, с которыми затруднен вербальный контакт, требуют внимания при оценке боли. В эту категорию могут быть включены пациенты с нарушениями когнитивных функций, эмоционально лабильные пациенты, а также пациенты, чей уровень образования и степень культурного развития намного ниже среднего.
· Немедленное обезболивание проводиться пациентам при очевидной боли (без оценки боли), в том случае, когда больные из-за выраженного болевого синдрома не могут быть достаточно сосредоточены, чтобы оценить выраженность боли.
· В некоторых случаях родственники пациентов могут участвовать в оценке боли, при условии адекватного реагирования и сотрудничества.
Выбирая способ оценки боли необходимо убедиться в том, что:
· Он соответствует образовательному уровню пациента, его физическому, психическому и эмоциональному статусу
· Он отвечает как интересам пациента, так и потребностям специалистов, занимающихся обезболиванием
Для определения интенсивности боли используют специальные шкалы оценки боли. Использование какой-то одной шкалы в пределах одной клиники позволяет всему персоналу, занимающемуся обезболиванием, «говорить на одном языке». Самооценка боли пациентом является наиболее ценным инструментом. Во всех случаях необходимо в первую очередь прислушиваться к мнению пациента и доверять его ощущениям. Для определения интенсивности болевого синдрома используются как правило описательные характеристики боли, даваемые самим пациентом, так и различные шкалы: визуальная аналоговая, словесная рейтинговая и другие. [2, 3, 5, 7, 9, 10, 11, 14, 15, 16, 19, 23]
Различные варианты визуальной аналоговой шкалы (ВАШ) применяются в клинической практике с 80-х годов прошлого века. ВАШ представляет собой горизонтальную линию 10 см, концы которой соответствуют крайним степеням интенсивности боли – от «нет боли» до «нестерпимая боль». Пациент делает отметку на этом отрезке в точке, которая отражает интенсивность его боли.
Метод описательных определений заключается в том, что больному предлагаются определения боли: «лёгкая», «умеренная», «терпимая», «сильная», - до «нестерпимой». Пациент выбирает определение и подчёркивает его.
На рисунке 1 представлены различные варианты шкал самооценки боли. [5, 7, 9, 10, 11, 13, 14, 16, 23]
Рисунок 1
Выбор способа оценки боли
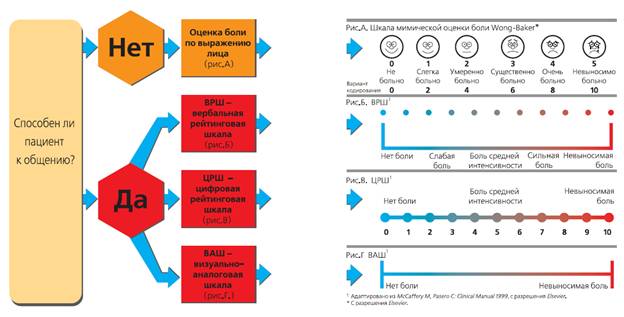
Рис. А. Оценка боли по выражению лица: пиктограмма шести лиц с различной мимикой, отражающей спектр ощущений от улыбки и хорошего настроения до страдания. Эта шкала может быть использована у пациентов, общение с которыми затруднено.
Рис. Б. Вербальная рейтинговая шкала (ВРШ): пациента просят оценить боль по одному из 5 критериев: «отсутствие боли, слабая, средняя, сильная, невыносимая боль».
Рис. В. Цифровая рейтинговая шкала (ЦРШ): представляет собой отрезок прямой с цифрами от 0 до 5 (или от 0 до 10), где 0 соответствует полному отсутствию боли, а 5 (или 10) – максимально возможной, невыносимой боли. Пациента просят оценить интенсивность боли соответствующей цифрой.
Рис. Г. Визуально-аналоговая шкала (ВАШ): представляет собой отрезок прямой длиной 100 мм, без делений и цифр, начало которого имеет обозначение «боли нет», а окончание – «невыносимая боль». Пациент делает отметку на этом отрезке в точке, которая отражает интенсивность его боли.
В рутинной клинической практике чаще используются шкалы ВРШ и ЦРШ, а ВАШ преимущественно применяется в исследовательских целях.
Для описательной характеристики боли, оценки ее силы и влияния на организм используют различные анкеты и опросники. Опросник МакГилла оценивает сенсорные, аффективные и моторно-мотивационные компоненты боли. Слова-дескрипторы отражают характер ощущений, интенсивность и продолжительность боли. В литературе сообщается о высокой информативности опросника, позволяющий уловить минимальные колебания уровня болевых реакций, что очень важно при подборе метода ведения и дозы анальгетика. К таким же опросникам можно отнести Дартмутскую болевую анкету.
По данным анкеты измеряется индекс интенсивности боли, число выбранных слов и общая интенсивность по шкале боли. Для удобства часто используют сокращенный вариант анкеты МакГилла (Melzack R., 1987;).
Словесная рейтинговая шкала позволяет адекватно оценить состояние больного, хорошо корреспондируется с результатами других измерений интенсивности боли, но слабо отражает персональные факторы, влияющие на формирование болевого синдрома. Часто сенсорные, аффективные и оценочные описания боли зависят от эмоционального состояния больного. Пациенты с хроническими болевыми синдромами для определения интенсивности боли. Пользуются несколькими словами. В таких случаях предлагается перекрестно-модальный подход в оценке боли, предусматривающий составление подробного ряда обозначений выраженности боли самим больным (Evans С J. et al., 2004;).
Для регистрации боли в течение ограниченного времени, например при клинических испытаниях нового лекарства или в послеоперационный период, полезной может быть специализированная компьютерная программа Pain Track. Пациент при помощи калибратора выбирает уровень, соответствующий его болевым ощущениям. Повторные оценки боли в течение нескольких дней дают диаграмму флюктуаций интенсивности боли, оцениваемую компьютером (Sto-ne А. А. et al., 2003; Cook AJ. et al., 2004; Aaron L.A. et al., 2004).
ВЕДЕНИЕ ДОКУМЕНТАЦИИ
Необходимо регулярно регистрировать интенсивность боли, изменения схемы обезболивания, эффективность анальгезии, побочные эффекты используемых препаратов и методов обезболивания. Вышеуказанные данные вносятся в отдельный раздел листа послеоперационного наблюдения или в специальную карту послеоперационного обезболивания.
A. Медсестра, ответственная за пациента, регистрирует интенсивность боли и проводит обезболивание в соответствии с принятыми национальными рекомендациями.
B. Врач, ответственный за пациента, при необходимости (недостаточная эффективность анальгезии) изменяет схему обезболивания.
C. В дальнейшем стратегия лечения боли определяется совместно врачом, ответственным за обезболивание, и палатными медсестрами.
D. Как врачи, так и медсестры уделяют особое внимание эффективности обезболивания, а также выявлению побочных эффектов используемых препаратов.
Таблица 6
Ориентировочный протокол оценки интенсивности
послеоперационной боли
Время | 10 | 13 | 16 | 19 | 22 | 01 | 05 |
(Покой/активизация) | П | А | А | П | П | А | С |
ВАШ | 2 | 6↓2 | 2 | 2 | 8↓3 | 3 |
Примечание. П - боль в покое; А - боль при активизации (кашель); ↓ - введение анальгетика; 6↓2 - интенсивность боли до и после введения анальгетика; С - пациент спит.
ИНФОРМИРОВАНИЕ ПАЦИЕНТОВ
Успех обезболивания во многом зависит от степени информированности пациентов и их веры в компетентность врача. В связи с этим целесообразно предоставить пациентам детальную информацию о послеоперационной боли и способах борьбы с ней. Подобная информация обычно включает:
· Сведения о важности лечения послеоперационной боли.
· Доступные методы послеоперационного обезболивания.
· Общепринятая практика оценки боли.
· Оптимальная оценка боли и адекватное обезболивание.
· Степень участия пациента в процессе обезболивания.
Информирование пациента и активное их участие в обезболивании является важной составляющей, которая не всегда выполняется в полном объеме. Для решения этой проблемы используются частные беседы, наглядная информация в виде брошюр, плакатов, ссылок на популярные интернет-сайты по обезболиванию.
До оперативного вмешательства в беседе с пациентами и его родственниками целесообразно обсудить следующие вопросы:
1. выбор метода анестезии и послеоперационного обезболивания;
2. выбор метода исследования боли и объяснение пациентам вариантов их использования;
3. план оценки интенсивности боли;
4. определение уровня боли по бальной оценке, выше которого будут рассматриваться варианты анальгезии;
5. важность сообщения об интенсивности боли, избегая преувеличения.
ЗАДАЧИ ПОСЛЕОПЕРАЦИОННОГО ОБЕЗБОЛИВАНИЯ
1. Повышение качества жизни пациентов в послеоперационном периоде.
2. Ускорение послеоперационной функциональной реабилитации.
3. Снижение частоты послеоперационных осложнений.
4. Ускорение выписки пациентов из клиники.
Нужно отметить, что в настоящее время в большинстве развитых стран неадекватное послеоперационное обезболивание рассматривается как нарушение прав человека.
СОВРЕМЕННЫЕ ВОЗМОЖНОСТИ
ЛЕЧЕНИЯ ПОСЛЕОПЕРАЦИОННОЙ БОЛИ
Предупреждение и лечение послеоперационной боли является одной из ключевых задач современной медицины. В большинстве развитых стран послеоперационное обезболивание осуществляется в соответствии с принятыми национальными и международными стандартами. Тем не менее в определенной степени можно руководствоваться международными рекомендациями, в частности "Acute Pain Management: Scientific Evidence" (2005), суммировавшими данные доказательной медицины об эффективности различных средств и методов послеоперационной анальгезии, а также руководством "Postoperative Pain Management - Good Clinical Practice" (2005), переведенным на русский язык.
В настоящее время во многих клиниках внедрена формулярная система использования лечебных препаратов тех или иных групп, целесообразность применения которых подтверждена данными доказательной медицины, а также обусловлена потребностями и особенностями конкретного лечебного учреждения. Многие авторы полагают, что все хирургические подразделения, а также отделения анестезиологии, реанимации и интенсивной терапии должны иметь в своем арсенале только те анальгетики и анестетики, эффективность и безопасность назначения которых подтверждена доказательствами I (систематизированные обзоры и метаанализы) и II (рандомизированные контролируемые исследования с определенными результатами) уровня (табл. 2).
Таблица 2.
Препараты, применение которых для послеоперационного обезболивания обосновано данными доказательной медицины
(Acute Pain Management: Scientific Evidence, 2-nd edition, 2005)
Группа | Препараты | Дозы, путь введения |
Неопиоидные анальгетики, НПВП | Диклофенак | 75 мг (150 мг суточная), в/м |
Неопиоидные анальгетики, прочие | Парацетамол (Перфалган®) | 1 г (4 г), в/в инфузия в течение 15 минут |
Опиоидные анальгетики, сильные | Морфин | 5-10 мг (50 мг), в/в, в/м |
Опиоидные анальгетики, слабые | Трамадол (Трамал®) | 100 мг (400 мг), в/в, в/м |
Адъювантные препараты | Кетамин | 0,15-0,25 мг/кг в/в |
Местные анестетики | Лидокаин 2% | (800 мг суточная)* |
*инфильтрация краев раны, интраплевральное введение, продленная блокада периферических нервов и сплетений, продленная эпидуральная анальгезия.
Мировой опыт послеоперационного обезболивания позволяет выделить следующие основные современные тенденции в его проведении:
1. Все более широкое применение неопиоидных анальгетиков – нестероидных противовоспалительных препаратов (НПВП) и парацетамола. В различных европейских клиниках частота назначения данных препаратов в качестве базиса послеоперационного обезболивания составляет от 45 до 99%.
2.Ограничение традиционного внутримышечного назначения опиоидных анальгетиков, что обусловлено низкой эффективностью и значительным количеством побочных эффектов данной методики.
3.Широкое применение высокотехнологичных методов обезболивания - продленной эпидуральной анальгезии посредством инфузии местных анестетиков, а также контролируемой пациентом внутривенной или эпидуральной анальгезии.
4.Мультимодальный характер послеоперационного обезболивания, т. е. одновременное назначение нескольких препаратов или методов обезболивания, способных воздействовать на различные механизмы формирования болевого синдрома. [2, 5, 7, 9, 11, 13, 14, 16, 19, 23, 25]
В настоящее время не существует идеального анальгетика или метода лечения острой послеоперационной боли. Максимально приближенное к решению проблемы адекватное обезболивание - это лечение послеоперационной боли, включающее множество факторов: хороший сестринский уход, сочетание нефармакологических и фармакологических методов, сбалансированная (мультимодальная) анальгезия с индивидуальным подбором безопасных средств разных уровней. Концепция мультимодальности предусматривает одновременное назначение двух и более анальгетиков и/или методов обезболивания, обладающих различными механизмами действия и позволяющих достичь адекватной анальгезии при минимальных побочных эффектах. [2, 5, 7, 9, 11, 13, 14, 16, 19, 23, 25]
Используемые в настоящее время методы послеоперационного обезболивания представлены в таблице 3.
Таблица 3
Методы послеоперационного обезболивания
1. Традиционное введение опиоидов: внутримышечные инъекции по требованию. 2. Опиоидные препараты агонисты/антагонисты: а) парентеральное введение опиоидов: внутривенно болюсно, длительная внутривенная инфузия, контролируемая пациентом анальгезия. б) непарентеральное введение опиоидов: щечное/подъязычное, пероральное, трансдермальное, назальное, ингаляционное, внутрисуставное 3. Методы регионарной анестезии: а) эпидуральное введение опиоидов; б) нестероидные противовоспалительные препараты; в) введение а2 - адренергических агонистов: - системное: - эпидуральное 4. Нефармакологические методы: - чрезкожная электростимуляция нервов; - психологические методы 5. Сочетанное использование представленных методов. |
Однако, говоря о методах лечения послеоперационной боли, нужно всегда помнить, что предотвращение ноцицептивной стимуляции, приводящей к развитию болевого синдрома гораздо проще и требует меньших медикаментозных затрат, нежели борьба с уже развившейся сильной болью. Так, ещё в 1996 году в Ванкувере метод предупреждающей анальгезии был признан перспективным направлением в патогенетической терапии болевых синдромов и широко используется прогрессивными клиниками в настоящее время. Для этих целей целесообразно использовать НПВП.
Опиоидная анальгезия и способы ее оптимизации
Традиционно системное введение опиоидных анальгетиков рассматривалось в качестве основы послеоперационного обезболивания как в отечественных, так и в зарубежных стационарах. В то же время данные препараты не являются "золотым стандартом" лечения острой боли. По оценкам зарубежных специалистов, эффективность обезболивания при традиционном назначении опиоидов в качестве монотерапии не превышает 25-30%.[2, 5, 13, 18, 23, 25]
Проблема заключается в том, что эффективная анальгетическая доза зачастую близка к той, которая вызывает депрессию дыхания.
Помимо депрессии дыхания увеличение дозы лимитировано увеличением частоты других побочных эффектов, таких как угнетение сознания, кожный зуд, тошнота и рвота, нарушение моторики ЖКТ, затруднение самостоятельного мочеиспускания в послеоперационном периоде.
Различия в свойствах разных опиоидов обусловлены их различными взаимоотношениями с рецепторами:
а) сродством к определенному типу рецепторов,
б) степенью связывания с рецептором (сила и продолжительность эффекта),
в) конкурентной способностью (антагонизмом) к определенному типу рецепторов.
В соответствии с этим, опиоиды могут быть агонистами или антагонистами тех или иных рецепторов, что и определяет присущий каждому опиоиду спектр свойств.
Группа опиатных анальгетиков насчитывает более 20 препаратов. Наиболее часто используемые препараты:
Морфин применяется обычно в дозе 10 мг в/м, действие его продолжается 3-5 часов. Максимальная доза для взрослых: разовая - 0,02г, суточная - 0,05г. Наиболее важные побочные эффекты это: угнетение дыхания, тошнота и рвота. Хотя морфин имеет ряд нежелательных побочных эффектов, он является отличным анальгетиком и принят в качестве «эталонного» препарата группы наркотических анальгетиков, в сравнении с которым оценивается действие всех остальных опиоидов.
Промедол применяется обычно в дозе 20 мг в/м, что вызывает 3-4-х часовую анальгезию. По анальгетической активности он в 3-5 раз слабее морфина, но значительно менее токсичен, в меньшей степени угнетает дыхательный центр, реже вызывает рвоту. В клинических дозировках не оказывает негативного воздействия на организм матери и плода.
Омнопон представляет собой смесь гидрохлоридов алкалоидов опия, где на долю морфина приходится около 50%, применяется в дозе 20 мг. Максимальная доза для взрослых: разовая - 0,03 г суточная - 0,1 г. Обладает меньшей анальгетической активностью, чем морфин и промедол, что обусловливает его меньшую популярность.
Трамадола гидрохлорид - анальгетик, опосредующий обезболивающий эффект как через m-опиоидные рецепторы, так и путем ингибирования норадренергического и серотонинергического механизма передачи болевой импульсации. Трамадол характеризуется сравнительно высокой биодоступностью - 60-70 % при разных способах введения, быстрым и длительным болеутоляющим эффектом. Существенное преимущество трамадола по сравнению с другими опиоидными анальгетиками крайне низкая степень привыкания и минимальный наркогенный потенциал этого препарата. В отличие от других опиоидов, в эквианальгетических дозах трамадол не вызывает запора, не угнетает кровообращения и дыхания. Из возможных побочных эффектов следует отметить развитие тошноты, головокружения, в редких случаях рвоты. Помимо применения трамадола в качестве анальгетика, с 1989 г. он используется для купирования мышечного тремора в раннем послеоперационном периоде.
Наиболее эффективные попытки улучшения качества послеоперационной опиоидной аналгезии основаны на оптимизации способов введения препаратов.
Способы введения препаратов:
1.Внутримышечное введение. Плюсы этого традиционного способа анальгезии: легкость применения, дешевизна метода, а также постепенное развитие побочных эффектов, что дает больше возможностей борьбы с ними. Однако эта методика часто приводит к неадекватному обезболиванию (более 60% пациентов отмечают неудовлетворительное качество послеоперационной анальгезии). Причины этого кроются в том, что вводятся фиксированные дозы, без учета фармакологической вариабельности; часто инъекции опиоидов производятся с большими перерывами, то есть тогда, когда уже произошел «прорыв» боли. Немаловажным моментом является также то, что при внутримышечном пути введения начало обезболивания - замедленное.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



