Уменьшение концентрации ионов может произойти в результате:
а) образования малорастворимого вещества:
AgNO3 + NaCl = AgCl↓ + NaNO3 (молекулярное уравнение)
Ag+ + NO3 – + Na+ + Cl – = AgCl↓ + Na+ + NO3 – (полное ионное уравнение).
Исключив ионы, не взаимодействующие между собой, получаем сокращенное ионное уравнение
Ag+ + Cl – = AgCl↓;
б) образования газообразного вещества, уходящего из раствора:
![]() CO2↑
CO2↑
![]() Na2CO3 + H2SO4 = Na2SO4 + H2CO3
Na2CO3 + H2SO4 = Na2SO4 + H2CO3
H2O
2Na+ + CO32 – + 2H+ + SO42 – = 2Na+ + SO42 – + H2O + CO2↑
CO32 – + 2H+ = H2O + CO2↑
в) образования растворимого, но малодиссоциированного вещества, например, воды, слабой кислоты или слабого основания:
NaOH + HCl = NaCl + H2O
Na+ + OH – + H+ + Cl – = Na+ + Cl – + H2O
OH – + H+ = H2O
CH3COONa + H2SO4 = Na2SO4 + CH3COOH
CH3COO – + Na+ = 2Na+ + SO42 – + CH3COOH
CH3COO – + H+ = CH3COOH;
г) образования из нескольких простых ионов сложного комплексного иона:
HgI2 + 2KI = K2[HgI4]
Hg2+ + 2I – + 2K+ + 2I – = 2K+ + [HgI4]2 –
Hg2+ + 4I – = [HgI4]2 –
7. Произведение растворимости
Абсолютно нерастворимых веществ нет. Твердые вещества отличаются своей растворимостью. Очевидно, что труднорастворимый электролит легко образует насыщенный раствор. Рассмотрим равновесия, наблюдаемые в насыщенном растворе какого-нибудь труднорастворимого вещества, например, CaSO4. В этой системе осадок находится в равновесии с насыщенным раствором этого вещества:
СaSO4 ![]() Ca2+ + SO42–
Ca2+ + SO42–
осадок раствор
Константа равновесия для процесса растворения осадка имеет следующий вид:
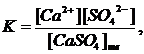
откуда K∙[CaSO4]тв = [Ca2+]∙[SO42-].
Концентрация твердого вещества есть величина постоянная:
[CaSO4]тв = const.
Учитывая это, K∙[CaSO4]тв как произведение двух постоянных величин также можно считать величиной постоянной, некоторой константой, характерной для данного вещества. Эту константу называют произведением растворимости. Её обозначают через ПР:
![]() .
.
Для насыщенного раствора сульфата кальция произведение растворимости при 25оС найдено равным 3,72∙10-5 г-ион2/л2.
Таким образом, ПР – это произведение концентраций ионов малорастворимого сильного электролита, содержащихся в свободном виде в его насыщенном растворе. Величина ПР означает, что в насыщенном растворе труднорастворимого электролита произведение концентраций его ионов есть величина постоянная (при данной температуре).
Произведение растворимости характеризует растворимость электролитов. Растворимость численно равна ![]() (для бинарных электролитов).
(для бинарных электролитов).
В общем случае для труднорастворимого электролита состава AnBm в растворе наблюдается равновесие:
AnBm = nAa+ + mBb–.
Тогда
ПР = [Aa+]n [Вb–]m
Сравнивая значения произведений растворимости труднорастворимых солей, можно видеть, какая из них растворяется лучше (приложение, табл. 3).
Из величины ПР вытекает условие образования и растворения осадка:
1. Если [Aa+]n [Вb–]m = ПР, то осадок находится в равновесии с раствором.
2. Если [Aa+]n [Вb–]m > ПР, то осадок выпадает.
3. Если [Aa+]n [Вb–]m < ПР, то осадок растворяется.
Таким образом, если при той или иной химической реакции произведение концентраций участвующих в ней ионов станет больше произведения растворимости, то выпадает осадок труднорастворимого вещества. И обратно, если произведение концентраций ионов данного электролита в насыщенном его растворе в результате той или иной реакции становится меньше произведения растворимости для ионов этого электролита, то осадок переходит в раствор.
8. Ионное произведение воды и водородный показатель
Измерение электропроводности химически чистой воды показало, что она обладает незначительной электропроводностью, т. е. в очень малой степени находится в диссоциированном состоянии (слабый электролит).
H2O H++OH –
H++OH –
К её диссоциации можно применять закон действующих масс
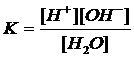 .
.
Константу диссоциации можно вычислить по данным электропроводности. При 22оС она равна 1,8∙10-16, а степень диссоциации 2,9∙10-9, т. е. из молекул воды диссоциирует только одна. При такой ничтожно малой диссоциации концентрацию недиссоциированных молекул воды H2O можно полагать равной концентрации общего количества воды, считать величиной постоянной и включить в константу диссоциации
![]()
т. е. произведение концентраций ионов водорода и гидроксильной группы в любом водном растворе есть величина постоянная (при данной температуре) и называется ионным произведением воды. Можно вычислить ![]()
Концентрация как недиссоциированных, так и исходных молекул воды ![]() моль/литр. Подставив эту величину в выражение для ионного произведения воды, получим
моль/литр. Подставив эту величину в выражение для ионного произведения воды, получим
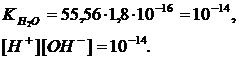
Как было отмечено, степень диссоциации воды повышается с повышением температуры. Поэтому с повышением температуры увеличивается концентрация [H+] и [OH–] ионов и величина ионного произведения; так, при 100 оС [H+][OH–] = 59∙10-14 , при 0 оС [H+][OH–] = 0,139∙10-14.
В воде и в любом водном растворе содержатся [H+]- и [ОН-]-ионы, их относительной концентрацией определяется реакция среды – кислая, щелочная или нейтральная.
В нейтральных растворах и в чистой воде (при 22оС)
![]() .
.
Эта величина концентрации водородных ионов соответствует нейтральной реакции среды.
В кислых растворах равновесие Н2О![]() H+ + OH– смещено влево, в сторону моляризации избытка одноименных Н+-ионов, но ионное произведение воды – величина при данной температуре постоянная, в любой среде (кислой, щелочной, нейтральной) также сохраняется его значение
H+ + OH– смещено влево, в сторону моляризации избытка одноименных Н+-ионов, но ионное произведение воды – величина при данной температуре постоянная, в любой среде (кислой, щелочной, нейтральной) также сохраняется его значение 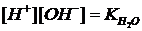 . Но при этом [H+]>[OH-]. Величина концентрации Н+-ионов обусловливает кислую реакцию среды [H+]>10-7 г-ион/л.
. Но при этом [H+]>[OH-]. Величина концентрации Н+-ионов обусловливает кислую реакцию среды [H+]>10-7 г-ион/л.
В щелочных растворах равновесие диссоциации воды также смещено влево от избытка одноименных ОН–-ионов; величина ионного произведения воды также сохраняется, причем [H+]<[OH-]; причиной щелочной реакции среды может быть концентрация ОН–-ионов (>10-7) или также концентрация Н+-ионов (<10-7) согласно 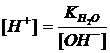 . Таким образом, концентрация Н+-ионов может быть использована для характеристики любой реакции среды. Характеристика реакции среды обычно выражается очень малыми величинами с отрицательными показателями степени. Для большего удобства принято пользоваться отрицательным значением логарифма величины [H+], который назван водородным показателем, обозначается рН:
. Таким образом, концентрация Н+-ионов может быть использована для характеристики любой реакции среды. Характеристика реакции среды обычно выражается очень малыми величинами с отрицательными показателями степени. Для большего удобства принято пользоваться отрицательным значением логарифма величины [H+], который назван водородным показателем, обозначается рН:
рН = –lg [H+] [H+] = 10–pH
Если реакция среды нейтральная, то [H+]=10–7, а рН=7.
Если реакция кислая, то [H+]>10–7, а рН<7.
Если среда щелочная, то [H+]<10–7, а рН>7.
Ввиду большого практического значения величины рН среды разработано много методов его непосредственного определения. В настоящее время применяют колориметрический метод (по окрашиванию), основанный на изменении окраски индикаторов, а также электрометрические методы с помощью специальных приборов рН-метров.
9. Индикаторы
Вещества, изменяющие окраску при изменении реакции среды, - индикаторы – чаще всего сложные органические соединения – слабые кислоты или слабые основания. Схематично состав индикаторов можно выразить формулами НInd или IndOH, где Ind – сложный органический анион или катион индикатора.
Принцип применения индикаторов основан на том, что недиссоциированные молекулы индикатора и его Ind–ионы имеют в растворе разную окраску, и окраска раствора изменяется в зависимости от пложения равновесия диссоциации индикатора. Например, фенолфталеин (кислотный индикатор) имеет молекулы бесцветные, а анионы малиновые; метилоранж (основной индикатор) – желтые молекулы и красные катионы.
фенолфталеин метилоранж
HInd H+ + Ind– IndOH
H+ + Ind– IndOH![]() Ind+ + OH–
Ind+ + OH–
бесцв. малинов. желт. красн.
Индикаторы, как слабые электролиты, имеют малые величины констант диссоциации. Например, Кд фенолфталеина равна 2∙10-10 и в нейтральных средах он находится преимущественно в виде своих молекул вследствие очень малой концентрации ионов, почему и остается бесцветным. При добавлении щелочи Н+-ионы фенолфталеина связываются, «стягиваются» с ОН–-ионами щелочи, образуя молекулы воды, и положение равновесия диссоциации индикатора смещается вправо – в сторону увеличения концентрации Ind–-ионов, появляется малиновое окрашивание. При добавлении в этот же раствор кислоты одновременно с нейтрализацией щелочи – при достаточной концентрации Н+-ионов – положение равновесия диссоциации индикатора смещается влево, в сторону моляризации, раствор снова обесцвечивается. Аналогично происходит изменение окраски метилоранжа: желтая в нейтральной среде переходит в красную в кислой среде при добавлении H+-ионов и снова в желтую при добавлении OH–-ионов.
Таким образом, окраска индикаторов зависит от рН-среды.
Раствор, содержащий индикатор, непрерывно изменяет свою окраску при изменении рН. Человеческий глаз, однако, не очень чувствителен к таким изменениям. Диапазон, в котором наблюдается изменение окраски индикатора, определяется физиологическими пределами восприятия цвета человеческим глазом. При нормальном зрении глаз способен различить присутствие одной окраски в смеси ее с другой окраской только при наличии как минимум некоторой пороговой плотности первой окраски: изменение окраски индикатора воспринимается только в той области, где имеется 5-10-кратный избыток одной формы по отношению к другой. Рассматривая в качестве примера HInd и характеризуя состояние равновесия
HInd H+ + Ind–
H+ + Ind–
соответствующей константой
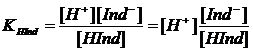 ,
,
можно написать, что индикатор проявляет свою чисто кислотную окраску, обычно улавливаемую наблюдателем, при
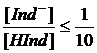 ,
,
а чисто щелочную окраску при
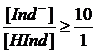 .
.
Внутри интервала, определяемого этими величинами, проявляется смешанная окраска индикатора.
Таким образом, глаз наблюдателя различает изменение окраски лишь при изменении реакции среды в интервале около 2-х единиц рН. Например, у фенолфталеина этот интервал рН от 8,2 до 10,5: при рН=8,2 глаз наблюдает начало появления розовой окраски, которая все усиливается до значения рН=10,5, а при рН=10,5 усиление красной окраски уже незаметно. Этот интервал значений рН, в котором глаз различает изменение окраски индикатора, называют интервалом перехода окраски индикатора.
Указанный диапазон рН величиной приблизительно в 2 единицы для различных индикаторов не приходится на одну и ту же область шкалы рН, так как его положение зависит от конкретного значения константы диссоциации каждого индикатора. В табл.4 приложения приведены интервалы перехода и цвета наиболее распространенных кислотно-основных индикаторов.
ЛАБОРАТОРНЫЕ РАБОТЫ ПО ТЕМЕ
«РАСТВОРЫ ЭЛЕКТРОЛИТОВ»
Лабораторная работа № 1. Сильные и слабые электролиты
Опыт 1. Окраска индикаторов в различных средах.
В одну пробирку налейте 5-6 капель 2 н. H2SO4, в другую – такой же объем 2 н. NaOH, в третью – такой же объем дистиллированной воды. Во все три пробирки добавьте по 1 капле раствора фенолфталеина. Отметьте цвет раствора в каждой пробирке. Аналогичный опыт проделайте с индикатором метиловым оранжевым. Результаты наблюдений занесите в таблицу:
Индикатор | Среда | ||
кислая | нейтральная | щелочная | |
Фенолфталеин | |||
Метиловый оранжевый |
Опыт 2. Определение pH растворов кислот
HCl, H2SO4, CH3COOH
На часовое стекло положить полоски универсального индикатора, нанести на них 1-2 капли испытуемого раствора и тотчас же сравнить окраску бумаги со шкалой универсального индикатора. Сделать выводы о силе электролитов. Записать уравнения диссоциации.
Опыт 3. Определение рН растворов оснований
NaOH, Ca(OH)2, NH4OH
На часовое стекло положить полоски универсального индикатора, нанести на них 1-2 капли испытуемого раствора и тотчас же сравнить окраску бумаги со шкалой универсального индикатора. Сделать выводы о силе электролитов. Записать уравнения диссоциации.
Лабораторная работа № 2. Смещение ионного равновесия. Ионные реакции с образованием слабого электролита
Опыт 1. Налейте в две пробирки по 5-6 капель 0,1 н. раствора гидроксида аммония и по 1-2 капли раствора фенолфталеина. Затем в одну из пробирок бросьте 1 кристалл хлорида аммония. Пробирку встряхните несколько раз. Наблюдайте ослабление интенсивности окраски раствора.
Гидроксид аммония – слабый электролит. В его растворе имеет место равновесие: NH4OH ↔ NH4++OH–. Ионы ОН– и обусловливают окраску фенолфталеина. Добавление NH4Cl, который диссоциирует на ионы NH4+ и Cl–, значительно увеличивает концентрацию ионов NH4+ в растворе. А это нарушает равновесие между молекулами NH4OH и ионами NH4+ и OH–, смещая его влево, т. е. ионы NH4+ и OH– соединяются и образуют недиссоциированные молекулы NH4OH. В результате концентрация ионов ОН– в растворе очень сильно понижается и окраска раствора бледнеет.
Опыт 2. Налейте в две пробирки по 5-6 капель 0,1 н. раствора уксусной (CH3COOH) кислоты и по 1-2 капли раствора метилового оранжевого. Затем в одну из пробирок введите 2-3 кристаллика ацетата натрия (CH3COONa). Пробирку встряхните несколько раз. Сравните интенсивность окраски в пробирках. Объясните причину изменения окраски раствора.
Опыт 3. Ионные реакции с образованием слабого электролита
а) Положите в пробирку несколько кристаллов хлорида аммония (NH4Cl) и прилейте раствор гидроксида натрия (NaOH). Определите выделяющийся газ по запаху, слегка нагрев пробирку.
б) Опустите в пробирку несколько кристаллов ацетата натрия (CH3COONa) и прилейте разбавленную серную кислоту. Напишите уравнение реакции.
Лабораторная работа № 3. Произведение растворимости
Опыт 1.Ионные реакции с образованием осадков
а) Налейте в три пробирки по 2-3 капли раствора хлорида бария (BaCl2) и добавьте в одну из них несколько капель раствора сульфата натрия (Na2SO4), в другую – раствора серной кислоты, в третью – раствора сульфата алюминия (Al2(SO4)3). Наблюдайте появление одинакового осадка. Составьте уравнения реакций. Что можно сказать о сущности реакций в проделанном опыте?
б) Налейте в одну пробирку 2-3 капли сульфата железа (FeSO4) (II)? а во вторую – такой же объем раствора сульфата меди (CuSO4) (II). Прилейте в обе пробирки по 3-4 капли раствора сульфида натрия (Na2S). Составьте уравнения реакций. Слейте растворы, а осадки сохраните для следующих опытов.
Опыт 2. Образование осадков и произведение растворимости
В две пробирки налейте по 3-4 капли 0,005 М раствора нитрата свинца (Pb(NO3)2). В одну из них прибавьте такой же объем 0,05 М раствора хлорида калия (KCl), а в другую – такой же объём 0,05 М раствора иодида калия (KI). В какой из пробирок выпал осадок? Объясните полученный результат, используя значения произведений растворимости. Составьте уравнения реакций.
Опыт 3. Растворение осадков и произведение растворимости
К осадкам FeS и CuS, полученным в опыте 1.б). Прилейте немного 2 н. раствора соляной кислоты. Какой из осадков растворился? Составьте уравнение реакции. Объясните различие в растворимости осадков, используя значения произведений растворимости.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
1. Слабые электролиты
Примеры решения задач
Задача 1.1. Степень диссоциации уксусной кислоты в 0,1 М растворе равна 1,32∙10–2. Найти константу диссоциации кислоты и значение рК.
Решение. Подставим данные задачи в уравнение закона разбавления Оствальда
К = α2CM/(1–α) = 1,77∙10–5 pK = - lg K = 4,75
Задача 1.2. Вычислить концентрацию ионов водорода в 0,1 М растворе хлорноватистой кислоты HClO (K=5∙10-8).
Решение: Найдем степень диссоциации HClO
![]() . Отсюда [H+] = α∙CM = 7∙10–5 моль.
. Отсюда [H+] = α∙CM = 7∙10–5 моль.
Задачу можно решить и другим способом, используя соотношение
![]() тогда [H+] = 7∙10–5 моль/л.
тогда [H+] = 7∙10–5 моль/л.
Задача 1.3. Во сколько раз уменьшится концентрация ионов водорода в 0,2 М растворе HCOOH (K = 0,8∙10–4), если к 1 л этого раствора добавить 0,1 моль HCOONa? Считать, что соль полностью диссоциирована.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



