Федеральное агентство по образованию
Государственное образовательное учреждение высшего
«УФИМСКИЙ ГОСУДАРСТВЕННЫЙ НЕФТЯНОЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
Кафедра общей и аналитической химии
Учебно-методическое пособие
к лабораторным работам по теме
«РАСТВОРЫ ЭЛЕКТРОЛИТОВ»
УФА 2005
В учебно-методическом пособии подробно рассмотрены основные положения теории электролитической диссоциации: механизм диссоциации сильных и слабых электролитов, понятие степени диссоциации, активности, ионной силы раствора, условия протекания ионно-обменных реакций, равновесие в растворах труднорастворимых электролитов, ионное произведение воды, рН раствора, кислотно-основные индикаторы. Приведены примеры решения задач и варианты домашних заданий, а также лабораторные работы по данной теме.
Составители: , доц., канд. хим. наук,
, проф., д-р. хим. наук,
, проф., канд. хим. наук,
, доц., канд. хим. наук.
Рецензент , доц., канд. хим. наук.
© Уфимский государственный
нефтяной технический университет, 2005
1. Основные положения теории электролитической диссоциации Сванте Аррениуса
Электролиты – вещества, водные растворы и расплавы которых проводят электрический ток. Эти вещества имеют ионную и ковалентную сильнополярную связи. Электролитами являются кислоты, основания, соли. Поведение электролитов в растворе объясняет теория электролитической диссоциации, сформулированная Сванте Аррениусом в 1887 году:
Вещества, растворы которых являются электролитами, при растворении распадаются на частицы (ионы), несущие положительные и отрицательные заряды.
Процесс распада электролита на ионы называется электролитической диссоциацией. Под действием электрического напряжения положительно заряженные ионы двигаются к катоду, а отрицательно заряженные – к аноду.
Ионы, заряженные положительно, называются катионами, а отрица-тельно заряженные ионы – анионами. Катионами являются положительно заряженные ионы металлов, ион водорода, NH4+, анионы –кислотные остатки и гидроксид-ион. Величина заряда иона совпадает с валентностью атома или кислотного остатка, а количество положительных зарядов равно количеству отрицательных. Поэтому раствор в целом электронейтрален. Процесс электролитической диссоциации изображается следующим образом:
NaCl ↔ Na+ + Cl‾
H2SO4 ↔ 2H+ + SO42–
Теория Аррениуса объяснила многие явления, связанные со свойствами растворов электролитов, но не ответила на вопрос: почему одни вещества являются электролитами, а другие – нет, а также какую роль в образовании ионов играет растворитель.
2. Механизм диссоциации
Теорию процесса диссоциации разработал (1891).
Представим себе, что ионный кристалл, например NaCl, внесен в воду. Каждый ион, находящийся на поверхности кристалла, образует вокруг себя электрическое поле. Вблизи от Na+ создается поле положительного знака, вблизи Cl– дается электростатическое поле отрицательного знака. Влияние этих полей распространяется на некоторое расстояние от кристалла. В растворе кристалл со всех сторон окружают беспорядочно движущиеся молекулы воды. Попадая в поле действия электрических заряженных ионов, они изменяют свое движение: в непосредственной близости от кристалла они ориентируются таким образом, что к отрицательно заряженному иону Cl– диполи воды оказываются направленными положительно заряженным полюсом, а к положительно заряженному иону Na+– отрицательно заряженным полюсом (рис. 1). Такое явление называется ориентацией полярных молекул в электростатическом поле. Между ионами и диполями воды действуют кулоновские силы притяжения. В результате ион-дипольного взаимодействия выделяется энергия, которая способствует разрыву ионных связей в кристалле и переведению иона из кристалла в раствор. Отделенные друг от друга ионы тотчас же после разрыва связи между ними вплотную окружаются полярными молекулами воды и становятся полностью гидратированными. Явление взаимодействия ионов с молекулами воды, в результате чего происходит образование гидратной оболочки, называется гидратацией ионов.
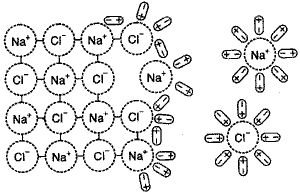
Рис. 1. Диссоциация ионных соединений
Гидратированные ионы, имеющие противоположные заряды, могут взаимодействовать друг с другом. Но так как ионы движутся в растворе вместе с гидратными оболочками, то сила их взаимодействия значительно уменьшена, и они способны к самостоятельному существованию.
При растворении полярных соединений происходит ориентация диполей воды вокруг растворенных молекул, вызывая еще большую поляризацию их. Полярная ковалентная связь между атомами переходит в ионную. Общая электронная пара сдвигается к одному из атомов (рис. 2).
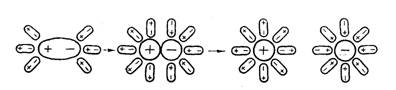
Рис. 2. Диссоциация молекул с полярной ковалентной связью
Например, в HCl электронная пара сдвигается к атому хлора, который превращается в гидратированный ион хлора, и протон с молекулой воды образует сложную положительно заряженную частицу H3O+ – ион гидроксония.
HCl + xH2O ↔ H3O+ + Cl–∙yH2O
Таким образом, электролитами могут быть соединения только с ионной или полярной ковалентной связью. Электролиты могут диссоциировать только в полярных растворителях.
3. Диссоциация солей, оснований и кислот
Характер ионов, образующихся при диссоциации разных электролитов, должен быть различен. В молекулах солей диссоциация всегда идет с образованием положительных ионов металла и отрицательно заряженных ионов кислотного остатка.
Соли могут быть определены как соединения, дающие в водном растворе ионы металла и кислотного остатка
KNO3 ↔ K+ + NO3–; Na2SO4 ↔ 2Na+ + SO42–;
MgCl2 ↔ Mg2+ + 2Cl–; MgSO4 ↔ Mg2+ + SO42–
При растворении кислых солей в растворе образуются катионы металла и сложные анионы кислотного остатка, а также ионы, являющиеся продуктами диссоциации этого сложного кислотного остатка, в том числе H+.
Например:
NaHCO3 ↔ Na+ + HCO3–; HCO3– ↔ H+ + CO32–
При диссоциации основных солей образуются анионы кислотного остатка и сложные катионы, состоящие из металла и гидроксогрупп. Эти сложные катионы также способны к диссоциации. Поэтому в растворе основной соли присутствуют OH–:
MgOHCl ↔ MgOH+ + Cl–; MgOH+ ↔ Mg2+ + OH–
Основания можно определить как соединения, дающие в водном растворе анионы гидроксила и катионы металла:
NaOH ↔ Na+ + OH–; Ba(OH)2 ↔ Ba2+ + 2 OH–
Кислотами называются соединения, дающие в водных растворах ионы водорода (точнее ионы гидроксония) и анионы кислотного остатка
HNO3 ↔ H+ + NO3–; H2SO4 ↔ 2H+ + SO4–
Характер электролитической диссоциации той или иной молекулы в значительной степени определяется полярностями ее валентных связей. Полярность связи водорода с кислородом в соединениях типа ROH существенно меняется в зависимости от химической природы радикала R. Если радикал характеризуется сильно выраженными металлическими свойствами, связь между ним и О резко полярна, связь же О−Н в этом случае малополярна. Наоборот, если R обладает резко выраженными неметаллическими свойствами, связи между ним и О малополярна, связь же О−Н резко полярна.
Таким образом, диссоциация соединений типа ROH может происходить по двум направлениям:

![]()

![]()

![]() R O H
R O H
Некоторые соединения, способные при одних и тех же условиях отщеплять и ионы водорода и ионы гидроксила, называются амфотерными. К амфотерным электролитам относятся Zn(OH)2, Al(OH)3, Cr(OH)3 и др.
Простейшим амфотерным соединением является вода, дающая при диссоциации ионы H+ и OH-. Однако диссоциация воды настолько мала, что концентрация H+ и ОН - в чистой воде равна 10-7 г-ион/л. Опыт показывает, что содержание ионов в воде с течением времени не изменяется. Следовательно, наряду с процессом распада (диссоциации) имеет место и обратный – образование из ионов недиссоциированных молекул (моляризация). Таким образом, электролитическая диссоциация есть процесс обратимый.
4. Степень диссоциации электролита. Закон разбавления Оствальда
Количественную характеристику равновесного состояния электролита дает его степень диссоциации (a), т. е. отношение числа молекул, распавшихся на ионы, к общему числу растворенных молекул.
a = n / N
a измеряется в % (долях). N – общее число молекул в растворе, n – число диссоциированных молекул.
Степень диссоциации электролита зависит от ряда факторов, среди которых:
· природа электролита;
· природа растворителя;
· температура;
· концентрация раствора;
· присутствие одноименных ионов.
Природа электролита – главный фактор, определяющий степень диссоциации. Чем более полярной является химическая связь между атомами или группами атомов в молекуле, тем сильнее растворитель с высоким значением диэлектрической проницаемости препятствует электростатическому взаимодействию ионов противоположного знака в растворе, тем больше степень диссоциации.
Природа растворителя также оказывает существенное влияние на степень диссоциации растворённого вещества. Степень диссоциации в значительной мере зависит от диэлектрической проницаемости растворителя. Диэлектрическая проницаемость (ξ) показывает, во сколько раз сила взаимодействия между двумя зарядами в данной среде меньше, чем в вакууме. Чем больше диэлектрическая проницаемость среды, тем больше степень электролитической диссоциации. Самое высокое значение ξ=81 имеет вода. Замена воды на растворитель с меньшей диэлектрической проницаемостью, например, на этиловый спирт (ξ=25), сильно понижает степень диcсоциации. Сильные электролиты в спирте становятся электролитами средней силы, а слабые – практически не диссоциируют.
В общем случае степень электролитической диссоциации сложным образом зависит от температуры. Для многих электролитов существует достаточно широкий температурный интервал, в котором наблюдается простая зависимость между тепловым эффектом, степенью диссоциации и температурой. Если процесс диссоциации экзотермичен, то с повышением температуры степень диссоциации падает. При эндотермическом процессе – повышение температуры ведёт к увеличению степени диссоциации. Так, степень диссоциации воды растёт с увеличением температуры. При 18 °С степень диссоциации воды равна 1,5∙10–9, а при 100 °С – 1,5∙10–8. Для каждого электролита существуют температурные условия, в которых он диcсоциирует в большей степени. Так, степень диссоциации уксусной кислоты максимальна при 25 °С (Кд = 1,75∙10–5). Выше и ниже этой температуры степень диссоциации уксусной кислоты меньше ( при 0 °С Кд = 1,65∙10–5, а при 50 °С Кд = 1,62∙10–5). Отсутствие чёткой зависимости степени диссоциации от температуры объясняется неравномерным изменением энтальпии гидратации, состава ионов, свойств растворителя и других с изменением температуры.
Изменение концентрации раствора будет различно отражаться на процессах диссоциации и моляризации. Степень диссоциации электролита при разбавлении раствора увеличивается.
Все электролиты в зависимости от степени диссоциации делятся на сильные, средней силы и слабые. Электролиты, диссоциированные при указанных условиях на 30 % и больше, называют сильными; диссоциированные на 5÷30%, – электролитами средней силы, еще менее диссоциированные - слабыми электролитами.
Все соли являются сильными электролитами. К сильным электролитам принадлежат следующие кислоты: HNO3, HClO4, HClO3, H2SO4, HCl, HBr, HI, HMnO4. К слабым кислотам относятся все органические кислоты, а также H2CO3, H2S, HCN, H2SiO3 и некоторые другие. К сильным основаниям относятся KOH, NaOH, Ca(OH)2, Ba(OH)2. К слабым основаниям принадлежат NH4OH, Al(OH)3, Zn(OH)2, Mg(OH)2, Cu(OH)2 и др.
В растворах слабых электролитов процесс диссоциации молекул на ионы обратим. Поэтому к ним, как к равновесным системам, приложим закон действия масс. Например, для диссоциации уксусной кислоты в водном растворе CH3COOH ![]() H++CH3COO–. Константа равновесия
H++CH3COO–. Константа равновесия
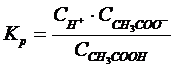 называется константой диссоциации (Кд).
называется константой диссоциации (Кд).
Чем меньше Кд, тем слабее электролит проявляет способность к диссоциации. Если молекула слабого электролита может диссоциировать на два и на большее число ионов, то диссоциация проходит по стадиям (ступенчатая диссоциация). При этом каждая стадия характеризуется своей константой диссоциации. Например, H3PO4 диссоциирует по уравнениям
H3PO4 ↔ H+ + H2PO4– K1
H2PO4– ↔ H+ + HPO42– K2
HPO42– ↔ H+ + PO43– K3
Значение констант изменяется в ряду К1 > К2 > К3. Это положение имеет общее значение, т. к. отщепление второго и третьего ионов водорода требует большей энергии (приложение, табл. 1).
Константа полной диссоциации слабого электролита равна произведению констант его диссоциации по ступеням.
Например, для H2CO3
Kд = K1K2 = 4,7∙10–11∙ 4,5∙10-7 = 2,1∙10-17
Константа диссоциации слабого электролита связана со степенью диссоциации. Обозначим: С – исходная концентрация электролита, α – степень диссоциации. Тогда концентрация ионов в состоянии равновесия для бинарного электролита Сα. Концентрация недиссоциированных молекул будет
(С – С∙α) = С (1–α).
Константу диссоциации для уксусной кислоты можно представить следующим образом:
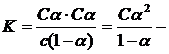 закон разведения Оствальда.
закон разведения Оствальда.
В слабых электролитах величина α << 1. Поэтому значением α можно пренебречь и величину (1-α) принять равной 1. Тогда K=Cα2, 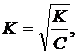 т. е. степень диссоциации слабых электролитов обратно пропорциональна квадратному корню из концентрации.
т. е. степень диссоциации слабых электролитов обратно пропорциональна квадратному корню из концентрации.
Таким образом, закон разбавления Оствальда формулируется следующим образом: степень диссоциации электролита при разбавлении раствора увеличивается.
При прибавлении в раствор слабой кислоты или основания соли, содержащей одноимённый анион или катион для кислоты или основания соответственно, то согласно принципу Ле-Шателье, следует ожидать смещения равновесия диссоциации влево, т. е. в сторону уменьшения степени диссоциации. Так, если к раствору уксусной кислоты добавить немного ацетата натрия, то добавленные ацетат-ионы смещают равновесие диссоциации кислоты
СН3СООН ↔ CH3COO – + H+
влево и степень диссоциации уксусной кислоты уменьшается. Об этом свидетельствуют приведенные ниже данные:
[СН3СООNa], моль/л 0,0 0,001 0,002 0,005 0,010 0,020
α СН3СООН, % 4,1 1,5 0,84 0,35 0,18 0,09
Подавление диссоциации под влиянием одноимённого иона называется “репрессией ионизации”. С репрессией ионизации связаны многие процессы, имеющие практическое значение. Так, её используют для уменьшения растворимости тех или иных соединений.
5. Растворы сильных электролитов
В водных растворах сильные электролиты обычно полностью диссоциированы. В несильно разбавленных растворах сильных электролитов среднее расстояние между ионами вследствие значительной концентрации мало. В таких растворах ионы не вполне свободны, движение их стеснено взаимным притяжением друг другу.
Вследствие этого притяжения каждый ион как бы окружен шарообразным роем противоположно заряженных ионов, получившим название «ионной атмосферы».
В отсутствие внешнего электрического поля ионная атмосфера симметрична и силы, действующие на центральный ион, взаимно уравновешиваются. Если же приложить к раствору постоянное электрическое поле, то разноименно заряженные ионы будут перемещаться в противоположных направлениях. При этом каждый ион стремится двигаться в одну сторону, а окружающая его ионная атмосфера – в противоположную, вследствие чего уменьшается сила тока.
Чем больше концентрация раствора, тем сильнее проявляется тормозящее действие ионной атмосферы на электропроводность раствора, о чем свидетельствуют следующие данные:
СKCl, н | 0,01 | 0,1 | 1 | 2 |
α, % | 94,2 | 86,2 | 75,6 | 71,2 |
Однако падение α объясняется не образованием молекул, а увеличением тормозящего действия ионной атмосферы. В связи с этим α сильных электролитов называется кажущейся степенью диссоциации.
Для оценки состояния ионов в растворе пользуются величиной, называемой активностью.
Под активностью иона понимают ту эффективную концентрацию его, соответственно которой он действует при химических реакциях. Активность иона а равна произведению его моляльной концентрации (Сm) на коэффициент активности (f):
a = f∙Cm
Коэффициенты активности различных ионов различны. Они изменяются с изменением концентрации растворов. В концентрированных растворах f<1, а с разбавлением раствора f→1. Если f<1, то это указывает на сильное межионное взаимодействие, если f≈1, то это свидетельствует о слабом межионном взаимодействии (приложение, табл. 2).
Коэффициенты активности ионов зависят от состава и концентрации раствора, от заряда и природы иона и от других условий.
В разбавленных растворах природа иона мало влияет на значение f. Поэтому приближенно можно считать, что в разбавленных растворах коэффициент активности иона в данном растворителе зависит только от заряда иона и ионной силы раствора I, которая равна полусумме произведений концентрации Cm каждого иона на квадрат его заряда z :
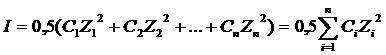
Приближенно коэффициент активности иона в разбавленном растворе можно также вычислить по формуле
![]() (табл. 2).
(табл. 2).
6. Ионно-обменные реакции в растворах
Если смешать разбавленные растворы двух электролитов АВ и СД, то раствор будет содержать все четыре возможных иона А и В, С и Д. При химическом взаимодействии растворов реакция протекает не между молекулами, а между ионами. При столкновении их образуются новые вещества:
АВ + СД = АД + СВ,
что можно выразить ионным уравнением
А+ + В – + С+ + Д – = А+ + Д – + В – + С+
В итоге установится равновесное состояние. Положение равновесия в подобной системе зависит от свойств образующихся веществ. Главную роль при этом играет вероятность возникновения того или иного из них, определяемая числом столкновений между соответствующими ионами.
Все ионные реакции могут быть обратимыми. Необратимыми они окажутся лишь в случае, если их продукты уходят из сферы реакции. Для равновесия ионных реакций можно сформулировать следующее положение: равновесие ионных реакций смещается в сторону образования менее диссоциированных веществ либо при удалении какого-либо вещества из «сферы реакции».

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



