Главенствующее положение кислорода в земной коре определяет то, что преобладающее число минералов, как по количеству, так и по массе — кислородные соединения. Кислород, согласно , входит в состав 1538 минералов.
Главными химическими элементами, образующими минералы земной коры, помимо кислорода, являются водород Н, кремний Si, алюминий А1, железо Fe, кальций Са, магний Mg, натрий Na, калий К. титан Ti, углерод С, марганец Мп, фосфор Р и сера S. Много минеральных видов образуют медь Си, свинец РЬ, мышьяк As, сурьма Sb, бор В, хлор С1, фтор F, уран U, ванадий V.
Количественное значение других элементов в образовании самостоятельных минералов несравненно ниже, таковы ниобий Nb, тантал Та, бериллий Be, никель N1, кобальт Со, литий Li и другие. Ряд элементов образуют очень ограниченное количество минералов (менее 10): платина Pt, индий In, скандий Sc, цезий Cs и др. Такие элементы, как, например, рубидий Rb, рений Re и некоторые другие, не образуют собственных минералов, они изоморфно рассеяны в кристаллических решетках других минералов.
Самый распространенный в природе класс минералов — силикаты (не менее 75% от всех минералов); самыми распространенными в земной коре минералами являются полевые шпаты (плагиоклаз, ортоклаз) и кварц, на долю которых согласно , приходится соответственно 55% и 12%.
Интересно распределение минералов по сингониям. Немецкий кристаллограф П. Грот (1843—1926) статистически пришел к такому закону: кристаллам более простого химического состава соответствует более высокая симметрия. Или, иначе говоря, чем сложнее состав кристаллов, тем обычно ниже их симметрия.
Статистическое распределение кристаллографически хорошо изученных минералов по сингониям приводится ниже (по ):
Триклинная.......................... 88(6,5%)
Моноклинная.................. 393(30,0%)
Ромбическая..................... 279(21,0%)
Тригональная....................... 143(11,5%)
Тетрагональная................. 131 (10,0 %)
Гексагональная................ 103(8,0%)
Кубическая........................ 171 (13,0%)
Тема 2 Химический состав минералов, морфология минеральных индивидов и агрегатов, физические свойства минералов ( 1час)
План лекции:
1. Типы химических связей в минералах. Атомные и ионные радиусы.
2. Понятие о координационных числах и плотнейшей упаковке шаров.
3. Изоморфизм, виды и типы изоморфизма.
4. Полиморфизм и его генетическое значение.
5. Форма и облик кристаллов.
6. Текстуры и структуры минеральных агрегатов.
7. Физические свойства минералов
Для выяснения химического состава минерала производят его химический анализ. В результате пересчета данных анализа определяют химическую формулу минерала. Формулы могут быть эмпирическими, показывающими только химический состав, и структурными, дающими представление о пространственном расположении атомов в минерале и их связи между собой.
Для некоторых минералов структурные формулы еще не установлены. Но благодаря рентгеновским методам исследования во многих случаях удалось определить взаимоотношение атомов в кристаллических структурах минералов. Этими вопросам/, связи химизма со строением вещества и его свойствами, как уже указывалось ранее, занимается кристаллохимия.
В минералах важно выявить катионы и анионные комплексы, характеризующие типы кристаллических структур. При написании формул минералов анионные комплексы отделяются от катионов квадратными скобками, например, сидерит Fe[CO3], барит Ba[SO4], сподумен LiAl(Si3O8], микроклин K[AlSi3O8]HF.
Следует иметь в виду, что эмпирические формулы минералов не отображают особенностей их внутреннего строения и в минералогии они в настоящее время заменены структурными формулами.
Формула минерала ковеллина может быть изображена как CuS, однако в ковеллине имеется два вида ионов серы — одиночные S2- и спаренные [S2]2~ —и два вида ионов меди Си+ и Си2+. Поэтому формулу ковеллина нужно писать Cu2S - CuS2.
В минералогии нередко различают безводные и водные минералы (сульфаты, фосфаты, карбонаты и др.). К водным относятся те минералы, которые имеют в своем составе электрически нейтральные молекулы воды.
Вода в составе минералов может быть связанной и свободной. Связанная, или кристаллизационная, вода входит в кристаллическую решетку минералов, занимая в ней определенные места. Примерами могут быть некоторые водные карбонаты и сульфаты, например гипс Ca[SO4]*2H2O. Свободная вода не участвует в строении кристаллической решетки минералов, количество ее может быть различным в зависимости, например, от температуры. Примерами свободной воды является вода цеолитов (см. цеолиты). И, конечно, вся гигроскопическая вода, удерживающаяся в тончайших трещинах минералов и пород силами поверхностного натяжения, также является свободной и удаляется при нагревании до 110°С.
Гидроксилсодержащие минералы в строгом смысле не могут быть названы водными. Между электрически нейтральной молекулой воды Н2О и отрицательно заряженным ионом гидроксила (ОН)"~ существует принципиальная разница. Гидроксил (ОН)~ может замещать в минералах такие ионы, как С1~ и F~, он прочно удерживается в кристаллических решетках, этими свойствами молекулы воды не обладают.
Химический состав многих минералов нельзя точно отобразить формулой. Это зависит от различных механических примесей в минералах и способности некоторых соединений образовывать изоморфные смеси или твердые растворы; по своей однородности последние аналогичны жидким растворам.
Изоморфизм — свойство атомов (или ионов) одних веществ замещать в структуре атомы (или ионы) других. Явления изоморфизма очень широко распространены в минералах. Так, химический состав минерала вольфрамита отображается формулой (Fe, Mn) [WO4]. Он представляет собой изоморфную смесь, где атомы марганца замещают, в структуре атомы железа, и на держащих минералах, где он и обнаруживается в наибольших количествах (например, в слюдах, в карналлите — KCl-MgCI2X6Н2О), и из которых извлекается.
Полиморфизм. В переводе с греческого слово «полиморфизм» означает многоформность. Это явление до известной степени противоположно изоморфизму и заключается в том, что одинаковые по химическому составу вещества образуют различные структуры.
Полиморфными могут быть элементы и сложные соединения. Происхождение различных полиморфных модификаций (разновидностей) связано с различием в условиях их образования. Каждая из модификаций имеет свою структуру, а отсюда и свои специфические свойства.
Хорошим примером полиморфизма углерода являются минералы алмаз и графит. Свойства их совершенно различны: алмаз самый твердый из минералов (твердость 10), графит имеет твердость 1. Плотность алмаза 3,5, графита 2,2. Алмаз кристаллизуется в кубической сингонии, графит — в гексагональной. Причина столь различных свойств указанных минералов объясняется их структурой, т. е. расположением атомов углерода (рисунок 8).
Связь атомов углерода в графите менее прочная, чем в алмазе, структура графита листоватая, в виде плоских гексагональных сеток. Значительные расстояния между этими сетками и определяют его свойства: легкую расщепляемость, меньшую плотность и др.
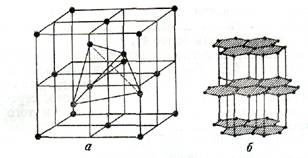
Рисунок 8 Структуры алмаза (а) и графита (б)
Несколько полиморфных модификаций имеет и сера; в природных условиях устойчивой является лишь сера ромбической сингонии. Примерами полиморфных модификаций соединений могут служить кальцит (Са[СО3] тригональной сингонии) и арагонит (Са[СО3] ромбической сингонии), пирит (FeS2 кубической сингонии) и марказит (FeS2 ромбической сингонии), полиморфные модификации кварца (S1O2) и т. д.
Различают два вида полиморфизма. Первый вид — энантио-тропия — характеризуется обратимостью (переходом) поли морфных модификаций из одной в другую при определенных температурах и давлениях. Примером энантиотропии могут служить переходы кварца в высокотемпературную разновидность S1O2 — тридимит, а также переходы алмаза в графит. Второй вид — монотропия — одна полиморфная модификация (нестабильная) может переходить в другую (стабильную), но обратный переход невозможен. Примером монотропии является переход марказита в пирит (обратного перехода нет).

Изометричные кристаллы или минеральные зерна имеют одинаковые размеры во всех направлениях. Таковы, например, кристаллы граната, магнетита, алмаза, сфалерита, пирита.
У минералов удлиненного типа значительно преобладает длина над шириной. Среди них встречаются столбчатые, игольчатые, волокнистые, нитевидные разновидности. Примером удлиненных минералов могут служить турмалин, берилл, натролит, хризотил-асбест, гипс-селенит.
Уплощенные минералы отличаются тем, что их толщина меньше ширины. Они представлены таблитчатыми, тонкотаблитчатыми, листоватыми и тонкочешуйчатыми разновидностями. Уплощенный вид и его разновидности имеют ильменит, гематит, биотит, хлорит.
К промежуточным удлиненно-уплощенным разновидностям принадлежат колумбит, барит, гипс; к уплощенно-удлиненным — кианит, сподумен, волластонит.
Внешний облик ограненных минералов или их габитус определяется преобладанием граней тех или иных простых форм. Габтусможет быть кубическим, октаэдрическим, тетраэдрическим, призматическим, дипирамидальным и т. д. Так, кубический га6итус имеют флюорит, пирит, галит; тетраэдрический — сфалерит, тетраэдрит; призматический — диопсид, скаполит, берилл; дипирамидальный — шеелит, циркон и т. д.
Габитус минералов зависит от условий их образования. Так, кварц магматической стадии имеет изометричный облик, образованный гранями двух равномерно развитых ромбоэдров, похожих на гексагональную дипирамиду без призмы; кварцы удлиненного габитуса (призматические) — низкотемпературные. Короткопризматический или дипирамидальный габитус циркона характерен для щелочных пород и пегматитов, а удлиненно-призматический — для гранитов и гранитных пегматитов.
При характеристике формы минералов также следует учитывать штриховку на гранях (кварц, топаз, турмалин и др.), двойники (ортоклаз, касситерит, кварц, гипс и др.), закономерные срастания, скульптуру граней и другие признаки. Все они хорошо помогают диагностике минералов: например, характерным отличием топаза от кварца является его грубая вертикальная штриховка на гранях призмы в отличие от горизонтальной штриховки у кварца.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |



