А. К. ШИРЯЕВ
КВАНТОВАЯ МЕХАНИКА
И КВАНТОВАЯ ХИМИЯ
Учебно-методическое пособие
Самара
Самарский государственный технический университет
2010
| ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «САМАРСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ» |
Кафедра органической химии
А. К. ШИРЯЕВ
КВАНТОВАЯ МЕХАНИКА
И КВАНТОВАЯ ХИМИЯ
Учебно-методическое пособие
Самара
Самарский государственный технический университет
2010
Печатается по решению редакционно-издательского совета СамГТУ
УДК 539.19.01
Рецензент: доктор хим. наук
Ширяев А.К.
Ш Квантовая механика и квантовая химия: учеб.-метод. пособие / А.К. Ширяев. – Самара: Самар. гос. техн. ун-т, 2010. – 119 с.: ил.
Рассмотрены постулаты квантовой механики и методы квантовой химии, используемые в настоящее время для расчетов органических молекул. Приведены основные команды квантово-химической программы GAMESS, а также примеры расчета электронной структуры и ИК спектров простых молекул, энергии активации и барьеров вращения.
Предназначается для студентов и аспирантов химических и химико-технологических специальностей.
УДК 539.19.01
Ó , 2010
Ó Самарский государственный
технический университет, 2010
ВВЕДЕНИЕ
В отличие от традиционной химии, рассматривающей молекулу как систему связанных атомов, квантовая механика описывает молекулу как набор ядер и электронов. Электроны и ядра принципиально отличаются от частиц классической механики, что экспериментально было обнаружено в начале XX века Резерфордом, Франком, Герцем, Вавиловым и др. Введение понятия кванта Планком, принципа неопределенности Гейзенбергом, построение Бором модели атома в итоге привели к созданию новой науки – квантовой механики.
Квантовая механика теоретически обосновала основные химические представления и закономерности, включая периодический закон . Развитие квантовой механики привело к созданию компьютерных расчетных методов, точность которых превышает экспериментальную для простейших систем. Квантовая химия использует эти методы для теоретического исследования химических частиц и их превращений. В результате квантовых расчетов можно получить геометрическое строение молекулы и относительные энергии ее возможных изомеров, скорость превращения одной молекулы в другую, а также различные свойства молекулы – дипольный момент, поляризуемость, константы спин-спинового взаимодействия и пр.
В настоящее время квантово-химические расчеты все чаще используются химиками-исследователями, поэтому целью данного пособия является развитие навыков самостоятельного проведения расчетов, для чего изложение основных понятий квантовой химии объединено с примерами расчетов и расчетными и учебными заданиями.
1. Основные постулаты квантовой механики
Полное описание состояния классической физической системы осуществляется заданием уравнений движения и начальных значений координат и скоростей. Используя эти данные, всегда можно полностью определить поведение системы во времени. Начальные значения координат и скоростей необходимо измерить, и здесь возникает коренное различие между классической и квантовой механикой. Классическая механика допускает возможность неограниченного уточнения любого измерения. В квантовой механике измерение какого-либо свойства микрочастицы неизбежно вызывает изменение ее состояния. Эта особенность описания микрочастиц сформулирована Гейзенбергом в принципе неопределенности (Dx · Dpx ³ h, Dy · Dpy ³ h, Dz · Dpz ³ h, DE · Dt ³ h и пр.): нельзя со сколь угодно высокой точностью одновременно измерить координату и импульс микрочастицы, а также, например, измерить изменение энергии и момент времени, когда это изменение произошло. Другими словами, локализация частицы в какой-либо малой области пространства требует физических условий, неблагоприятных для измерения ее количества движения; и наоборот, условия, необходимые для точного измерения количества движения частицы, исключают возможность локализации ее в достаточно малой области пространства. Уточнение одной из физических величин всегда увеличивает неопределенность другой. В результате описание микрообъектов осуществляется меньшим числом величин, т. е. является менее подробным. Поэтому квантовая механика не может делать строго определенных предсказаний относительно будущего поведения микрообъекта. Ее задача состоит лишь в определении вероятности получения того или иного результата при измерении. Для описания системы частиц в квантовой механике используется некая волновая функция, свойства которой отражены в следующих постулатах.
Постулат 1. Состояние частицы (или системы частиц) задано, если известна волновая функция Ψ(q). Квадрат модуля волновой функции |Ψ(q)|2dq.определяет распределение вероятностей значений координат частицы (или системы частиц).
Волновая функция должна удовлетворять следующим требованиям:
- функция должна быть непрерывной;
- функция должна быть однозначной;
- квадрат ее модуля должен быть интегрируемым, т. е. должен существовать интеграл 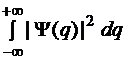 ;
;
- функция должна быть нормированной, т. е. этот интеграл должен быть равен единице: 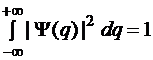 .
.
Функция Ψ(q) зависит от координат q всех частиц исследуемой системы и может быть как действительной, так и комплексной.
Постулат 2. Волновые функции подчиняются принципу суперпозиции: если в состоянии с волновой функцией Ψ1(q) некоторое измерение приводит к результату Х1, а в состоянии Ψ2(q) – к результату Х2, то всякая функция вида Ψ = с1Ψ1(q) + с2Ψ2(q) описывает такое состояние, в котором измерение дает либо результат Х1, либо Х2.
Постулат 3. Всякой физической величине G в квантовой механике сопоставлен линейный самосопряженный оператор Ĝ. Единственно возможными величинами, которые может иметь эта физическая величина, являются собственные значения g операторного уравнения Ĝ Ψ = g Ψ.
Постулат 4. Возможная волновая функция состояния системы получается при решении стационарного дифференциального уравнения Шрёдингера
![]()
где ![]() – оператор Гамильтона, представляющий собой сумму операторов кинетической и потенциальной энергии
– оператор Гамильтона, представляющий собой сумму операторов кинетической и потенциальной энергии 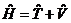 , Е – энергия системы, которая может принимать как дискретные, так и непрерывные значения, являющиеся собственными значениями оператора Гамильтона.
, Е – энергия системы, которая может принимать как дискретные, так и непрерывные значения, являющиеся собственными значениями оператора Гамильтона.
Постулат 5. Если произвести многократные измерения какой-либо динамической переменной g системы, находящейся в состоянии Ψ, то на основании результатов этих измерений можно определить ее среднюю величину. Эта средняя величина вычисляется по формуле
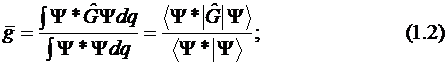
где ![]() – функция, комплексно сопряженная функции
– функция, комплексно сопряженная функции ![]() .
.
2. Решение уравнения Шрёдингера
для атома водорода
Оператор Гамильтона состоит из двух частей – оператора кинетической энергии (![]() ) и оператора потенциальной энергии (
) и оператора потенциальной энергии (![]() ). Первый представляет собой оператор Лапласа (в атомных единицах), второй в случае атома водорода выражается в соответствии с законом Кулона в виде 1/r (также в атомных единицах):
). Первый представляет собой оператор Лапласа (в атомных единицах), второй в случае атома водорода выражается в соответствии с законом Кулона в виде 1/r (также в атомных единицах):
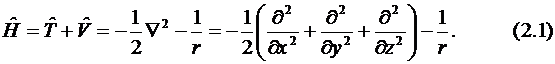
Так как атом водорода обладает сферической симметрией, то для решения уравнения необходимо перейти к сферическим координатам (рис. 2.1):
x = r sin θ cos φ;
y = r sin θ sin φ;
z = r cos θ;
0 ≤ r < ∞; 0 ≤ θ ≤ π; 0 ≤ φ ≤ 2π.
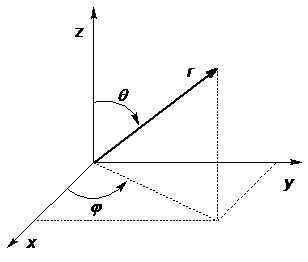
Р и с. 2.1. Связь сферических координат с декартовыми
При решении уравнения Шрёдингера (1.1) в сферических координатах переменные (r, θ, φ) легко разделяются, что приводит к следующим функциям для атома водорода:
![]()
где ![]() – радиальная часть функции,
– радиальная часть функции, ![]() – часть функции, зависящая только от угловых переменных (сферическая гармоника), N – нормировочный множитель.
– часть функции, зависящая только от угловых переменных (сферическая гармоника), N – нормировочный множитель.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 |



