2. Во вторую пробирку добавляют 1 каплю 1 % раствора CH3COOH и нагревают. Хлопьевидный осадок белка выпадает скорее и полнее, т. к. при подкислении рН раствора приблизится к изоэлектрической точке белка.
3. В третью пробирку добавляют 0,5 мл 10 % раствора CH3COOH и нагревают. Даже при кипячении осадка не образуется, поскольку белковые мицеллы перезаряжаются и несут положительный заряд, что повышает их устойчивость.
4. В четвертую пробирку приливают 5 капель 10 % CH3COOH и 2 капли насыщенного раствора NaCl и нагревают. Выпадает белый хлопьевидный осадок, т. к. частицы белка теряют заряд вследствие взаимодействия белка с разноименно заряженными ионами хлористого натрия, а так же теряют гидратную оболочку.
5. В пятую пробирку добавляют 2 капли 10 % раствора NaOH, создавая щелочную среду. При кипячении жидкости осадка не образуется, поскольку в щелочной среде отрицательный заряд на частицах белка увеличивается.
Результаты занести в таблицу 3. Отметить положительную реакцию осаждения плюсом, а отрицательную - минусом. Указать в каждом случае причины появления или отсутствия осадка белка.
Таблица 3
Нейтральная среда | Слабокислая среда | Сильнокислая среда | Сильнокислая среда + электролит | Щелочная среда |
ВЫВОД:
Лабораторная работа №5
ОСАЖДЕНИЕ БЕЛКОВ СОЛЯМИ ТЯЖЕЛЫХ МЕТАЛЛОВ
ПРИНЦИП РАБОТЫ:
Осаждение белков солями тяжелых металлов (в отличие от высаливания) происходит при небольших концентрациях солей. Белки при взаимодействии с солями тяжелых металлов (свинца, меди, серебра, ртути и др.) адсорбируют их, образуя с ними солеобразные и комплексные соединения, растворимые в избытке этих солей (за исключением солей AgNO3, HgCl2), но нерастворимые в воде. Соли тяжелых металлов вызывают необратимое осаждение белков, т. е. денатурацию. Растворение осадка в избытке солей называется адсорбционной пептизацией. Данное явление происходит вследствие возникновения одноименного положительного заряда на частицах белка.
РЕАКТИВЫ и ОБОРУДОВАНИЕ:
1) раствор яичного белка; 2) CuSO4, 5 %; 3) (CH3COO)2Pb, 5 %; 4) AgNO3, 3 %; 5) FeCl3, 5 %; 6) пробирки.
ХОД РАБОТЫ:
В 4 пробирки наливают по 1-2 мл раствора белка и по каплям добавляют растворы солей: в 1-ую – уксуснокислого свинца; во 2-ую - сернокислой меди; в 3-ю – хлорного железа; в 4-ую – азотнокислого серебра (до выпадения осадков).
Затем прибавляют избыток указанных солей.
РЕЗУЛЬТАТЫ и ВЫВОД:
Лабораторная работа №6
ОСАЖДЕНИЕ БЕЛКОВ
КОНЦЕНТРИРОВАННЫМИ МИНЕРАЛЬНЫМИ КИСЛОТАМИ
ПРИНЦИП РАБОТЫ:
Концентрированные минеральные кислоты вызывают резкую дегидратацию белковых частиц и нейтрализацию их заряда, при этом происходит образование комплексных соединений. В результате происходит денатурация белка. Ортофосфорная кислота осадка не дает. В избытке всех минеральных кислот, за исключением азотной, выпавший в осадок белок растворяется.
РЕАКТИВЫ и ОБОРУДОВАНИЕ:
1) раствор яичного белка; 2) HNO3, конц.; 3) H2SO4, конц.; 4) HCl, конц.; 5) пробирки.
ХОД РАБОТЫ:
В 3 пробирки наливают по 1 мл кислот: в 1-ую – серной; во 2-ую – азотной; в 3-ю – соляной. Пробирки наклоняют под углом 45 º и осторожно (из пипетки) наслаивают по стенке раствор белка (пробирку следует держать отверстием от себя!). На границе белка и кислоты появляется белое кольцо.
Пробирки осторожно встряхивают и добавляют в них избыток соответствующих кислот.
РЕЗУЛЬТАТЫ и ВЫВОД:
Лабораторная работа №7
ОСАЖДЕНИЕ БЕЛКОВ ОРГАНИЧЕСКИМИ ВЕЩЕСТВАМИ
ПРИНЦИП РАБОТЫ:
Органические кислоты вызывают необратимое осаждение белков, чаще используют растворы трихлоруксусной и сульфосалициловой кислот. Сульфосалициловая кислота кроме белков осаждает также продукты их распада - высокомолекулярные пептоны и полипептиды. Трихлоруксусная кислота способна осаждать только белки и не осаждает продукты распада белков.
В органических растворителях (спирт, ацетон и др.) белки не растворяются и выпадают в осадок. В зависимости от природы белка для его осаждения требуются различные концентрации спирта. Спирт связывает воду, вызывая дегидратацию мицелл белка и неустойчивость их в растворе. При осаждении спиртом раствор белка должен быть нейтральным или слабокислым, но не щелочным. Реакция облегчается присутствием электролита хлористого натрия вследствие снятия заряда с частиц белка. Реакция осаждения белка спиртом или кратковременным действием спирта обратима при охлаждении. Если осадок быстро отделить от спирта, то белок может сохранить нативное состояние.
РЕАКТИВЫ и ОБОРУДОВАНИЕ:
1) сульфосалициловая кислота, 20 %; 2) трихлоруксусная кислота, 10 %; 3) этиловый спирт; 4) раствор яичного белка; 5) пробирки.
ХОД РАБОТЫ:
В 3 пробирки отбирают по 5 капель раствора яичного белка.
В 1-ую пробирку добавляют 2 капли раствора сульфосалициловой кислоты. Во 2-ую – 2 капли трихлоруксусной кислоты. В 3-ю приливают 15-20 капель этилового спирта (раствор мутнеет), затем добавить 1 каплю насыщенного раствора хлористого натрия.
РЕЗУЛЬТАТ и ВЫВОД:
КОНТРОЛЬНЫЕ ВОПРОСЫ:
Объясните факторы устойчивости коллоидного раствора белка.
От чего зависит заряд белка в водном растворе?
Что такое изоэлектрическая точка белка? Какой заряд будут иметь водные растворы белка с избыточным количеством свободных карбоксильных групп?
Какой заряд будут иметь водные растворы белка с избыточным количеством аминогрупп? В какой среде будет ИЭТ такого белка?
Чем обусловлены реакции осаждения белков? При каких температурных условиях возможно осаждение белков?
Что такое обратимое и необратимое осаждение белков?
Что такое денатурация белка? Дайте характеристику денатурирующим агентам?
Что происходит с белковой молекулой при высаливании?
Тема 3
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ БЕЛКА. ОЦЕНКА НА ОСНОВАНИИ ФОТОМЕТРИИ ПРОДУКТОВ ЦВЕТНОЙ РЕАКЦИИ. ПОСТРОЕНИЕ КАЛИБРОВОЧНЫХ ГРАФИКОВ
Наиболее распространенным методом количественного определения белка является метод, основанный на биуретовой реакции, с последующей фотометрией цветных продуктов реакции. Биуретовая реакция открывает пептидную связь в белке.
Метод оценки количества вещества базируется на использовании калибровочного графика, а также концентрации стандартных проб, обрабатываемых параллельно с опытными в одинаковых с ними условиях.
Построение калибровочного графика:
1. Построение калибровочной кривой начинается с приготовления ряда разведений стандартного раствора исследуемого вещества. Стандартный раствор содержит вещество в известной концентрации. Разведения стандартного раствора должны охватывать диапазон физиологических концентраций и выходить за пределы их минимальных и максимальных величин.
(!) Например, при исследовании содержания белка в сыворотке крови концентрация стандартного вещества (альбумина) должна быть в интервале от 40 до 120 г/л (при физиологической концентрации общего белка 65-85 г/л).
Ряд калибровочных разведений получают путем разбавления основного стандартного раствора.
2. Затем ведут обработку стандартных растворов аналогично опытным пробам. Измеряют оптическую плотность калибровочных растворов и опытной пробы на одном и том же приборе. Измерения оптической плотности начинают со стандартного раствора наименьшей концентрации.
3. Усредненные (соответствующие отдельным концентрациям) значения оптической плотности - D (абсорбции - А, экстинкции - Е) наносят на миллиметровую (калибровочную) бумагу. На оси абсцисс (горизонтальной) с соблюдением одинаковых интервалов в равномерно возрастающей концентрации откладывают показатели содержания вещества в стандартном растворе; на оси ординат (вертикальной) - соответствующие им величины оптической плотности (рисунок 5).
Зависимость между концентрацией вещества в стандартных (калибровочных) пробах и оптической плотностью, соответствующей этим пробам, отражается линией, построенной по точкам. Строить калибровочный график следует не менее чем по пяти точкам.
Калибровочная кривая прокладывается таким образом, чтобы по возможности большее число точек (например, 3 из 5) лежало на линии, а остальные располагались близ нее, равномерно отклоняясь в ту и другую стороны. Отдельные точки, значительно смещающиеся от калибровочной кривой и обычно являющиеся результатом грубой ошибки в определении, исключаются из учета.
Расположение кривой определяют так, чтобы она исходила из нулевой отметки под углом ~45 ° к осям координат: при этом достигается наибольшая точность измерений. Последней способствует также выбор оптимального, достаточно крупного масштаба.
Определение количества вещества в опытной пробе с использованием калибровочного графика:
1. Определение оптической плотности раствора вещества с неизвестной концентрацией (опытной пробы). Исследование проводят против контроля, либо, если опытная проба слабоокрашенная, смотрят против дистиллированной воды.
2. Полученное значение откладывают на калибровочном графике путем опускания перпендикуляров: - с оси ординат на калибровочную кривую; - с кривой на ось абсцисс.
3. Полученное в результате значение концентрации на оси абсцисс и является искомой концентрацией.
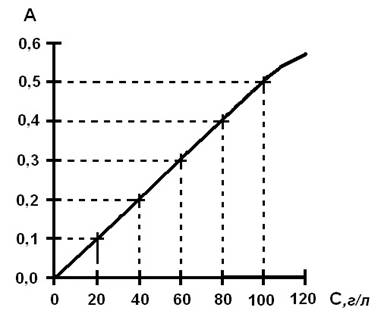
Рисунок 5. Схема построения калибровочного графика.
Лабораторная работа №8
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ БЕЛКА
ПРИНЦИП МЕТОДА:
Белки реагируют в щелочной среде с сернокислой медью с образованием соединений, окрашенных в фиолетовый цвет (биуретовая реакция). Реакция обусловлена образованием биуретового комплекса в результате соединения меди с пептидной группировкой белка.
РЕАКТИВЫ и ОБОРУДОВАНИЕ:
1) NaCl, 0,9 %; 2) биуретовый реактив: 0,15 г CuSO4 · 5H2O и 0,6 г NaKC4H4O6 · 4H2O (виннокислый натрий-калий, или сегнетова соль) растворяют в 50 мл Н2О, при энергичном перемешивании приливают туда 30 мл 10%-ого раствора NaOH (свободного от Na2CO3), добавляют 0,1 г KI и раствор доводят водой до 100 мл. Хранят в полиэтиленовой склянке; 3) стандартный раствор альбумина (БСА – бычий сывороточный альбумин), 10 мг белка в 1 мл; 4) раствор сыворотки с разведением в 10 раз: взять 1 мл сыворотки крови довести дистиллированной водой или 0,9 % раствором NaCl до объема 10 мл. Полученная концентрация белка будет соответствовать 6,5-8,5 г/л; 5) пробирки, пипетки; 6) ФЭК.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |



