В другом варианте серная кислота, содержащаяся в воздухе больших городов, образует туман из мельчайших капелек. Попадая на растение в больших концентрациях, она вызывает ожоги, а в малых очень быстро проникает через устьица внутрь межклетников, энергично отнимает воду от углеводов, образующихся в процессе фотосинтеза, вызывая гибель клеток и обугливание тканей листа:
С12Н22О11 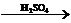 12С + 11Н2О.
12С + 11Н2О.
Живая клетка отличается от мертвой хорошо выраженным плазмолизом.
Оборудование, реактивы, материалы
1) микроскоп; 2) предметные и покровные стекла; 3) эксикатор; 4) бритва; 5) концентрированная серная кислота, разведенная дистиллированной водой (1:1); 6) 1 М раствор сахарозы; 7) листья разных древесных растений.
Ход работы
Берут листья разных древесных растений, растущих в относительно чистой зоне, но встречающихся в уличных посадках города. Из листа растения вырезают пластинки размером 2-4 см2 и кладут в эксикатор над серной кислотой, разбавленной в соотношении 1:1. Пластинки выдерживают в течение 2-3 часов, затем делают срезы, окрашивают «нейтральным красным» и плазмолизируют молярным раствором сахарозы, просасывая его между предметными и покровными стеклами. Просматривают под микроскопом в разных полях зрения и подсчитывают оставшиеся живыми клетки по возникшему плазмолизу. Чем больше осталось живых клеток, тем лучше растение выносит обезвоживание.
Строят ряд устойчивости клеток разных растений к обезвоживанию (устойчивости к сернистому газу).
Можно одновременно определить и содержание воды в вырезанных пластинках листа. В этом случае можно узнать не только число оставшихся живых клеток, но и при каком содержании воды устойчивость выше.
В случае отсутствия древесных растений можно использовать комнатные.
Работа № 7. Влияние низких температур
на коагуляцию белков у растений
Большинство растений средних и северных широт подвергается действию низких температур. Устойчивость к этому фактору определяется генетическими свойствами растений, их физиологическим состоянием. Особенно сильно страдают южные интродуценты в ботанических садах, также сельхозкультуры, ввезенные из южных широт в более северные (кукуруза, томаты, перец, в отдельные годы – картофель). Это выражается в обратимой или необратимой потере листьями тургора, частичной или полной гибели ассимилирующей поверхности. Страдают в первую очередь молодые листья, плохо одревесневшие побеги. Это явление сглаживается при наличии в клеточном соке защитных веществ (криопротекторов), роль которых выполняют сахара, свободные аминокислоты, соли органических и неорганических кислот. Сахара образуются в процессе фотосинтеза и их накопление у определенных групп растений смягчает или предотвращает коагуляцию белков.
Оборудование, реактивы, материалы
1) центрифуга; 2) центрифужные пробирки; 3) термометр; 4) ступки с пестиками; 5) смесь; снег-соль (3:1); 6) сахароза; 7) дистиллированная вода; 8) листья различных растений.
Ход работы
1. Взвесить 2-3 г молодых листьев акации белой или катальпы (неморозостойкие породы), тополя черного (морозостойкая порода) или листья комнатных растений, растереть в ступке с 4 мл воды, добавив 6 мл при смывании, отделить обрывки тканей центрифугированием и разлить зеленый раствор хлорофилл-протеида в пробирки. Следует отметить, что у комнатных растений зимой белок образуется плохо, поэтому надо увеличивать навеску до 3-5 г.
Заморозить растворы во всех пробирках в смеси снег – соль или лед – соль, рассматривая их через каждые 5 мин; отметить разницу в замерзании растворов от разных растений.
Растопить образовавшийся лед и подвергнуть растворы центрифугированию. Отметить разницу в величине осадка, представляющего коагулированный хлорофилл-белковый комплекс.
Опыт показывает разное время замерзания растворов и разную степень коагуляции белков у различных растений при замораживании.
2. Подготовить растертый образец, как указано выше, и до замораживания добавить в пробирку сахарозу до полного ее растворения при встряхивании и перемешивании. Заморозить растворы хлорофилл-белкового комплекса с сахарозой и без нее, проследить коагуляцию белка и защитное действие сахарозы.
Использовать следующую градацию;
1. Начало замерзания (гомогенная масса с кристаллами льда) – «+».
2. Частичное замерзание (множественные кристаллы льда, но не сплошной слой) – «++».
3. Полное замерзание (появление сплошного слоя льда; при перевертывании пробирки вода не выливается) – « + + + ».
Результаты записать в таблицу
Вариант | Время, мин | Величина осадка, мм | |||||
5 | 10 | 15 | 20 | 25 | 30 | ||
Приготовление охладительной смеси
К трем частям снега или битого льда добавить одну часть поваренной соли, тщательно перемешать лопаточкой (температура должна быть –20 °С). Изолировать смесь в ведерке плотной бумагой. Лед предварительно наморозить в морозилке и сложить в 2-3-литровый широкогорлый термос.
Для охлаждения можно пользоваться и сухим льдом, однако его нельзя хранить в замкнутом пространстве (термосе), т. к. при освобождении газа может быть взрыв.
Работа № 8. Определение устойчивости растений
к засолению почвы и воздуха
На территории нашей страны и сопредельных государств встречаются засоленные почвы, которые особенно характерны для засушливых районов. Наиболее широко распространены засоленные почвы в Казахстане, на юге Западной Сибири, Среднем и Нижнем Поволжье, на юге Украины, Северо-Восточном Предкавказье, Среднеазиатских государствах. Это почвы, содержащие в своем профиле легкорастворимые соли в токсичных количествах. Влияние таких солей на растения – мощный экологический фактор, сдерживающий их нормальный рост. В основном засоление почвы в той или иной степени вызывается следующими солями: NaCl, Na2SO4, Na2CO3, MgCl2, MgSO4.
В районах широкого распространения соленых озер и солончаков (озерные системы Аральского региона Туркмении, озера Тувы, Хакасии) большую роль в переносе солей играют ветровые процессы. При переносе солей ветром на поверхности суши может отлагаться (по подсчетам Ф. Кларка) от 2 до 20 т легкорастворимых солей на 1 км2. Для степных экосистем и полупустынь Закавказья приводится цифра 47 т на км2 в год (Ковда, 1973). Эти соли попадают на растения и воздействуют на них в виде солевой пыли, в виде растворов (с утренней росой), переносятся на огромные расстояния и выпадают в виде солевых осадков. Из почвенных растворов засоленных почв растения с трудом извлекают минеральные вещества и воду для своей жизнедеятельности. Соли также применяются (преимущественно NaCl) на улицах городов для борьбы с гололедом, их растворы проникают в почву и наносят большой вред растениям.
В данной работе приводятся три опыта, охватывающие все вышеприведенные случаи повреждения растений. При этом они могут ставиться как отдельно, так и вместе в зависимости от цели и продолжительности занятия (2 или 4 часа). В опытах могут использоваться соли тяжелых металлов, являющиеся сильными загрязнителями биосферы.
Оборудование, реактивы, материалы
1) большие пробирки или цилиндры на 100 мл; 2) штативы к пробиркам; 3) мерные пробирки или цилиндры; 4) технохимические весы; 5) разновесы; 6) острая бритва; 7) соли NaCl, Na2CO3; 8) вода; 9) веточки разных растений с 3-4 одинаковыми небольшими листьями (березы, тополя, яблони и др.).
Опыт 1
Влияние опудривания растений солями на их устойчивость
Опыт иллюстрирует влияние на растения ветровых отложений солей.
Ход работы
Ветки разных древесных растений взвешивают и уравнивают (путем подрезания) до одинаковой массы, выдерживают в воде 15 мин до их насыщения влагой, вынимают, обсушивают фильтровальной бумагой, обрабатывают смачивателем (1-2 %-й раствор зеленого мыла или ОП-7, ОП-10). Роль смачивателя в естественной обстановке выполняют растворы некоторых солей, образующих гель, гуминовые и фульвокислоты, содержащиеся в эоловых переносах, а главное – выделения самих растений.
После этого срез ветки быстро обновляют бритвой и ставят в сосуд (большую пробирку или цилиндр) со строго дозированным количеством водопроводной отстоянной воды. Отверстие сосуда плотно закрывают листочком станиоля, пробирки надписывают.
Соли (NaCl, Na2CO3) растирают в ступке до мелкодисперсного состояния. Кусочки ваты рыхло накручивают на палочку, затягивают ниткой и используют как кисточку, которой опудривают равномерно листья, черешки, кору подопытных растений солями. Контролем служат растения без опудривания.
Ветки выставляют на рассеянный свет на 1-2 недели, избегая сильного их нагревания. Затем учитывают такие признаки, как потеря тургора, появление инфильтрационных просвечивающих пятен, появление некрозов (отмершей ткани), подсыхание краев листа, их скручивание и др. Одновременно измеряют поглощение воды из пробирок (цилиндров), используя мерную пробирку.
В результате решаются следующие задачи.
1. Определяются степень и характер повреждения листьев разными солями, при этом определяется на глаз (в процентах от всей площади листьев) площадь, занятая некрозами.
2. Сравнивается степень поглощения воды ветками разных растений при опудривании различными солями.
3. Проводится сравнительная оценка солеустойчивости разных растений к разным видам солей.
Опыт 2
Опыт имитирует влияние солевых осадков на лист (или выпавшей росы на солевой покров листа), т. е. действие на лист раствора солей.
Ход работы
Ветки разных видов древесных растений с одинаковым числом листьев выравнивают путем взвешивания, как и в предыдущем опыте, выдерживаются путем полного погружения в 5 %-е растворы солей (NaCl, Na2CO3) в течение 15, 30, 45 минут.
Контрольные ветви выдерживают в воде. Для опыта требуется не менее четырех веток каждого вида. После этого срезы быстро обновляют бритвой и ветви ставят в воду (одинаковое количество во всех опытах и контрольных вариантах). Испарение воды из пробирок предотвращают изолированием фольгой. Через 1-2 недели производится оценка состояния растений и измерение поглощенной воды по схеме, предложенной в предыдущем опыте. Делаются соответствующие выводы.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



